Реферат: Алифатические амины
Алифатические амины
Амины - производные аммиака, в которых атомы водорода замещены на углеводородные радикалы. Амины классифицируют по числу атомов водорода, замещенных на углеводородные радикалы. Различают первичные R-NH2, вторичные R2-NH и третичные R3-N амины.
Известны и соединения с четвертичным атомом азота - соли аммония - R4N+X-. В этом случае азот несет положительный заряд.
В зависимости от типа радикала различают алифатические и ароматические амины:
CH3NH2 CH3CH2NH2 CH2=CH-CH2-NH2 С6H5-NH2
Амины жирного ряда (алифатические амины)
Изомерия в ряду алифатических аминов связана с изомерией углеводородного радикала и количеством заместителей у атома азота.
Многие амины имеют тривиальные названия. По рациональной номенклатуре названия аминов образуются из названий углеводородных остатков, связанных с атомом азота и окончания -амин:
(CH3)2CH-NH2 (CH3)2CHCH2-NH2 CH3-NH-CH2CH3
изопропиламин изобутиламин метилэтиламин
По номенклатуре IUPAC для простых аминов используют рациональные названия. По правилам IUPAC к названию углеводородного радикала добавляют окончание -амин. Углеводородная цепь начинается с атома углерода, соединенного с аминогруппой: CH3CH2CH2CH-NH-CH3 1-метилбутиламин. При наличии других функциональных групп аминогруппа обозначается приставкой: NH2-CH2CH2-OH – 2-аминоэтанол.
Способы получения алифатических аминов
1. Аммонолиз галогеналканов.
При нагревании галогеналканов со спиртовым раствором аммиака в запаянных трубках образуется смесь соединений. При взаимодействии аммиака с галогеналканами образуются первичные алкиламины. Моноалкиламины являются более сильными нуклеофилами, чем аммиак; они будут дальше реагировать с галогеналканом, давая значительные количества вторичных и третичных аминов и даже четвертичные соли аммония:
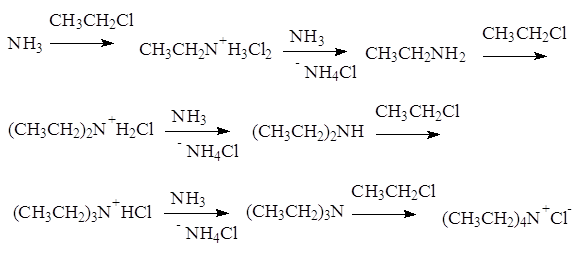
Аммонолиз галогенпроизводных относится к реакциям нуклеофильного замещения. В частности, реакция CH3CH2Cl+NH3 протекает по механизму:
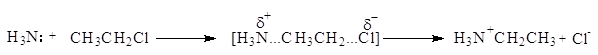
Поэтому первичные амины получают обычно другими способами.
2. Аммонолиз спиртов.
Состоит в замещении атомов водорода в аммиаке или амине на алкильные группы. Это важнейший способ синтеза аминов:
CH3OH + NH3 ® CH3NH2 + H2O
Аммонолиз спиртов реализован в значительных масштабах для синтеза низших алифатических аминов (метил- и этиламины). Они применяются в качестве топлива для жидкостных ракетных двигателей и как промежуточные продукты органического синтеза (получение других аминов, диметилгидразина, анионоообменных смол и анионоактивных веществ, пестицидов, карбаматов и дитиокарбаматов).
3. Синтез Габриэля.
Синтез Габриэля позволяет получать первичные амины, свободные от более высокоалкилированных продуктов. Алкилирование фталимида калия по механизму SN2 дает N-алкилфталимид, который можно легко гидролизовать до соответствующего амина:
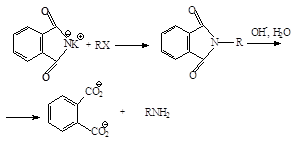
Фталимид получают при нагревании фталевого ангидрида с аммиаком:
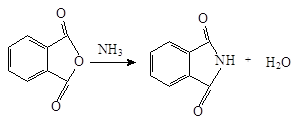
Фталимид обладает кислотными свойствами из-за делокализации отрицательного заряда имид-аниона на двух ацильных атомах кислорода. Он теряет протон, связанный с азотом, при взаимодействии с основанием типа гидроксида калия. В результате этой реакции образуется фталимид-ион – анион, который стабилизируется:
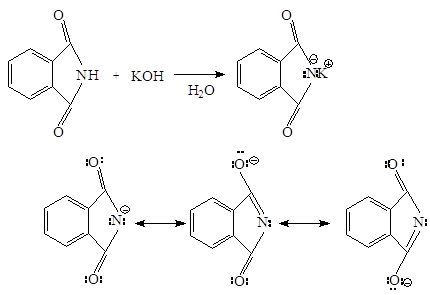
4. Восстановительное аминирование карбонильных соединений
Многие карбонильные соединения превращаются в амины в процессе восстановления в присутствии аммиака. Восстановление осуществляется либо каталитическим гидрированием, либо с помощью цианборгидрида натрия NaBH3CN. Механизм этой реакции включает две важные стадии: образование имина и восстановление имина в амин:
R-COH + NH3 « RH-C=NH + H2O ® RH2-C-NH2
CH3(CH2)5CHO + NH3 ® CH3(CH2)6-NH2
Если вместо аммиака использовать первичный амин, то продуктом реакции будет вторичный амин.
5. Восстановление нитроалканов, оксимов, нитрилов, амидов
Азотсодержащие соединения (нитроалканы, оксимы, амиды, нитрилы и изонитрилы) под действием водорода или других восстановителей дают либо первичные амины, либо вторичные, либо их смесь:
R-NO2 + 3 H2 ® R-NH2 + 2 H2O
R-CN + 2 H2 ® R-NH2 + 2 H2O
R-NC + 2 H2 ® R-NH-CH3
Катализаторы – Pt, Pd, Ni.
3. Расщепление амидов кислот (перегруппировка Гофмана).
Амиды алифатических и ароматических карбоновых кислот реагируют со щелочными растворами иода, брома или хлора с образованием первичных аминов. Это так называемая гипогалогенитная реакция Гофмана позволяет не только синтезировать первичные амины, но и укорачивать углеродную цепь на один атом.
Br2 + H2O + RC(O)NH2 + 2 OH - ® R-NH2 + CO2 + 2 H2O + 2 Br-
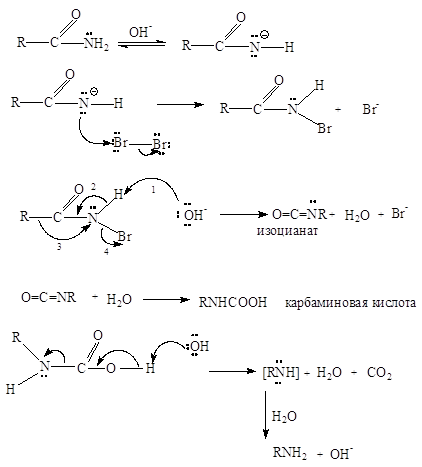
Сначала из стабилизированного резонансом амид-иона образуется N-галогензамещенный амид (здесь N-бромамид), который в щелочном растворе неустойчив и превращается в изоцианат.
Изоцианаты, так же как их углеродные аналоги (кетены), быстро реагируют с водой. Продукт гидратации, карбаминовая кислота, легко декарбоксилируется с образованием амина.
7. Перегруппировка Курциуса.
Хлорангидриды кислот, взаимодействуя с азидом натрия NaN3, дают ацилазиды (азиды кислот), которые при нагревании превращаются в изоцианаты:
R-CO-Cl + NaN3 ® R-CO-N-NºN
Превращение ацилазидов в изоцианаты, как показано ниже, представляет собой согласованный процесс. Эта реакция носит название перегруппировки Курциуса:
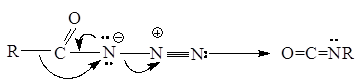
Затем изоцианаты реагируют с водой и образуются амины:
O=C=N-R + H2O ® CO2 + R-NH2
Первичные и вторичные амины способны образовывать межмолекулярные водородные связи. Поэтому амины имеют более высокие температуры кипения, чем неполярные соединения с той же молекулярной массой. Спирты и карбоновые кислоты образуют более прочные водородные связи, чем амины. Поскольку третичные амины не содержат водородных атомов при атоме азота, они не образуют водородных связей.
Низкомолекулярные амины смешиваются с водой в любых соотношениях.
Алифатические амины. Ароматические амины
Химические свойства аминов
1. Реакции аминов с кислотами
R-NH2 + HCl ® R-NH3+Cl -
Эти соли при взаимодействии с водными растворами оснований выделяют амины.
Основность аминов определяется легкостью, с которой амин отщепляет протон от воды.
2. Алкилирование аминов галогеналканами - см. Лекцию №31. На последней стадии образуются четвертичные соли аммония - четыре органических группы ковалентно связаны с азотом, положительный заряд уравновешен наличием отрицательного иона:
2 RN+X- + Ag2O + HOH ® 2 AgX¯ + OH- + 2 RNOH « R4N+
Четвертичные аммониевые основания (белые кристаллические вещества) по основности сопоставимы с NaOH, KOH.
4. Ацилирование аминов (получение амидов).
Первичные и вторичные амины реагируют с ангидридами и галогенангидридами кислот с образованием амидов:
CH3CH2NH2 + CH3COCl ® CH3CO-NH-CH2CH3 + HCl
(CH3)2NH + (CH3CO)2O ®(CH3)2N-COCH3 + CH3COOH
Замещенные амиды называют как производные незамещенных амидов карбоновых кислот.
Образующаяся в ходе реакции кислота связывает эквивалентное количество непрореагировавшего амина. Такой метод становится неэкономичным, если амин трудно синтезировать или он представляет собой дорогостоящий реактив. Поэтому амины часто ацилируют по реакции Шоттен-Баумана, которая заключается во взаимодействии амина и ацилирующего агента в присутствии водного раствора едкого натра:
(CH3)2C-CH2-COCl + R2-NH + OH- ® (CH3)2C-CH2-CO-N-R2 + HCl
Ароматические амины
Ароматические амины могут быть первичными ArNH2 (анилин, толуидины), вторичными Ar2NH (дифениламин), и третичными Ar3N (трифениламин).
Способы получения ароматических аминов
1. Восстановление нитросоединений (реакция Зинина).
В качестве восстановителей используются железо и соляная или серная кислота, олово и соляная кислота, сероводород и сернистые щелочи, гидросульфиты, водород в присутствии катализаторов. Восстановление также можно осуществить электролитически.
Ar-NO2 + 2H2 ® Ar-NH2 + 2H2O
В зависимости от характера среды восстановление идет разными путями. В кислой среде в качестве промежуточных продуктов образуются нитрозосоединения и производные гидроксиламина. Последние могут быть получены как конечные продукты при восстановлении в нейтральной среде. В щелочной среде процесс идет более сложно. Вслед за нитрозосоединениями получаются азоксисоединения, затем азосоединения, гидразосоединения и, наконец, амины.
2. Аммонолиз арилгалогенидов (алкилирование аммиака арилгалогенидами).
Ароматические амины получают из арилгалогенидов и аммиака:
ArCl + 2 NH3 ® Ar-NH2 + NH4Cl
Вследствие малой подвижности галогена реакцию приходится вести при высоких давлениях и температурах в присутствии катализаторов - меди и ее солей. Только в тех случаях, когда в о- или п-положении к галогену находится сильно электроотрицательные группы, например, нитрогруппа, галоген легко замещается на аминогруппу.
3. Реакция Гофмана.
Ароматические амины могут также быть получены из кислот через амиды по реакции Гофмана (см. Лекцию№31).
4. Получение вторичных ароматических аминов.
Ароматические вторичные амины получают нагреванием ароматических аминов с их солями:
Ar-NH2 + Ar-NH2×HCl ® Ar2NH + NH4Cl
Вторичные жирноароматические амины получают алкилированием первичных ароматических аминов галогенпроизводными или спиртами.
5. Третичные амины.
Третичные ароматические амины получают алкилированием или арилированием первичных или вторичных аминов:
C6H5-NH2 + 2 CH3OH ® C6H5-N(CH3)2 + 2 H2O
Менее доступные третичные ароматические амины получают нагреванием вторичных аминов с арилиодидами в присутствии медного порошка:
(C6H5)2-NH + C6H5J ® (C6H5)3N + HJ
Химические свойства ароматических аминов
Ароматические амины имеют менее выраженный основный характер, чем алифатические. Так, Кb метиламина составляет 4,4×10-5, тогда как для анилина Кb=3,8×10-10. Уменьшение основности анилина по сравнению с алифатическими аминами объясняется взаимодействием неподеленной пары электронов азота с электронами ароматического ядра - их сопряжением. Сопряжение уменьшает способность неподеленной электронной пары присоединять протон.
Присутствие электроноакцепторных групп в ядре уменьшает основность. Например, константа основности для о-, м- и п-нитроанилинов составляет соответственно 1×10-14, 4×10-12 и 1×10-12.. Ведение второго ароматического ядра также заметно уменьшает основность (для дифениламина Kb=7,6×10-14). Дифениламин образует сильно гидролизующиеся в растворах соли только с сильными кислотами. Трифениламин основными свойствами практически не обладает.
С другой стороны, введение алкильных групп (электронодонорные группы) увеличивает основность (Kb N-метиланилина и N,N-диметиланилина равны соответственно 7,1×10-10 и 1,1×10-9
1. Алкилирование ароматических аминов.
Ароматические амины способны замещать водород аминогруппы на алкилы. Эта реакция приводит ко вторичным и третичным аминам:
C6H5NH2 + CH3J ® C6H5NH-CH3 + CH3J ® C6H5N-(CH3)2
Алкилирование ведут спиртами или хлоралканами, в качестве катализаторов используют соли одновалентной меди в виде аммиачных комплексов. Важно, что процесс N-алкилирования является последовательно-параллельным, обусловленный тем, что образовавшийся амин, в свою очередь, способен реагировать с алкилирующим агентом. Состав продуктов зависит от соотношения реагентов.
2. Ацилирование ароматических аминов.
При действии ацилирующих агентов (кислоты, ангидриды, хлорангидриды) водородные атомы аминогруппы замещаются на ацильные остатки.
C6H5NH2 + (CH3CO)2O ® C6H5NHCO-CH3 + CH3COOH
C6H5NH2 + CH3COOH ® C6H5NH2×HOCOCH3®C6H5NHCO-CH3 + H2O
Ацильные производные не обладают основными свойствами. Они обладают устойчивостью к окислителям и потому используются в качестве промежуточных веществ в реакциях аминов в присутствии окислителей (например, нитрование).
3. Синтез азометинов (оснований Шиффа).
При слабом нагревании ароматических первичных аминов с ароматическими альдегидами легко образуются так называемые основания Шиффа или азометины:
C6H5NH2 + C6H5COH ® C6H5N=CH-C6H5 + H2O
Под действием разбавленных кислот основания Шиффа гидролизуются до альдегида и амина.
4. Реакции аминов с азотистой кислотой.
Азотистая кислота HONO неустойчива, но ее водный раствор можно получить, растворив нитрит натрия, при охлаждении в разбавленной кислоте, например, соляной.
Первичные алифатические амины реагируют с холодным водным раствором азотистой кислоты с образованием алкилдиазониевых солей, при разложении которых образуется смесь разнообразных продуктов:
CH3CH2CH2-NH2 + HONO ® [CH3CH2CH2N2+] ® [CH3CH2CH2+] + H2O ® CH3CH2CH2-OH + CH3CH(OH)CH3 + CH3CH=CH2 + (CH2)3
Вторичные алифатические амины реагируют с азотистой кислотой с образованием N-нитрозоаминов желтого цвета. Эти соединения, амиды азотистой кислоты, являются очень слабыми основаниями.
(CH3)2NH + [HONO] ® (CH3)2N-N=O
N-нитрозодиметиламин (канцероген!)
При взаимодействии третичных алкиламинов с азотистой кислотой образуются сложные смеси.
Важнейшие представители ароматических аминов
Анилин впервые был получен в результате перегонки индиго с известью (1826г.). В 1842 г. его получил Зинин восстановлением нитробензола. В незначительных количествах содержится в каменноугольной смоле. В промышленности получают из нитробензола каталитическим гидрированием с медным катализатором в газовой фазе. Анилин в больших количествах идет на получение красителей, циклогексиламина, капролактама, пестицидов и др.
п-Толуидин широко применяется в производстве красителей, особенно фуксина.
N,N-диметиланилин применяется в производстве красителей и взрывчатых веществ.
| Изучение вопросов биотехнологии в курсе химии средней школы | |
|
Изучение вопросов биотехнологии в курсе химии средней школы Введение Актуальность исследования: в настоящее время российское химическое образование ... Алифатические кислоты Ацил-КоА Ацетил-КоА HOOC-CH2-CH(NH2) - COOH = CH3-CH(NH2) - COOH+CO2 |
Раздел: Рефераты по педагогике Тип: курсовая работа |
| Переработка жидкого топлива | |
|
ПЕРЕРАБОТКА ЖИДКОГО ТОПЛИВА К жидким химическим топливам относятся нефть и продукты ее переработки (нефтепродукты), а также продукты гидрирования ... изомеризации R-CH=CH-CH3 = R-C=CH2, При карбамидной депарафинизации карбамид образует с алканами нормального строения с числом углеродных атомов более шести и циклическими углеводородами с длинными алифатическими ... |
Раздел: Рефераты по химии Тип: курсовая работа |
| Дибензальацетон | |
|
СОДЕРЖАНИЕ 1. Введение.. 2 1.1. Свойства дибензальацетона. 2 1.2. Применение дибензальацетона. 2 1.3. Методика синтеза. 2 2. Литературный обзор. 4 2.1 ... Альдегиды, не содержащие в ѭ-положении к карбонильной группе атома водорода, т.е. преимущественно ароматические альдегиды, в присутствии гидроксидов щелочных или щелочноземельных ... Перкина реакция, метод синтеза b-арилакриловых кислот (коричной кислоты, её производных и аналогов) взаимодействием ароматических альдегидов с ангидридами карбоновых кислот в ... |
Раздел: Рефераты по химии Тип: курсовая работа |
| Развитие, становление и основные аспекты фармации | |
|
РАЗВИТИЕ, СТАНОВЛЕНИЕ И ОСНОВНЫЕ АСПЕКТЫ ФАРМАЦИИ Для ветеринарного провизора необходимы знания, с помощью которых можно контролировать качество ... ртуть (цветные реакции с аминоспиртами, арилалкилами-нами, оксифенилалкиламинами, гидразидами изоникотиновой кислоты, первичными ароматическими аминами, причем последние ... Первичные алифатические и ароматические аминокислоты и их соли (кислота амино-капроновая, калия и магния аспарагинаты, кислота глутаминовая, ПАСК-натрий), взаимодействуя с ... |
Раздел: Рефераты по медицине Тип: книга |
| Общая и неорганическая химия | |
|
Квантово-механическая модель атома. Квантовые числа. Атомные орбитали. Порядок заполнения орбиталей электронами Теория строения атома основана на ... ... в некоторых других (хлор, сера).Наиболее прочные водородные связи имеются в воде, фтороводороде, кислородсодержащих неорганических кислотах, карбоновых кислотах, фенолах, спиртах, ... Гидропероксидный радикал, образовавшийся на стадии инициирования, в результате реакции HO2- + RH ° H2O2 + R- превращается в радикал R- с неспаренным электроном на атоме углерода. |
Раздел: Рефераты по химии Тип: учебное пособие |