Контрольная работа: Взаимодействия в коллоидных системах
Раздел: Рефераты по химии
Тип: контрольная работа
Контрольная работа
по химии
вариант № 11
2009
Содержание
Взаимодействия в коллоидных системах
Взаимодействие двойных электрических слоев и устойчивость коллоидных систем
Уравнение Пуассона-Болъцмана
Контактная теорема и осмотическое давление
Добавление соли и "приближение слабого перекрывания"
Ван дер Ваальсовы взаимодействия и константа Гамакера
Структурные взаимодействия
Гидратные силы отталкивания
Силы, действующие между поверхностями слюды в среде линейного и разветвленного алканов
Гидрофобное притяжение
Силы деплеции
Непосредственное измерение взаимодействий в коллоидных системах
Взаимодействия в коллоидных системах
Потенциал взаимодействия между большими агрегатами или частицами в жидкой дисперсионной среде является эффективным потенциалом. Однако взаимодействие между коллоидными частицами настолько важно, что заслуживает отдельного обсуждения.
Взаимодействие двойных электрических слоев и устойчивость коллоидных систем
Стабилизация или дестабилизация коллоидной системы - это центральная проблема для многих промышленных процессов. Разработаны различные способы ее решения, но наиболее общий подход связан с регулированием электростатических взаимодействий. Если коллоидные частицы заряжены, основное внимание нужно уделять электростатическим взаимодействиям. Заряженные коллоидные частицы присутствуют почти везде - в глине и в почве, в мембранах, в бумаге и в бумажной пульпе, в торфе, красках и т.д. Белки также представляют собой заряженные коллоидные частицы. Заряд коллоидных частиц может возникнуть при диссоциации функциональных групп или в результате специфической адсорбции ионов на частицах. Геометрическая форма частиц может широко варьироваться: в золях присутствуют сферические частицы, глины состоят из плоских частичек, молекула ДНК имеет цилиндрическую форму. Несмотря на это такие системы имеют много общих свойств, которые рассматриваются ниже.
Уравнение Пуассона-Болъцмана
Для простоты ограничим математическое описание двумя плоскими заряженными поверхностями, находящимися друг от друга на расстоянии 2а. Примем, что заряд равномерно распределен по поверхностям, т.е. плотность заряда у одинакова. Согласно результатам моделирования, такую систему можно считать достаточно хорошим приближением. Кроме того, для упрощения примем, что в системе присутствуют только противоионы, способные нейтрализовать заряд поверхностей. Случай с присутствием других солей обсудим позже.

Две заряженные стенки, разделенные раствором, который содержит противоионы. Заряды на стенках равномерно распределены по поверхности и плотность заряда одинакова в любой ее точке. Рассмотрим потенциал ф и объемную плотность заряда р вдали от поверхности. Комбинируя уравнения Пуассона и Больцмана, получают так называемое уравнение Пуассона-Больцмана, описывающее термодинамику заряженной поверхности, которая находится в контакте с водным раствором:
![]()
где Z - зарядовое число противоиона и ро-нормировочная константа с размерностью плотности заряда. Уравнение является приближением среднего поля. Уравнение Пуассона-Больцмана для большинства случаев не имеет аналитического решения, поэтому необходимо прибегать к численным решениям. Для рассматриваемого здесь частного случая имеется аналитическое решение:
![]()
где величина s задается выражением
![]()
Решение этого уравнения можно получить простой итерацией, начиная с предположения, что s = р/4 и решая уравнение относительно tg S9 что дает более точное значение для S9 и т.д. На рис. показан типичный концентрационный профиль противоионов со значительным накоплением ионов вблизи заряженных стенок. Особенно простое решение получается в том случае, когда правая часть уравнения становится очень большой. При этом условии s стремится к р/2. Это решение имеет ряд интересных свойств. Рассмотрим, что будет происходить при разбавлении системы. Тогда пристеночная концентрация будет стремиться к предельному значению, которое определяется следующим выражением:
![]()

Концентрационный профиль однозарядных противоионов между двумя заряженными поверхностями, находящимися в воде на расстоянии 21 А. Поверхностная плотность заряда равна 0.224 Кл/м2. Кривая соответствует уравнению Пуассона-Больцмана, точки - моделированию методом Монте-Карло.
Это означает, что противоионы нельзя полностью удалить. Иногда это явление называют ионной конденсацией. Однако конденсированный слой не связан непосредственно с поверхностью, речь идет о концентрации противоионов вблизи поверхности.
Плотность заряда посредине между стенками описывается следующим уравнением:
![]()
Таким образом, при увеличении расстояния между пластинами плотность заряда в центре уменьшается с расстоянием как Ma, независимо от поверхностной плотности заряда. Другими словами, вдали от поверхности ион обнаруживает знак плотности поверхностного заряда, но не ее величину!
Контактная теорема и осмотическое давление
Для стабильности коллоидных систем важна сила, действующая между двумя заряженными стенками. Выражение для силы легко выводится из основных положений, а получающиеся уравнения иногда называют контактными теоремами. Выражение для осмотического давления можно получить из двух независимых контактных соотношений в рамках приближения Пуассона-Больцмана:
![]() ,
, ![]()
Первое соотношение не содержит корреляционного члена и не является точным. Второе соотношение представляет собой точное выражение. Из данных, приведенных на рис., видно, насколько результаты приближения Пуассона-Больцмана согласуются с результатами моделирования методом Монте-Карло.

Зависимость осмотического давления от поверхностной плотности заряда в отсутствие электролита. Сплошные линии - результаты оценок на основании уравнения Пуассона-Больцмана. Точные зависимости, полученные методом Монте-Карло показаны штриховыми линиями. Расстояние между стенками 21 А: а - однозарядные противоионы; б - двухзарядные противоионы.
Осмотическое давление пропорционально концентрации ионов посередине между заряженными стенками, из чего следует, что отталкивание двойных слоев имеет главным образом энтропийную природу. При сближении заряженных поверхностей вторая поверхность ограничивает объем, в котором находятся противоионы, относящиеся к первой поверхности, и наоборот. Вследствие этих пространственных ограничений для противоионов и возникает отталкивание. В трактовке этого вопроса иногда можно встретиться с недопониманием сути, когда физической природой отталкивания между двумя заряженными коллоидными частицами считают их прямое электростатическое взаимодействие. Эта сила, конечно, имеет электростатическую природу, поскольку у незаряженных коллоидных частиц не существует противоионов, но она проявляется в виде энтропийного вклада. Корреляционный член, показанный на рис., всегда отражает притяжение и имеет ту же природу, что и квантово-механические дисперсионные силы. Он также действует между сферическими макроионами, окруженными противоинами. В этом случае корреляционная свободная энергия уменьшается с расстоянием г между макроионами как г*. Заметим, что величина корреляционного вклада практически одинакова для одно - и двухзарядных ионов. Однако он становится значительным в последнем случае из-за относительно небольшого вклада энтропии. Необходимо твердо помнить о том, что применять уравнение Пуассона-Больцмана для систем с двух - или многозарядными противоионами, а также при очень высоких концентрациях солей следует с очень большой осторожностью.
До сих пор мы анализировали системы в отсутствие солей, что, как правило, далеко от реальных систем. В то же время нужно представлять, что концентрация электролита во многих системах часто гораздо ниже, чем концентрация противоионов, необходимая для нейтрализации поверхности. В таких условиях полученные выше уравнения очень полезны, поскольку имеют аналитические решения.
Добавление соли и "приближение слабого перекрывания"
В наиболее общих и сложных ситуациях, когда в систему добавлены соли, уравнение Пуассона-Больцмана необходимо решать численно. При равновесии двойного электрического слоя с раствором соли обычно интерес представляет только величина осмотического давления, т.е. разница осмотического давления в растворе между двумя поверхностями и осмотического давления в объеме раствора. Другими словами:
Однако существует особенно простое асимптотическое выражение для свободной энергии и силы. Оно основано на решении Гуи-Чепмена и применимо для двух слабо перекрывающихся двойных электрических слоев. При этом условии уравнение Пуассона-Больцмана может быть линеаризовано, что позволяет избежать решения полного нелинейного уравнения. Свободная энергия G, нормированная на единицу площади, выражается уравнением
![]()
![]()
а величина осмотического давления Pocm:
![]()
где со - концентрация электролита в растворе, к - величина, обратная дебаев-скому радиусу экранирования, который был определен ранее), D = - расстояние между поверхностями, г - величина, связанная с потенциалом поверхности через выражение
![]() .
.
Таким образом, сила, действующая между двумя полярными поверхностями, экспоненциально уменьшается с расстоянием между ними. Это полезное приближение, которое в большинстве случаев пригодно для расчета силы, действующей между плоскими заряженными стенками, погруженными в раствор электролита. Асимптотическое поведение осмотического давления согласно уравнению было подтверждено многочисленными экспериментами. Было доказано не только экспоненциальное уменьшение давления с расстоянием, но и установлено, что наклон зависимостей в пределах экспериментальной ошибки равен толщине ДЭС к-1. Это можно рассматривать как проверку справедливости теории Дебая-Хюккеля и лежащего в ее основе приближения непрерывной диэлектрической среды. Изменение силы на коротких расстояниях при D < к-1 не очень точно описывается теорией, но несмотря на это можно "подогнать" решение полного нелинейного уравнения Пуассона-Больцмана под экспериментальные кривые, используя наряду с другими параметрами плотность поверхностного заряда как свободный параметр.
Для двух заряженных сферических коллоидных частиц свободная энергия взаимодействия имеет аналогичный вид:
![]()
где r - расстояние между сферами. Уравнение представляет собой соотношение Дебая-Хюккеля, уже встречавшееся нам ранее:

Силы взаимодействия между отрицательно заряженными поверхностями слюды в растворах L1NO3 различной концентрации. Эксперимент проведен с использованием прибора для измерения поверхностных сил
Ван дер Ваальсовы взаимодействия и константа Гамакера
Известная теория устойчивости дисперсных систем Дерягина, Ландау, Фервея и Овербека включает две составляющие: силу отталкивания двойных электрических слоев, которая рассчитывается по уравнению Пуассона-Больцмана, и силу притяжения Ван дер Ваальса.
Сила Ван дер Ваальса включает несколько вкладов. Во-первых, квантово-механические дисперсионные взаимодействия. Второе слагаемое появляется как результат термически усредненного диполь-дипольного взаимодействия. Третий вклад обусловлен взаимодействиями индуцированных диполей. Ван-дер-ваальсовы силы действуют как между полярными, так и неполярными молекулами и мало зависят от природы вещества. Это отличает их от электростатических сил, величина которых может меняться на порядки при добавлении небольших количеств электролита. Наиболее прямой путь расчета силы Ван дер Ваальса заключается в предположении, что взаимодействие попарно аддитивно, - этот способ расчета известен как подход Гамакера. Взаимодействие двух бесконечных плоских стенок описывается как:
![]()
где А - константа Гамакера, D - расстояние между стенками. Для большинства конденсированных фаз значение константы Гамакера лежит в интервале 10-19 Дж.
Предположение попарной аддитивности не совсем корректно; более строгая теория была создана Е.М. Лифшицем с коллегами. Для надежного использования подхода Лифшица необходимо знать частотную зависимость диэлектрической проницаемости во всей области спектра. К счастью, простого приближения Гамакера, как оказалось, вполне достаточно для описания большинства экспериментальных результатов.
Уравнение справедливо и для взаимодействия двух частиц в среде. Единственное изменение при этом состоит в том, что константа Гамакера уменьшается. Следует помнить правило, что при взаимодействии углеводородов в воде взаимодействие уменьшается на - 90% по сравнению с их взаимодействием в воздухе.
Недостаток теорий Гамакера и Лифшица заключается в постулировании постоянства плотности жидкости в зазоре между частицами, которая принимается равной плотности объемной жидкости. Правильнее исходить из постоянства химического потенциала. Для асимптотик выбор не имеет значения, но при промежуточных расстояниях плотность жидкости в зазоре будет отличаться от плотности жидкости в объеме. Эти вариации плотности будут приводить к отклонению от простого уравнения. На рис. показано, как простая жидкость стремится избежать пространства между инертными поверхностями, что приводит к понижению плотности жидкости по сравнению с объемом. Это понижение, не учтенное ни в теории Гамакера, ни в теории Лифшица, приводит к усилению притяжения. Аналогичное притяжения будет наблюдаться для воды в зазоре между гидрофобными поверхностями.
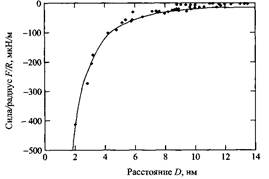
Зависимость силы притяжения Ван дер Ваальса между двумя поверхностями слюды в воздухе от расстояния между пластинами.
Структурные взаимодействия
На расстояниях между двумя поверхностями, сравнимых с размерами молекул, на взаимодействие частиц начинают влиять эффекты упаковки. При определенных условиях это приводит к осцилляции профиля плотности и к появлению осциллирующей силы, зависящей от расстояния между поверхностями. Осцилляции могут накладываться на зависимости, отражающие как притяжение, так и отталкивание. Профили плотности для таких модельных систем детально исследованы с помощью компьютерного моделирования. В то же время рассчитать суммарное взаимодействие оказалось намного труднее. Иногда высказывается мнение, что осциллирующий профиль плотности автоматически приводит к осциллирующему профилю силы. Возможно, что это положение справедливо, однако до сих пор оно не доказано. Была осуществлена попытка измерить осцилляторные силы между скрещенными цилиндрами слюды в среде октаметилциклотетрасилана. Оказалось, что период осцилляции вполне соответствует молекулярным размерам. Эти силы слабо зависят от температуры, но небольшие добавки других растворителей или примесей полностью изменяют поведение системы и разрушает картину осцилляции.

Жидкость Леннард-Джонса между двумя инертными стенками, а - Зависимость приведенной плотности от расстояния между стенками для трех значений приведенной температуры. б - Усиление притяжения вследствие понижения плотности. В подходе Гамакера при расчете притяжения ^ham плотность в зазоре принимается постоянной и равной объемной плотности
Осцилляторные силы обнаруживаются также в среде линейных алканов, но они не проявляются в среде разветвленных алканов. Подобные силы зарегистрированы между поверхностями слюды в водных растворах, но в этом случае обнаружен более короткий период осцилляции по сравнению с ОМЦТС, что объясняется разницей молекулярных размеров воды и ОМЦТС.
Гидратные силы отталкивания
Легко представить, что заряженная поверхность или поверхность, несущая противоположные заряды, при погружении в водный раствор будет связывать один или несколько слоев молекул воды, гидратирующих поверхность таким же образом, как растворенный ион формирует гидратную оболочку. Приведение таких поверхностей в контакт вызывает их дегидратацию. Можно предположить, что в результате возникают гидратные силы отталкивания.

Осцилляторные силы между поверхностями слюды в инертной силиконовой жидкости, диаметр молекул ОМЦТС составляет ~9 A

Силы, действующие между поверхностями слюды в среде линейного и разветвленного алканов
Было обнаружено очень сильное, короткодействующее взаимодействие между липидными бислоями. Расстояния, на которых проявляется это взаимодействие, лежат в диапазоне 10-30 А. Отталкивание экспоненциально уменьшается с увеличением расстояния между липидным монослоями. Для измерения соответствующей силы была использована методика, основанная на измерении осмотического давления. Аналогичным образом методом измерения поверхностных сил с помощью специального прибора были измерены силы отталкивания между поверхностями слюды. Гидратные силы отталкивания, по-видимому, действуют как между нейтральными, так и между заряженными поверхностями. Несмотря на то что поверхности слюды жесткие, а би-слойные структуры - гибкие, оба исследования дали удивительно хорошо согласующиеся результаты. Отталкивание между поверхностями слюды наблюдалось и в других жидких средах.
Проведенные эксперименты привели к интенсивным поискам теоретической интерпретации результатов. Одной из причин отталкивания предложено считать структурную поляризацию или поляризацию водородных связей на поверхности. В случае липидных бислоев механизм отталкивания может быть обусловлен возможностью волнообразных деформаций и взаимодействием отображения заряда. Недавно было высказано предположение, что липиды "выдавливаются" в растворитель; при сближении поверхностей возможность образования выступов уменьшается, что приводит к появлению отталкивания. Этот механизм близок к идее отталкивания из-за волнистости. Разница заключается главным образом в масштабе флуктуации. Исходная модель основана на "волнистости" с большой длиной волны, тогда как модель "выступов" справедлива на расстояниях, сопоставимых с молекулярными размерами.

Гидратные силы отталкивания между поверхностями слюды в растворе электролита. Следует отметить, что отталкивание возникает только при концентрации соли > 1мМ.
Моделирование методом Монте-Карло обнаружило короткодействующие силы отталкивания даже для идеально гладких поверхностей. Необходимо сказать, что как гидратные силы отталкивания, так и гидрофобное притяжение, которое описано ниже, можно достаточно просто моделировать, варьируя силу взаимодействия между растворителем и поверхностью. Сильное притяжение растворитель-поверхность автоматически приводит к появлению силы отталкивания поверхность-поверхность. Если поверхности инертны, т.е. нет сил притяжения между поверхностью и растворителем, то между поверхностями действует сольватационное притяжение. В обоих случаях взаимодействие ограничено расстояниями менее 100 А.

Гидратные силы отталкивания и гидрофобное притяжение для смачиваемой и несмачиваемой стенок соответственно. Теоретические данные получены из обобщенной теории Ван дер Ваальса
Гидрофобное притяжение
Накоплено множество результатов измерений силы, действующей между гидрофобными поверхностями. Обычно для исследований используют поверхности слюды, модифицированные монослоями углеводородных или фторированных групп, обращенных к воде. Эти исследования привели к неожиданному результату: было обнаружено, что между такими поверхностями сила притяжения действует на больших расстояниях. Притяжение распространяется на сотни ангстрем. При этом притяжение нельзя объяснить силами Ван дер Ваальса в рамках подхода Гамакера. Кроме того, на него практически не влияют добавки солей. Экспериментально наблюдаемое дальнодействие невозможно объяснить аналогично тому же типу гидрофобного взаимодействия, с которым мы встречались, например, при взаимодействии двух атомов неона в воде. Хотя принято считать, что "обычное" гидрофобное взаимодействие проявляется только на близких расстояниях, реально его величина может увеличиваться по механизму уменьшения плотности.
Считается, что гидрофобное притяжение ответственно за быструю коагуляцию гидрофобных частиц в воде и играет важную роль в фолдинге белков. Однако, как и в случае гидратных сил отталкивания, теоретические разработки гидрофобных взаимодействий практически отсутствуют. Одним из возможных механизмов, способных обеспечить притяжение, может быть образование полостей, т.е. маленьких пузырьков газа, на гидрофобизованной поверхности слюды. В зависимости от условий такая кавитация вызывает увеличение силы отталкивания или притяжения. Другая возможная причина притяжения между гидрофобизованными поверхностями заключается в том, что поверхности локально не нейтральны и корреляция между положительно и отрицательно заряженными участками вызывает притяжение.
Силы деплеции
Для кристаллизации белков обычно используют полиэтиленоксид. Считается, что ПЭО вызывает силу деплеции между макромолекулами белка. Другими словами, ПЭО не может проникать в пространство между молекулами белка из-за очень сильного ограничения конформационной свободы полимерных цепей ПЭО. Накапливаясь в растворе, ПЭО создает осмотическое давление, действующее на молекулы белка. Это очень интересный механизм, в том смысле, что вводимый полимер влияет на взаимодействие между коллоидными частицами, не находясь между ними! Диапазон сил притяжения деплеции по порядку величины совпадает с радиусом инерции полимерной молекулы. Для идеального полимера радиус инерции равен г1/2, где r - степень полимеризации.
Иногда на больших расстояниях до проявления сил притяжения деплеции появляются силы отталкивания. Это явление часто называют деплеционным отталкиванием. И притяжение, и отталкивание этой природы наблюдались экспериментально и описаны теоретически.

Притяжения между двумя поверхностями слюды, покрытыми монослоями фторированных ПАВ, измеренные в этиленгликоле и при различных концентрациях воды. Пунктирные линии представляют ван-дер-ваальсово взаимодействие. Усиление притяжения между поверхностями, покрытыми неионным ПАВ, с ростом температуры. Предполагается, что гидрофобность монослоя НПАВ увеличивается с температурой. С разрешения

Взаимодействие двух нейтральных поверхностей в растворе полимера как функция расстояния. Раствор в зазоре находится в равновесии с раствором в объеме при определенной концентрации
Непосредственное измерение взаимодействий в коллоидных системах
Исследования фазовых диаграмм, кинетики коагуляции, электрофореза и других явлений дают косвенную информацию о силах, действующих между агрегатами. Непосредственно измерить взаимодействие между заряженными коллоидными частицами значительно сложнее. Методика, основанная на измерении осмотического давления, является прекрасным методом, пригодным для изучения систем, которые самопроизвольно образуют, например, ламелярные структуры. Система находится в равновесии с объемом водного раствора, чьи химический потенциал и осмотическое давление можно контролировать. Расстояние между агрегатами измеряется с помощью дифракции рентгеновских лучей. В равновесии осмотическое давление раствора равно давлению, действующему между частицами.
Прибор для измерения поверхностных сил технически сложнее, но и более универсален. Он состоит из двух скрещенных цилиндров, покрытых пластинками гладкой отрицательно заряженной слюды. Расстояние между цилиндрами измеряется интерферометрически с разрешением в несколько ангстрем. Сила измеряется с помощью набора пружин и пьезоэлектрического кристалла, присоединенного к одному из цилиндров. Сила FcyI, действующая между искривленными поверхностями, может быть преобразована в свободную энергию для плоской поверхности Gpian с помощью приближения Дерягина:
![]()
где R - радиус цилиндра. Метод измерения поверхностных сил имеет то преимущество, что поверхность слюды может быть модифицирована адсорбцией:

Прибор для измерения поверхностных сил различных веществ из раствора
Например, можно измерить взаимодействие между поверхностями, покрытыми полимером. Поверхность можно гидрофобизировать посредством адсорбции монослоя катионных ПАВ. Можно нанести на поверхность слюды бислои. Таким образом? можно изучать огромный спектр систем.
Атомно-силовая микроскопия и сканирующая туннельная микроскопия существенно расширили возможности прямого измерения взаимодействий в коллоидных системах.