Курсовая работа: Лекарственное растительное сырье, содержащее фенолгликозиды
КУРСОВАЯ РАБОТА
по фармакогнозии:
Тема: “ Лекарственное растительное сырье, содержащее фенолгликозиды ”
Содержание
Введение
1. Фенольные гликозиды
2. Физико- химические свойства. Химическое строение фенолгликозидов
3. Фармакологические свойства фенолгликозидов
4. Методы выделения и идентификации
5. Качественное определение
6. Методики обнаружения фенолгликозидов
7. Количественное определение
7.1 Титриметрический метод количественного определения
7.2 Инструментальные методы количественного определения
8. ЛР и ЛРС, содержащие феногликозиды
8.1 Брусника обыкновенная
8.2 Толокнянка обыкновенная
8.3 Ива
8.4 Красная щётка
8.5 Родиола розовая
8.6 Бадан толстолистный
Заключение
Используемая литература
Введение
Биохимические и биологические научные исследования состава лекарственных растений и его влияния на обмен веществ человеческого организма позволяют выявить то действующее начало, которое и обеспечивает целебное воздействие в случае заболевания человека, затем разработать метод извлечения из фитосырья этого конкретного химического соединения или их группы. При определенных технологических возможностях возможно и синтезировать это биологически активное соединение (далее - БАВ). Так появляются новые фармацевтические препараты с научно выверенной концентрацией БАВ, удобные в применении и весьма эффективные в лечении. Проходят годы и при анализе материалов клинического применении нового «чуда-лекарства» выявляются неучтенные побочные действия препарата и часто оказывается, что удаленные «балластные» соединения обладали способностью предотвратить их. Ведь человеческий разум не всегда в состоянии постичь мудрость матушки- Природы. Проводятся дополнительные научные изыскания, выявляется новая формула, на основе которой готовится лекарственный препарат нового поколения, обладающий фантастической эффективностью. Пройдут десятилетия прежде, чем более совершенный клинический анализ покажет явно, что формула была не совершенна и в ней «необходимо что-то подправить». Благодаря новым достижениям наука благополучно завершит еще один виток, а совершенствованию нет границ и предела… А народная медицина существовала до появления научных методов ее исследования, существует сейчас и, не исключено, что скоро выяснится, что ее методики окажутся наиболее оптимальными, конечно, если учесть отдаленные и пока неочевидные последствия и побочные действия фармакологических препаратов. Очевидно, что в связке народная медицина (многовековой опыт фитотерапии) и наука имеется и обратная связь. Благодаря научным исследованиям и успешным попыткам создания лекарственных препаратов нового поколения, фитотерапия также развивалась и в своем развитии достигла (или скоро достигнет) состояния научной дисциплины [1, 2].
Фитотерапевтический эффект при лечении различных заболеваний определяется прежде всего составом и количественным содержанием БАВ в используемых лекарственных растениях, а затем правильностью подбора дозировки и состава фитосбора. Оказывающее лечебное воздействие вещества имеют самый разнообразный состав и относятся к различным классам химических соединений. Огромным терапевтическим действием обладают БАВ, относящиеся к следующим классам органических соединений: алкалоиды, гликозиды, фенольные соединения, терпеноиды, полисахариды и др. Среди неорганических соединений большое значение для жизнедеятельности и здорового обмена веществ имеют минеральные соли неорганических кислот, в состав которых входят микроэлементы. Результаты научных исследований показали физиологическое влияние БАВ на метаболизм человеческого организма и позволили разработать новые эффективные лекарственные препараты, которые успешно используются в терапии многих заболеваний [3, 4, 5, 6].
В растениях наряду с белками, нуклеиновыми кислотами, углеводами, липидами и витаминами содержатся различные вещества, называемые обычно веществами вторичного происхождения. Часто они играют весьма важную роль в обмене веществ у растений [7, 8].
Многие из этих веществ, например, некоторые органические кислоты, образуясь в растении, тотчас же используются растительной клеткой для различных синтетических процессов; они не накапливаются в растении в большом количестве и являются промежуточными продуктами обмена веществ. Для выделения их из растений иногда необходимо прервать или как-то изменить цепь закономерных превращений веществ в клетке, т.е. предотвратить дальнейшее потребление этих веществ [7].
Некоторые из этих веществ, накапливаясь в растениях нередко в большом количестве, например, фенольные соединения, обусловливают тем самым специфику их обмена [7, 8].
Многочисленные вещества этого класса (их выделено значительно больше 1000) присутствуют практически во всех растениях. В своей основе они содержат бензольное кольцо, несущее одну или несколько гидроксильных групп, в том числе замещенных, окисленных до карбоксила, боковые цепочки из 1-3 углеродных атомов, часто циклизующиеся с бензольным кольцом в более сложные соединения. Условность объединения их в один химический класс демонстрируется чрезвычайным разнообразием действующих начал, синтезируемых растением на основе фенола и часто имеющих мало сходства с исходным веществом. Общность биосинтеза, пожалуй, основной повод для объединения [1, 7].
О химической пестроте класса свидетельствует отнесение к нему простых фенолов и ароматических кислот, полифенолов, катехинов, кумаринов, антахинонов, флавоноидов. Как и терпеноиды, фенольные соединения разных групп могут образовывать эфиры с углеводами, то есть гликозиды с многообразным фармакологическим действием, определяемым природой агликонов [1].
Значительно различается и их функциональная роль в растения. Одна из важнейших функций фенольных соединений - участие в окислительно- восстановительных процессах. Фенольные соединения выполняют в растениях также защитные функции. При механических повреждениях тканей в них начинается интенсивное новообразование фенольных соединений, сопровождающееся окислительной конденсацией в поверхностных слоях; продукты конденсации образуют защитный слой. Кроме того, некоторые фенольные соединения способны сообщать растениям устойчивость к заболеваниям [8]. Многие фенольные соединения являются антиоксидантами и находят все более широкое применение. Антиоксидантная активность фенольных соединений объясняется двумя обстоятельствами: 1) фенольные соединения связывают ионы тяжелых металлов в устойчивые комплексы, тем самым лишая последние каталитического действия; 2) они служат акцепторами образующихся при аутоксидации свободных радикалов (т.е. фенольные соединения способны гасить свободно- радикальные процессы) [4, 5, 9].
Из других свойств фенольных соединений следует отметить стимуляцию ими деления клеток в культуре растительных тканей, подавление прорастания семян, разобщение окислительного фосфорилирования и др [4, 6].
В целом фенольные соединения играют важную роль в обмене веществ растительной клетки [8].
Фенольные соединения также выступают и как один из факторов, определяющих особенности онтогенеза растений и влияющих на возобновление и распределение особей в ценопопуляциях [6, 8].
В природе фенольные соединения могут быть моно-, ди-, олиго- и полимерные [1, 8].
Многие из перечисленных выше групп этого класса соединений представляют большой и самостоятельный интерес для фитотерапии. Внутри они объединены некими общими фармакологическими свойствами, что позволяет дать им групповые характеристики [1].
В обширный класс фенольных соединений входит группа фенольных гликозидов, которые важны, как и для самих растений, так и широко применяются в медицине. Их я и хочу рассмотреть в своей курсовой работе.
1. Фенольные гликозиды
Фенолгликозидами называется группа гликозидов, агликоном которых являются фенолы, оказывающие дезинфицирующее действие на дыхательные пути, почки и мочевые пути. Фенольные соединения содержат ароматические кольца с гидроксильной группой. В этих соединениях сахара соединены с производными фенола [1].
Соединения, содержащие в ароматическом кольце больше одной гидроксильной группы, называются полифенолами. Они встречаются в различных частях многих растений - листьях, цветках (придают им окраску и аромат), плодах [8].
В природе распространены довольно широко. Встречаются в семействах ивовых, брусничных, камнеломковых, толстянковых и др [8, 10].
2. Физико- химические свойства. Химическое строение фенолгликозидов
Выделенные в чистом виде фенольные гликозиды - это белые кристаллические вещества, растворимые в воде, этиловом спирте, нерастворимые в этиловом эфире и хлороформе. Отличаются оптической активностью, способны к гидролизу при нагревании с минеральными кислотами [1, 11].
При гидролизе фенольных гликозидов образуются различные типы фенолов: арбутин (образуется гидрохинон), салицин (орто- гидроксибензиловый спирт), хелицин и спиреин ( салициловый альдегид), геин (эвгенол) и т.д [1, 11].
Фенольные гликозиды, со свободной гидроксильной группой дают все реакции, характерные для фенолов (реакция с железоаммониевыми квасцами, диазотирования и др.) [1, 2].
Первый фенолгликозид, выделенный из растений – салицин (рисунок 1)- представляет собой глюкозид салицилового спирта. Его получил из коры ивы французский ученый Леру (1828) [1, 2].
Салицин С13Р18О7- кристаллический глюкозид, горького вкуса, нейтральной реакции, трудно растворяется в холодной воде и спирте, легче в горячей воде и горячем алкоголе [1, 11].
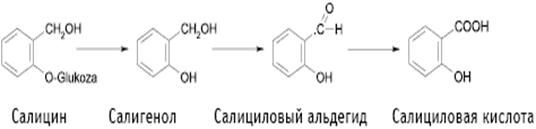
Рисунок 1 - Салицин
Арбутин (риcунок 2) (арбутозид, или эриколин)- гликозид фенольного типа, состав С12Н16О7∙½ Н2О, (бета- D- глюкопиранозид), принадлежит группе арил – бета - гликозидов (производное гидрохинона). Молекулярная масса 272.251 [1, 2].
Название по номенклатуре IUPAC: (2R, 3S, 4S, 5R, 6S) – 2 гидроксиметил-6- (4- гидроксифенокси) оксан-3,4,5- триол. Другие названия: арбутозид, вакцинин, гидрохинон- β-D- глюкопиранозид [1, 2, 11].

Рисунок 2 - Арбутин
Арбутин – горькое вещество, легко растворимое в горячей воде. Кристаллизуется в виде длинных, шелковистых игл. Температура плавления- 170º С (по другим источникам – 199.5ºС) [1,2].
С хлорным железом дает голубое окрашивание; разведенной серной кислотой гидролизуется с образованием сахара и гидрохинона [1,12].
В 1967 году при изучении химического состава родиолы розовой и родиолы четырехчленной были выделены тирозол и родиолозид (рисунок 3) [1, 2].
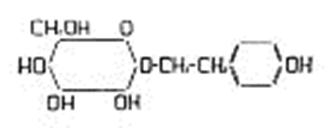
Рисунок 3 - Родиолозид
Позднее оказалось (Thieme, 1969), что родиолозид сходен с гликозидом салидрозидом (рисунок 4), выделенным Bridel и Beguin в 1926 году из ивы трехтычинковой (Salix triadra L., Salicaceae), и идентифицированным (1964,1965) как 2-[4- оксифенил] – этанол -1- β- D-гликопиранозид [2].
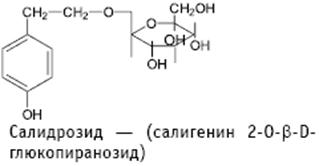
Рисунок 4 - Салидрозид
Родиолозид легко растворим в воде, низших спиртах, растворим в ацетоне, пиридине, плохо в диэтиловом эфире, хлороформе, этилацетате и не растворим в бензоле, петролейном эфире. С раствором хлорного железа родиолозид дает сине-фиолетовое окрашивание; как и тирозол, он вступает в реакцию с 1,2-нитрозанафтолом в присутствии азотной кислоты с образованием продуктов красно- оранжевого цвета (реакция специфична для паразамещенных фенольных соединений). При хроматографировании на тонком слое окиси алюминия Rf=0.48-0.49 (система n-бутанол-этанол-вода 5:1:2), при хроматографировании на бумаге Rf=0.68 (система n-бутанол-этанол-вода 5:1:2) и Rf=0.67 (система бутанол-уксусная кислота-вода 4:1:5) [12,13].
Кониферин (С16Н22О8хН2О) (рисунок 5)- фенольный гликозид. При ферментативном гидролизе распадается на глюкозид и конифериловый спирт С10Н12О3 - один из исходных продуктов при биосинтезе лигнина [1, 7].
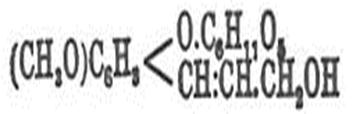
Рисунок 5 - Кониферин
Открыт Hartigom в камбальном соке Larix europaea, находится также в соке хвойных растений вообще. Найден также в свекловице и спарже. Белое кристаллическое вещество, Слабо растворим в холодной, хорошо в горячей воде и спирте. Точка плавления 185ºС. Водный раствор имеет горький вкус. Вращает влево (α) D20= -66,9. Не действует на Фелингову жидкость. Растворяется в концентрированной серной кислоте с красным цветом; при прибавлении воды раствор дает смолу индиго - синего цвета. С фенолом и концентрированной соляной кислотой, особенно на солнечном свете, окрашивается в густой синий цвет [2, 12].
3. Фармакологические свойства фенолгликозидов
Фенольные гликозиды - арбутин (арбутозид) расщепляется на глюкозу и свободный гидрохинон, а метиларбутин расщепляется на глюкозу и монометиловый эфир гидрохинона, оказывая слабое антибактериальное действие [9].
Он хорошо всасывается в тонкой кишке, фильтруется через почки в мочу. Для достижения необходимого лечебного эффекта богатые этим гликозидом растения необходимо использовать длительно и в достаточных количествах [4, 9].
Применение растений, содержащих арбутин, показывает, что их лечебный эффект значительно выше, чем чистого арбутина, что связано с наличием в растениях дубильных веществ и флавонов. Следует отметить, что больным со щелочной реакцией мочи назначать растения, содержащие арбутин, нецелесообразно, так как он не распадается до бактерицидно действующего гидрохинона [5].
В опытах на кроликах арбутин снижает уровень сахара в крови [4].
Арбутин, как гликозированный гидрохинон, может быть источником повышенной канцерогенной опасности, хотя утверждают также, что арбутин снижает риск возникновения рака. В немецком институте The German Institute Of Food Research (Потсдам) установлено, что микрофлора кишечника способна метаболизировать арбутин в гидрохинон, который является фактором канцерогенеза внутренних органов. Установлено, что 64-75% арбутина выводится с мочой, а арбутин, трансформированный в гидрохинон, обеспечивает антимикробное действие в мочевыводящих путях, что поясняет эффективность брусники в народной медицине, но пока нет доказанных данных относительно реального риска онкологических заболеваний от применения препаратов арбутина [3].
Гидрохинон обладает мочегонным и антисептическим действием эффективен при воспалительных заболеваниях мочевыводящей системы, интенсивно выводится из организма с мочой, что подтверждено в опытах на добровольцах после применения препаратов толокнянки [4, 9].
С арбутином связаны антиоксидантные свойства растений, содержащих данный гликозид. Арбутин тормозит перекисное окисление линолевой кислоты и обладает способностью нейтрализовать свободные радикалы в бесклеточных системах in vitro [5, 9].
На основе изучения кинетики доказано, что арбутин выступает в роли конкурентного ингибитора тирозиназы, и его действие является обратимым. Арбутин конкурирует с L-тирозином в процессе связывания последнего с активным центром фермента [5].
В исследовании на добровольцах установлено, что арбутин на 43.5% уменьшал развитие пигментации кожи при ультрафиолетовом облучении. В связи с этим предлагается использовать отвары растений для отбеливания кожи в косметологии [4].
Фенолгликозиды родиолозид, салидрозид и розавин обладают ярко выраженными адаптогенными и стимулирующими нервную систему свойствами, подобно препаратам женьшеня, аралии и элеутерококка. Салициловая кислота и ее производные известны как противовоспалительные, жаропонижающие и болеутоляющие средства [6, 9].
Салидрозид обладает бифункциональными свойствами, т.е. проявляет себя как ингибитор или инициатор окислительных процессов. Проявление того или иного свойства зависит от концентрации салидрозида в реакционной среде- при низких концентрациях салидрозид выступает как ингибитор окислительных процессов, при высоких – как инициатор [6].
По-видимому, этими химическими свойствами салидрозида определяется и его фармакологический эффект. В опытах на мышах, в малых дозах салидрозид действует стимулирующе на спонтанную активность мышей, а при больших дозах снижает двигательную активность интактных животных. По- разному влияет салидрозид на холинергические и моноаминергические процессы в центральной нервной системе в зависимости от доз используемого препарата [4, 6].
Фенолгликозид салицин, используется в народной медицине при лихорадочных состояниях, при воспалениях слизистых ротовой полости и верхних дыхательных путей (полоскания), при кожных заболевания (примочки) [5].
Учитывая фармакологические свойства салицина и используя достижения синтетической химии в 20 столетии научными работниками разных стран мира было синтезировано значительное количество органических соединений. Они со временем нашли широкое применение в фармации и научно- практической медицине как противовоспалительные и анальгетические средства [2, 4, 5].
4. Методы выделения и идентификации
Фенольные гликозиды из растительного материала извлекают этиловым и метиловым спиртами (96, 70 и 40º). В дальнейшем очистку спиртовых извлечений ведут общепринятым для гликозидов методом [12, 13, 14, 15].
Выделение индивидуальных соединений приводят, как правило, методом адсорбционной хроматографии на полиамиде, силикагеле, целлюлозе. В качестве элюирующих смесей используется вода и водный спирт, если адсорбентом служит полиамид или целлюлоза, либо различные смеси органических растворителей для всех перечисленных адсорбентов [1, 13, 14].
Фенольные гликозиды в лекарственном растительном сырье могут быть идентифицированы хроматографией в тонком слое сорбента или на бумаге [1, 12, 13, 14].
Для хроматографирования в тонком слое сорбента используют системы растворителей: 1) n-бутанол - уксусная кислота – вода (4:1:5); 2) n-бутанол - уксусная кислота – вода-ксилол (6:2:3:4); 3)хлороформ - метиловый спирт (8:2) [1, 12, 13, 14].
При хроматографии на бумаге используют 5, 10 и 15% - ную уксусную кислоту [1].
Для индивидуальных веществ определяют t-плавления, удельное вращение, снимают УФ, ИК спектры [1, 12, 14, 15].
Рассмотрим УФ и ИК спектры на примере арбутина. В связи с наличием в молекуле фенольных гликозидов ароматических С-С связей фенольные гликозиды имеют макисмум поглощения в УФ спектре при 270-300 нм. Максимум поглощения арбутина находится при 287 нм (в составе арбутина есть остаток гидрохинона с достаточной сопряжённой системой) и может быть использован как для качественной характеристики, так и количественного определения арбутина а растительном материале. При анализе УФ-спектров у растений, содержащих арбутин можно отметить, что на них присутствуют 2 максимума поглощения, характерных для данного соединения при 220 и 284 нм, причем интенсивность (выраженность) пиков соответствует содержанию арбутина в исследуемых видах. Например, при исследовании толокнянки, брусники, зимолюбки, черники и голубики, наибольшая интенсивность пика при 220 нм характерна для толокнянки, брусники и зимолюбки, менее выражены пики в этой области для черники и голубики (рисунок 6) [12, 14].
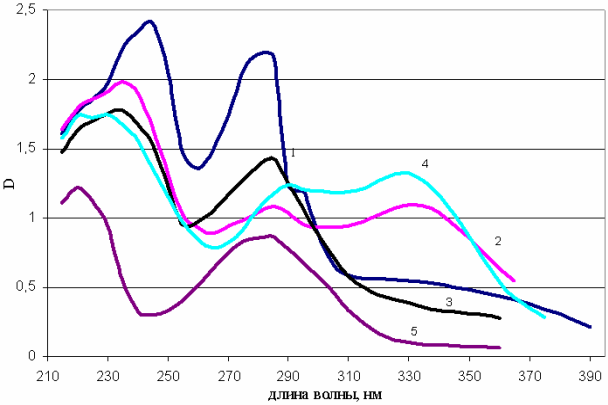 Рисунок 6 - УФ-спектры этанольных
экстрактов листьев брусники (1), толокнянки (2), зимолюбки (3), черники (4) и
голубики (5)
Рисунок 6 - УФ-спектры этанольных
экстрактов листьев брусники (1), толокнянки (2), зимолюбки (3), черники (4) и
голубики (5)
В ИК спектре арбутина имеются характерные полосы при 3200- 3400 смˉ¹, обусловленные наличием спиртовых и фенольных гидроксильных групп; полоса 1515,1460 , 1440 смˉ¹ типична для С=С- связей. Имеется ряд полос в области 800-1300 смˉ¹ (область “отпечатка пальцев”). Совпадение спектров исседуемого гликозида со спектром достоверного образца указывает на идентичность соединения. Для идентификации фенольных гликозидов широко используются химические превращения, анализ, ацетилирование, метилирование и т.д. и сравнение продуктов превращения с литературными данными для предполагаемого гликозида [12, 14].
Также сейчас распространяется идентификация фенолгликозидов с помощью метода ВЭЖХ [16, 20]. На рисунке ниже (риcунок 7) показана ВЭЖ-хроматограмма водного экстракта зимолюбки зонтичной, на которой по УФ-спектрам в сравнении с достоверным образцом идентифицирован арбутин. В данном конкретном случае, анализ проводился на высокоэффективном жидкостном хроматографе «Миллихром-А-02» с последующей компьютерной обработкой результатов исследования с помощью программы МультиХром-СПЕКТР для Windows. В качестве неподвижной фазы использовали колонку ProntoSIL 120-5-C18 AQ, №80303 размером 2,0×75 мм, размер частиц – 5,0 мкм; в качестве подвижной фазы – [4M LiClO4+0,1M HClO4] : H2O в соотношении 5:95. Скорость подачи элюента – 100,00 мкл/мин. Температура – 40 °C. Давление – 2,0 MPa. Продолжительность анализа – 115 мин. Параллельно с испытуемым раствором в хроматограф вводились растворы достоверных образцов арбутина, гидрохинона и рутина. Детектирование данных веществ проведены по УФ-спектрам при длинах волн 210–300 нм [14].
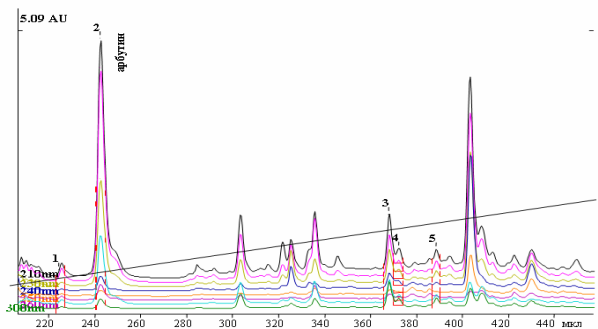
Рисунок 7 - ВЭЖ-хроматограмма водного экстракта зимолюбки зонтичной
Существенную практику препаративного выделения индивидуальных растительных соединений из-за трудоемкости технологических приемов и высокой себестоимости конечного продукта следует считать оправданной при наличии в них преобладающих компонентов [2].
5 .Качественное определение
Фенольные гликозиды, имеющие свободную гидроксильную группу, дают все реакции, характерные для фенолов, например, с железоаммониевыми квасцами, реакцию диазотирования и др [1, 11].
В случае если фенольный гидроксид гликозирован, как у салицина, реакции проводят после предварительного гидролиза гликозида кислотами или ферментами. Эти же качественные реакции используют для обнаружения фенольных гликозидов на хроматограммах [1, 13].
В случае хроматографирования в тонком слое силикагеля хроматограммы можно обработать кроме перечисленных реактивов еще и 4%- ной Н2SO4 в абсолютном этиловым спирте [13].
При этом фенольные гликозиды в зависимости от строения обнаруживаются в виде желтых, красных, оранжевых и голубых пятен [13].
При обработке хроматограмм раствором нитрата серебра и щелочью фенольные гликозиды обнаруживаются в виде коричневых пятен с различными оттенком [1, 13].
При обработке хроматограмм реактивом Паули фенольные гликозиды в зависимости от строения проявляются в виде желтых, оранжевых или красных пятен [1, 13].
6. Методики обнаружения фенольных гликозидов
Ниже я приведу некоторые возможные методики обнаружения фенольных гликозидов в ЛРС, описанные в литературе и НД [1, 2, 8, 12-15].
1. 0.5 гр измельченного сырья кипятят с 10 мл Н2О 2-3 минуты и после охлаждения фильтруют. К 1 мл фильтрата прибавляют кристаллик сульфата закисного Fe, жидкость окрашивается сначала в сиреневый, затем темно- фиолетовый цвет, и наконец, образуется темно- фиолетовый осадок (арбутин) [1].
2. К 1 мл фильтрата (в фарфоровой чашке) прибавляем 4 мл раствора аммиака и 1 мл 10% раствора Na фосфорно - молибденовокислого в 10%- ной HCl; появляется синее окрашивание (арбутин) [1, 2].
3. 0.5 гр мелкоизмельченного растительного сырья заливают 5 мл этилового спирта и экстрагируют при периодическом встряхивании и слабом нагревании на водяной бане в течение 1 часа [1, 14].
Полученное извлечение с помощью капилляра наносят на бумагу (3-4 прикосновения капилляра) и хроматографируют восходящим способом в 5%- ной уксусной кислоте до прохождения фронта растворителя 15-17 см (хроматограмма проходит в течение 1 часа при использовании бумаги FN-3). Хроматограмму вынимают, высушивают, обрабатывают раствором 10%- ной спиртовой щелочи и затем реактивом Паули [14].
Арбутин имеет самое высокое значение R=0.75, отделяется от сопутствующих гликозидов и проявляются в виде ярко-красного пятна. Аналогичные результаты можно получить на пластинке “Силуфол” при хроматографировании в системе хлороформ-этиловый спирт (7:3) с последующей обработкой раствором щелочи и реактивом Паули [14].
Хроматограммы до и после обработки реактивами целесообразно просматривать в УФ свете с целью идентификации сырья по отдельным компонентам [16].
Схема хроматограммы экстракта брусники показана на рисунке 8 [14].
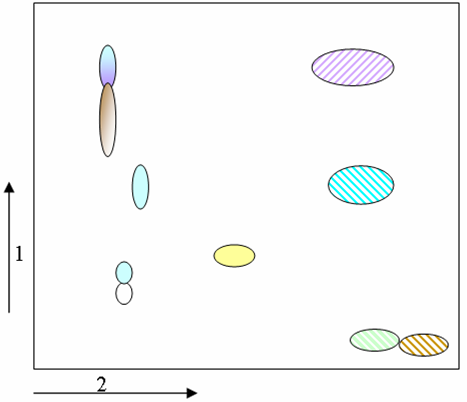
Рисунок 8 - Схема хроматограммы экстракта брусники
1-е направление – 15% уксусная кислота;
2-е направление – БУВ (н-бутанол – уксусная
кислота – вода)
4. Согласно ГФ РБ и Европейской Фармакопее [16, 17] идентификацию фенольных гликозидов в листьях толокнянки проводят методом тонкослойной хроматографии. К 0.5 г. измельченного сырья прибавляют 5 мл смеси из равных объемов метанола и воды, нагревают с обратным холодильником в течение 10 минут. Горячее извлечение фильтруют. Фильтр промывают смесью из равных объемов метанола и воды и доводят до объема 5 мл этим же растворителем.
В качестве раствора сравнения используют 25 мг арбутина, 25 мг галловой кислоты и 25 мг гидрохинона растворяют в метаноле и доводят до объема 10,0 мл этим же растворителем.
Пластинка: ТСХ пластинка со слоем силикагеля.
Подвижная фаза: кислота муравьиная безводная–вода-этилацетат (6:6:88 об/об/об).
Наносимый объем пробы: 10 мкл раствора сравнения и 20 мкл испытуемого раствора в виде полос.
Фронт подвижной фазы: не менее 15 см от линии старта.
Высушивание: при температуре от 105 до 110 С до исчезновения запаха растворителей.
Проявление: пластинку опрыскивают раствором 10 г/л дихлоринохлоримида в метаноле. Затем опрыскивают раствором 20 г/л натрия карбоната безводного. Просматривают при дневном свете.
Согласно ГФ РБ [14] идентификацию арбутина в листьях брусники проводят следующим образом.
Испытуемый раствор. К 0,5 г измельченного сырья прибавляют 5 мл смеси из метанола и воды (50:50, об/об) и кипятят с обратным холодильником в водяной бане в течение 10 мин. Горячее извлечение фильтруют. Фильтр и пробирку промывают смесью из метанола и воды (50:50, об/об) и доводят до объема 5 мл этим же растворителем.
Раствор сравнения. 2,5 мг арбутина растворяют в 5 мл метанола.
Пластинка. ТСХ пластинка со слоем силикагеля GР.
Подвижная фаза: этилацетат — кислота муравьиная безводная — вода (44:3:3,об/об/об).
Наносимый объем пробы: по 10 мкл в виде полос.
Фронт подвижной фазы: не менее 15 см от линии старта.
Высушивание: при температуре от 100°С до 105°С.
Проявление: пластинку опрыскивают раствором 10 г/л 4-аминопиразолона, затем раствором 20 г/л калия ферроцианида и проявляют в парах аммиака. Просматривают при дневном свете.
Результаты: Арбутин: зона красного цвета. На хроматограмме испытуемого раствора в верхней половине могут обнаруживаться и другие зоны. Пирозид - зона красного цвета.
7. Количественное определение
При количественном определении фенолгликозидов применяют химические (титриметрические) и инструментальные (спектрофотометрические и хроматографические) методы анализа.
Нормативно-техническая документация предусматривает количественное определение арбутина в листьях толокнянки и брусники. Метод определения основан на иодометрическом титровании гидрохинона, полученного после извлечения и гидролиза арбутина [16].
Разработан спектрофотометрический метод определения салидрозида в экстрактек корневищ с корнями родиолы розовой, который можно использовать для количественного определения салидрозида в растительном материале [1].
Исходя из строения фенольных гликозидов и их УФ спектров, возможно количественное хромато-спектрофотометрическое определение всех представителей этой группы [14].
И хотя сейчас всё более широкое применение получают инструментальные методы установления колличественного содержания фенолгликозидов [16], ещё применяется и включён в НТД [16] титриметрический метод количественного определения.
Рассмотрим подробнее методы количественного определения фенолгликозидов в ЛРС.
7.1 Титриметрический метод количественного определения фенолгликозидов [16]
Около 0.5 гр (точная навеска) сырья, измельченного и просеянного через сито с диаметром отверстий 1 мм, помещают в колбу вместимостью 100 мл, заливают 50 мл воды и нагревают с обратным холодильником поддерживая слабое кипение, в течение 30 мин. Горячее извлечение фильтруют в мерную колбу вместимостью 100 мл через бумажный фильтр, избегая попадания частиц сырья на фильтр. В колбу с сырьем повторно прибавляют 25 мл воды и кипятят в течение 20 мин. Горячее извлечение вместе с сырьем переносят на тот же фильтр и остаток на фильтре дважды промывают горячей водой порциями по 10 мл. К фильтрату прибавляют 3 мл раствора свинца (II) ацетата основного, перемешивают, охлаждают и доводят водой до объема 100,0 мл. Колбу помещают в водяную баню и выдерживают до полной коагуляции осадка. Горячую жидкость полностью отфильтровывают в колбу через бумажный фильтр, прикрывая воронку часовым стеклом. Охлаждают, к фильтрату прибавляют 1 мл кислоты серной, колбу взвешивают с точностью до 0,01 г и кипятят с обратным холодильником в течение 1,5 ч, поддерживая равномерное и слабое кипение. Охлаждают до комнатной температуры, взвешивают, доводят массу колбы до первоначальной водой, и полностью отфильтровывают через бумажный фильтр в колбу вместимостью 250 мл. К фильтрату прибавляют 0,1 г порошка цинка и встряхивают в течение 5 мин.
Жидкость нейтрализуют натрия гидрокарбонатом (около 1—2 г) по красной лакмусовой бумаге, прибавляют еще 2 г натрия гидрокарбоната и после его растворения фильтруют через бумажный фильтр.
50,0 мл фильтрата переносят в плоскодонную колбу вместимостью 500 мл, прибавляют 200 мл воды и немедленно титруют из микро- или полумикробюретки 0,1 М раствором йода до появления синего окрашивания, не исчезающего в течение 1 мин, используя в качестве индикатора раствор крахмала, свободный от йодидов.
1мл 0.1н раствора йода соответствует 0.01361 арбутина. Процентное содержание арбутина в растительном материале х в пересчете на абсолютно сухое сырье вычисляют по формуле:
Х= V0.01361∙2∙100∙100 / m (100-w)
где V - объем 0.1н раствора йода, израсходованного на титрование, мл;
m- масса навески сырья, гр; w - потеря в массе сырья при высушивании, %
Содержание арбутина в сырье регламентируется НТД.
Известно, что в зеленых листьях бадана толстолистного содержится арбутина 20%, в листьях брусники- 10-16%.
Способ выделения арбутина из листьев бадана включает: двух- кратную экстракцию сырья кипящей водой, фильтрацию и сепарирование извлечения, осаждение полифенолов раствором ацетата свинца, отделение осадка, упаривание фильтрата до сухого остатка, двух- кратную эктракцию сухого остатка 96%-ным этанолом, упаривание этанольного экстракта и обработка маслянистого остатка смесью хлороформ- этанол, кристаллизация арбутина из этой смеси. Выход арбутина-4%. Способ позволяет получить получить химически чистый арбутин без примесей, что подтвердается данными УФ-, ИК, ПМР-спектров. УФ- спектр арбутина имеет максимальное поглощение при 285 нм, в ИК- спектре имеются для характерные для арбутина полосы поглощения при 817, 831, 1513, 1447.
7.2 Инструментальные методы
Среди инструментальных методов определения можно выделить фотоэлектроколориметрический и спетрофотометрический. Рассмотрим эти методы на примере колличественного определения арбутина.
В основе определения арбутина фотоэлектроколориметрическим методом лежит реакция образования азокрасителя после его взаимодействия с диазотированным сульфаниламидом (например, сульфацил-натрий) [14].
Количественное содержание определяется по калибровочному графику. Осаждение полифенолов проводится раствором свинца ацетата основного. Потери арбутина при данном способе определения составляют около 1,5%. Это объясняется тем, что очистка извлечения от сопутствующих полифенольных соединений раствором свинца ацетата основного приводит к соосаждению арбутина [14].
Спектрофотометрический метод для определения арбутина основан на измерении оптической плотности в видимой области спектра после получения антипиринового красителя. В качестве реактивов, например, используют 2% водный раствор 4-аминоантипирина, аммиак и 2% водный раствор калия феррицианида. Окрашенный продукт извлекают хлороформом и измеряют оптическую плотность окрашенного продукта на спектрофотометре при длине волны 455 нм. [14, 15].
8. ЛР и ЛРС, содержащие феногликозиды
8.1 Брусника обыкновенная(Vaccinium vitis idaea, сем.-Vaccinaceae)
Вечнозеленый низенький ветвистый кустарничек, высотой до 25 см. Корневище ползучее. Стебли прямостоячие, ветвистые. Листья очередные, мелкие, кожистые, блестящие, эллиптические, с завернутыми на нижнюю сторону краями, с черными точесными железками. Цветки белые или розоватые, в кистях на концах ветвей, венчик колокольчатый. Цветет в мае- июне. Плод - округлая многосеменная, шаровидная красная ягода.Плоды созревают в августе- сентябре [10].
Распространение брусники связано с равнинными сухими и свежими с моховым покровом сосновыми борами, а также с пихтовоелово- кедровой горной тайгой, где в надпочвенном покрове преобладают мхи, встречается черника, грушанки, линнея [10].
Химический состав. Фармакологические свойства. Листья и ягоды содержат гликозид арбутин (в листьях до 9%), который в организме отщепляет гидрохинон, а также флавоноиды, дубильные вещества, органические кислоты- яблочную, лимонную, винную, бензойную, обладающую антисептическим действием, сахара, аскорбиновую кислоту, микроэлементы, финонциды, каротин и другие вещества [1, 2].
Применение. Водные настои и отвары листьев применяют в научной медицине как мочегонное, антисептическое и вяжущее средство при воспалениях почек и мочевого пузыря, поносах, подагре и ревматизме. Ягоды брусники рекомендуют при авитоминозах. Сушеные ягоды входят в витаминные и мочегонные сборы. Морс из ягод полезен при лихорадящих заболеваниях [9].
В народной медицине ягоды брусники применяют при анацидных гастритах, диабете, поносах, подагре и ревматизме [4].
Настой листьев употребляют при воспалениях почек и мочевого пузыря. Листья брусники заваривают вместо чая как средство, снимающее усталость [4].
Лекарственные формы. Настой.Столовая ложка листьев настаивают 30 минут в стакане кипятка, охлаждают и пьют по столовой ложке 3-4 раза в день [9].
Отвар. 2-3 чайные ложки кипятят в стакане воды 15 минут, выпивают в течение дня [9].
Сбор, обработка, сушка. Листья собирает до цветения (при более позднем сборе они при сушке чернеют), в том числе ранней весной- перезимовавшие под снегом; сушат в сухом теплом помещении или на чердаках, разложив тонким слоем (3-5 см) на бумаге или ткани, часто перемешивая. Выход сухого сырья 20-22%. Сухие листья упаковывают в мешки весом по 20-25 кг и хранят в сухих, хорошо проветриваемых помещениях на стеллажах. Срок хранения не установлен [10].
Ягоды собирают в стадии полной зрелости руками или специальными граблистыми совками в небольшие корзины. Очещенная от примесей, недозрелых и поврежденных ягод брусника затаривается в осиновые, липовые или еловые 50-100- литровые бочки с вложенными внутрь бочки полиэтиленовыми мешками. После заполнения ягод мешок завязывается льняным шпагатом [10].
8.2 Толокнянка обыкновенная(Arctostaphylos uva ursi, сем.-Ericaceae)
Вечнозеленый распростертый кустарничек с ползучими и приподнимающимися побегами, длиной 20-50 см. Листья кожистые, короткочерешковые, сверху более темно-, снизу- более светло- зеленые, блестящие. К основанию листья клиновидно сужены, обратнояйцевидной формы, твердые и ломкие. Цветки собраны с малоцветковые кисти и расположены на верхушках веток. Венчик кувшинчатый, розовый или белый, с 5 изогнутыми наружу зубчиками. Плод сферическая красная ягода с 6 семенами. Цветет с мая по июль [10].
Встречается на сухихи каменистых местах и лесных полянах в хвойных лесах. Встечается почти по всей Европе ( без крайних южных районов) [10].
Химический состав. В сырье содержатся фенольные гликозиды- арбутин и метиларбутин (в среднем около 10%). В этой смеси из гликозидов, в зависимости от происхождения, метиларбутин
Рисунок 10 - Толокнянка варьирует от 5 до 45%. Содержание арбутина в листьях не должно быть меньше 6%. Некоторое сырье содержит только арбутина около 9%, небольшие количества свободного гидрохинона, дубильные вещества ( галлолинины) около 20%, флавоноидные вещества, урсоловую кислоту и др [1, 2].
Установлено, что осенью содержание арбутина в листьях толокнянки выше, чем весной [2].
Сотрудниками Санкт-Петербургского химико–терапевтического института разработана технология получения жидкого концентрата из листьев толокнянки с содержанием арбутина 14-15% (для экстракции использовали 20% водно- спиртовую смесь) [2].
Фармакологические свойства. В опытах in vitro водно- спиртовые и этилацетатные экстракты листа толокнянки угнетают рост золотистого стафилококка (Staphylococcus aureus), энтерококка (Enterococcus faecalis), сенной палочки (Bacillus subtilis), энтеробактерий (Escherichia coli, Enterobacter aerogenes , Salmonella typhimurium, Proteus mirabilis, Proteus vulgaris) и синегнойной палочки (Pseudomonas aeruginosa). Тем не менее 95% этанольный и хлороформный эктсракты растения противомикробными свойствами не обладают. Водный экстракт листа толокнянки угнетает также рост кариогенного Streptococcus mutans OMZ176 (Namba T. Etc., 1981). Кроме того, он проявляет противовирусную активность – в концентрации 10% угнетает репродукцию вирусов простого герпеса типа 2, гриппа А2 (штамм Mannheim 57) и оспенной вакцины в культуре клеток [5].
Уроантисептическое действие обусловлено наличием в листьях фенольных гликозидов- арбутина (арбутозида) и метиларбутина [2].
Доказано слабое антибактериальное действие отвара из листьев толокнянки на туберкулезные микобактерии. Сырье обладает также и слабым диуретическим эффектом, обусловленным влиянием на канальцевый эпителий почек [5].
Применение. Листья толокнянки широко применяют в виде отвара, настоя, экстракта ка дезинфицирующее и мочегонное средство. Применять листья толокнянки как антисептик для лечения хронического цистита и пиелита можно только при щелочной реакции мочи. Имеются данные и о хорошем эфекте при лечении поносов и гематурии, а также выжущем действии [5, 9].
Лекарственная форма. Столовую ложку нарезанных мелких листьев залить 2 стаканами холодной воды, оставить на ночь и процедить. Получают суточную дозу, которую следует пить по192 столовых ложки 3-4 раза в день. Некоторые авторы рекомендуют применять в виде отвара [4, 5, 9].
Лекарственное сырье представляет собой листья растения, собранные во время цветения и высушенные при обыкновенной температуре [10].
8.3 Ива
Известно примерно 50 выдов ив. Медицинское применение имеют ива белая (ветла), ива козья, ива ломкая и другие [9, 10].
Все ивы- многолетние, деревянистые растения, деревья ( ива белая, ива ломкая) или кустарники ( ива серая, ива сибирская и т.д.) с прстыми листьями с прилистниками на черешках, сверху зелеными, снизу часто белоопушенными. Цветки без околоцветников, однополые, собраны в сережки. Цветут до появления листьев или во время олиствения [10].
Ивы обычно растут по берегам и ручьев, под пологом леса, нередко у дорог, в садах, на болотых повсеместно [10].
Химический состав. Кора ивы белой содержит значительный арсенал биологически активных веществ, среди которых наиболее важными являются фенольный гликозид- салицин, производные салициловой кислоты и флавоноиды [1, 2]. Сотрудник Фармацевтического института Университета им.Карла Маркса г.Лейпцига в Германии Y. Tieme в 60-ых годах с помощью хроматографических и спектральных методов анализа в коре разных видов ивы идентифицировал гликозиды салициловой кислоты, среди которых определены такие вещества, как салицин, гликозид, расщепляющийся при ферментативном гидролизе на спирт салигенол, который в дальнейшем гидролизуется на салициловый альдегид и салициловую кислоту. Поэтому в коре ивы также имеется и свободная салициловая кислота. Кроме салициловой кислоты в коре и листьях разных видов ивы помещаются другие гликозиды салициловой кислоты, в частности салидрозид, саликозид, салирепозид, фрагалин, саликортин, триандрин, вималин, тремулоидин и другие соединения [2].
О. Dytkowska (1964) при разработке хромато - спектрофотометрического метода количественного определения салициловых гликозидов выяснила, что наибольшее количество гликозидов в перерасчете на салицин помещается в коре ивы ушастой - до 0.367%. В коре ивы белой количество фенолгликозидов в пересчете на салицин составляет 0.106% [4].
Кроме гликозидов производных салициловой кислоты, в коре и листьях разных видов ивы насчитывается до 5% флавоноидов, среди которых выявлены антоцианы и их гликозиды, в частности пурпуринидин, 3-глюкозид цианидина, 3- глюкозид дельфинидина, катехины, эпикатехин, галлокатехин, флавоноиды [1].
Проводились исследования содержания фенолгликозидов и флавоноидов в листьях ивы рода Salix, произрастающих в РБ(ВГМУ) [18]. Материалом для исследования являлись образцы листьев ив 13 видов, заготовленных в окрестностях г.Витебска: Salix rosmarinifolia L (Ива розмаринолистная), S. Cinerea L. (Ива пепельная ), S.purpurea L. (Ива пурпурная), S. triandra L. (Ива трехтычинковая), S. aurita L. (Ива ушастая), S. pentandra L.(Ива пятитычинковая), S. caprea L. (Ива козья), S. dayclados Wimm. (Ива шерстистопобеговая), S. wiminalis L.(Ива корзиночная, ива прутьевидная), S.alba L. (Ива белая), S. myrsinifolia L. (Ива чернеющая), S.acutifolia Willd. (Ива остролистная), S. fragilis L. (Ива ломкая). Сушка воздушно- теневая.
Количественная определение фенолгликозидов в пересчете на салидрозид проводили по методике ГФ XI на сырье родиолы розовой.
Содержание фенолгликозидов в листьях большинства изученных видов не превышает 1%. Максимальное содержание группы фенолгликозидов было отмечено у ивы прутьевидной и ивы розмаринолистной, 2.49% и 2.29% соответственно. Виды ив, относящиеся к одной секции, показывали сходное содержание флавоноидов. Связи накопления фенолгликозидов с таксономическим положением не выявлено.
Зависимость содержания флавоноидов и фенолгликозидов в листьях ив от их потребности в аэрации почв выражается сложной кривой с двумя максимумами. Наиболее интересным фактом является как бы зеркальное расположение пиков накопления фенолгликозидов по отношению к накоплению флавоноидов: максимуму содержания фенолгликозидов соответствует минимум содержания флавоноидов. Это может быть связано с конкуркнтными путями биосинтеза данных классов соединений. Наиболее перпективным видом ив из числа произрастающих в РБ для создания препаратов с адаптогенным действием является ива прутьевидная.
Фармакологические свойства и применение. В медицине отвар коры ивы употребляют при поносах, жаропонижающее при остром ревматизме, малярии и т.д. Используется для полосканий при воспалении слизистых оболочек и как обеззараживающее средство для очищения воды от бактерий. Кора входит в состав потогонных чаев [4, 5, 9].
В народной медицине отвар коры употребляют в основном при лихорадочном состоянии (вместо хинина), ревматизме, как вяжущее и противовоспалительное при хронических поносах, как желчегонное, при катарах желудка, заболеваниях селезенки [4].
Отвар мужских соцветий ивы козьей пьют при воспалении почек. Иногда оказывает глистогонное действие [4].
Кору собирают ранней весной, до цветения и развертывания листьев сушат в тени. Мужские сережки собирают в пору цветения, сушат в тени, рассыпаны тонким слоем [10].
8.4 Красная щетка (Родиола холодная, сем.-Crassulaceae)
Красная щетка (родиола холодная)- произрастает только в горах Алтая [6].
Прием препаратов на основе красной щетки рекомендован в качестве дополнительного источника гликозида - салидрозида. С лечебной целью коренные алтайцы используют корни растения, удивительно похожие на щетку или кедровые лапки [6].
Химический состав. Многокомпонентный химический состав красной щетки (гликозид салидролизид, антоцианы, дубильные вещества и др.) обуславливает многофункциональность действия [1, 2].
Фармакологические свойства и применение. Одно из основных действующих веществ красной щетки - гликозид салидролизид способствует проявлению онкопротекторных, противовоспалительных, противоинфекционных и адаптогенных свойств растения, устраняя эндокринные нарушения при гинекологических заболеваниях, патологии щитовидной железы, надпочечников. Антоцианы вызывают профилактический и лечебный эффект при заболеваниях бактериальной, вирусной, грибковой этиологии [6].
Красная щетка оказывает выраженное кровоостанавливающее действие, снимает спазмы головного мозга, очищает кровеносную систему, стабилизирует артериальное давление, восстанавливает формулу крови и нужна, в первую очередь, тем, у кого лейкемия, лимфолейкоз, лимфогранулематоз [5, 6].
По мнению народных целителей - красная щетка уникальный природный гормон, устраняющий эндокринные нарушения: щитовидной железы, лимфоузлов, надпочечников и другие. Он обладает сильным противовоспалительным, антибактериальным, иммуностимулирующим действием, нормализует обмен веществ, улучшает энергетический обмен в мышцах и центральной нервной системе [4].
Лекарственная форма. 40-50 гр корешков измельчить, залить 0.5 л водки и настоять месяц в темном месте, периодически встряхивая. Пить по 1 ч.л. с 1/3 ст. воды три раза в день до еды [5].
8.5 Родиола розовая (Rhodiola rosea, сем.-Crassulaceae)
Родиола розовая - одно из популярнейших лекарственный растений. Родиола розовая лишь в 60-ых годах прошлого столетия была идентифицирована как «золотой корень». С этого момента под рукововодством Е.А.Краснова и А.С.Саратикова начинается изучение химического состава родиолы розовой как фармакопейного вида. В ней содержатся вещества, стимулирующие нервную систему и обладающие адаптогенными свойствами, т.е. повышающие сопротивляемость организма человека при неблагоприятных воздействиях [4, 6, 9].
Многолетнее травянистое растение с утолщенным бронзовым, внутри лимонно- желтым корневищем с запахом розового масла и горьковато – вяжущим вкусом. Стебли прямые, ветвистые, высотой до 70 см в благоприятных условиях и до 10 см в угнетенных. Листья светло- зеленые, нежные, мясистые, овально- яйцевидные, часто с зубчатыми краями, очередные. Цветки мелкие, однополые, Рисунок 12 - Родиола розовая двудомные, венчики четырехлепестные, золотисто – желтые, краснеющие перед созреванием плодов. Собраны в щитковидное соцветие на верхушках стеблей. Цветет в июне- первой половине июля. Плод - прямостоячая листовка с отогнутым наружу носиком [10].
Впервые растение описал в I веке н.э. врач Диоскорид. Научное название дано Карлом Линнеем в 1755 году, видовое – rosea- растение получило потому, что запах свежеразломанного корневища немного напоминает запах розы [10].
Растет чаще всего на сырых лугах, по каменистым берегам горных рек и ручьев [10].
Золотой корень известен на Алтае как средство, повышающее выносливость и работоспособность человека. Чабаны и охотники во время трудных переходов по горам издавна пьют чай, используя в качестве заварки высушенный корень родиолы. Вообще растение это применяли при многих болезнях, но способы лечения сохраняли в тайне. Старинное алтайское поверье гласит: тот, кто найдет золотой корень, до конца дней своих будет удачлив и здоров, проживет два века. Широкое применение находит родиола розовая в восточной медицине, ее называют даже «тибетским женьшенем» [6].
Химический состав. Основными биологическими активными веществами являются гликозид – родиолозид, флавоноиды- производные гербацетина, трицина и кемпферола, гликозиды коричного спирта, монотерпены, дубильные вещества (около 20%), эфирное масло и органические кислоты, флавонолигнаны, стероиды, алкалоиды, органические кислоты [1].
Фармакологические свойства и применение. Химическое исследование родиолы розовой и изучение воздействие ее препаратов на человека началось с 1961 года в Томском медицинском институте и Биологическом институте Сибирского отделения АН СССР. Стимулирующее и тонизирующее свойства препаратов родиолы доказаны экспериментами на животных и наблюдениями в клиниках. Основное действующее вещество, от которого зависят специфические свойства родиолы розовой- фенольный гликозид родиолозид. С 1975 года Фармакологическим комитетом Минздрава СССР разрешен к выпуску препарат «экстракт родиолы жидкий». Его назначают как стимулирующее и адаптогенное средство для повышения умственной и физической работоспособности практически здоровых людей и для лечения функциональных заболеваний нервной системы. Экстракт родиолы розовой противопоказан при резко выраженных симптомах повышенной нервной возбудимости и истощаемости корковых клеток мозга, лихорадочных состояниях, гипертонических кризах [4, 5, 9].
Очищенный препарат родозин оказывает ан6алогичное стимулирующее и адаптогенное действие и обладает меньшей токсичностью, чем экстракт золотого корня, тормозит развитие лейкоцитоза и вызывает реакцию организма при различной интоксикации [6].
В народной медицине водочную настойку корневища (1:10) применяют при заболеваниях желудка, малярии, нервных болезнях, импотенции, упадке сил, переутомлении и как общеукрепляющее и тонизирующее средство [4].
Лекарственная форма. В домашней обстановке из 100 г свежесобранных корней или 50 гр высушенных можно приготовить 500 гр экстракта. Корень заливают сорокаградусным спиртом или водкой, дают настояться семь дней в темном месте, затем процеживают через марлю и отделяют экстракт от использованных кусков корня [4].
Заготовка. Раньше запасы сырья родиолы розовой были значительны. Однако неорганизованные и бессистемные сборы, часто просто варварское уничтожение этого растения привели к тому, что естественные запасы сильно сократились или даже исчезли совсем в некоторых регионах, особенно на Алтае. Родиола розовая занесена в Красную книгу «Дикорастущие виды флоры СССР, нуждающиеся в охране», в региональную Красную книгу «Редкие и исчезающие растения Сибири» [6, 10].
Для восстановления зарослей родиолы требуется 15-20 лет. Ученые рекомендуют создавать специальные заказники и промышленные плантации расьения, сторого соблюдать правила заготовок. В Горном Алтае заготовки родиолы розовой строго регламентированы и осуществляются по лицензиям республиканского комитета по охране природы. Родиола розовая хорошо растет в культуре, но в промышленных масштабах ее не выращивают Установлено, что в культуре процентное содержание действующих веществ у родиолы снижается, но увеличивается масса корневищ, число закладываемых на корневищах почек возобновления, количество семян [6].
Так что общая биологическая продуктивность родиолы в культуре компенсирует уменьшение процентного содержания действующих веществ [6].
8.6 Бадан толстолистный (Bergenia crassifolia (L.) Fritsch., сем.-Saxifragaceae)
Бадан толстолистный или чагирский чай многолетнее травянистое растение, высотой до 50 см с мясистым ползучим сильноразветвленным корневищем и мощным корнем. Листья крупные, кожистые, темно- зеленые, к осени краснеющие, собраны в прикорневую розетку, зимующую под снегом. Цветки лилово- щитковидном соцветии на верхушке голого стебля. Цветет с мая до июля, в зависимости от географической широты и высоты местности [10].
Химический состав. Растение отличается высоким содержанием дубильных веществ не только в корнях (25%), но и в листьях (10- 20%). Кроме того, во всех его частях обнаружено значительное количество гликозида арбутина, а в листьях также крахмал, сахара, фитонциды, витамин С и микроэлементы (марганец, железо и медь). В корневищах, кроме того, найден бергенин- производное изокумарина [1, 2].
Фармакологические свойства и применение. Препараты бадана обладают способностью суживать кровеносные сосуды и уплотнять сосудистую стенку, а также выраженным и противовоспалительным и бактерицидным действием. Фармакологические и клинические исследования показали, что экстракт из корней бадана действует на дизентерийную палочку [2, 5].
По данным омских фармакологов, бадан понижает артериальное давление и увеличивает частоту сердечных сокращений [19].
Из корневищ и корней бадана приготовляют жидкий экстракт, назначаемый как вяжущее и антисептическое средство при лечении колитов, энтероколитов и других желудочно- кишечных расстройств неинфекционного происхождения, не действующее при этом на нормальную микровлору организма. Иногда его применяют при консервативном лечении эрозий шейки матки, а также для полосканий при стоматитах и гингивитах. Из листьев готовят препараты бергальбин и беркрассин для лечения воспалительных процессов мочевых путей [5].
Экстракт из листьев показал антистрессорное, антигипоксическое и стимулирующее работоспособность действие [5].
В народной медицине бадан издавна применяют как сильное вяжущее, противовоспалительное, кровоостанавливающее и дезинфицирующее средство при расстройствах желудочно- кишечного тракта, изъязвлении и воспалении слизистой оболочки полости рта и носа, головной боли, женских болезнях [4].
Порошком из корней присыпают долго незаживающие раны и мокнущие сыпи. Чай из сухих листьев бадана- признанный тонизирующий напиток [4, 5].
В тибетской медицине бадан применяют при туберкулезе, воспалении легких, желудочно- кишечных заболеваниях, суставном ревматизме, а также как жаропонижающее средство [4].
Лекарственная форма. Отвар корневищ бадана. Готовят из расчета одна столовая ложка на стакан воды. Принимают по 1-2 столовые ложки 2-3 раза в день [4, 5].
Заготовка.Сушка. Практически сырье можно заготовлять все лето с оборотом (возвратом на одно и то же место)- при сборе листьев в 3-4 года и корневищ - в 10 лет [10].
Срезанные ножом листья откладывают отдельно от корневищ. Последние слегка провяливают на деревянных вешалах, затем досушивают в сушилках до воздушно- сухого состояния [10].
Заключение
В заключение своей курсовой работы мне хотелось бы сделать следующие выводы:
1 Лекарственные растения в народной медицине используются с древних веков до нашего времени, количество лекарственных растений многообразно. И поиски все новых достижений в фармакогнозии не останавливаются, и появляются новые методы исследований, что позволит выделить еще большее количество лекарственных растений и лекарственного растительного сырья [2, 4, 5].
2. Фенольные гликозиды оказывают самое различное действие на организм человека. Но, необходимо отметить, что несмотря на применение растений, содержащих фенольные гликозиды, в современной терапевтической практике, все-таки их возможности еще не раскрыты в полной мере. Поэтому, создание новых, изучение уже открытых свойств растений, содержащих фенольные гликозиды, может занять достойное место в будущих научно- исследовательских работах.
Конечно, я не склонен противопоставлять травы и фармакологические препараты для решения проблем здоровья. Но я считаю, что даже самая совершенная фармакологическая терапия является необходимым, но недостаточным условием восстановления здоровья человека. Ведь лекарственные травы способны не только воздействовать на очаг патологии, но и существенно повышать защитные силы организма. Прием трав основан на древнем и важнейшем, но, к сожалению, забытом, постулате медицины - лечить не болезнь, а больного.
3. При написании данной курсовой работы, изучая материал, я пришел к выводу, что растения, содержащие фенольные гликозиды, представляют особый интерес в плане профилактики и лечения заболеваний, сопровождающиеся ослаблением антиоксидантной защиты организма, повышением противоопухолевой резистентности, препятствованию развития метастазов [3]. Особенно желательно их применение на экологически неблагоприятных территориях, к которым относится Беларусь. Мы живем в век стрессов, загрязнения окружающей среды, химизации, искусственной ароматизации продуктов и многих других неблагоприятных факторов. Статистические исследования последних лет показывают, что наблюдается значительный рост онкологических заболеваний.
Родиола розовая, красная щетка - известные и почитаемые многими веками растения, обладают редкой способностью восстанавливать равновесие организма, стимулируя или замедляя определенные биологические процессы, нарушенные вследствие воздействия различных факторов. Ведь, используя опыт народной медицины, совершенно очевидно, что препараты из этих растений представляют собой крайне эффективное природное средство, помогающее приспособиться к неблагоприятным внешним факторам [3, 6].
К сожалению, ни один из видов лекарственных растений с адаптогенной активностью не произрастает дико на территории РБ, поэтому актуальной задачей является поиск отечественных заменителей этих растений. Наиболее перспективным является ива прутьевидная, из числа произрастающих ив в РБ, для создания препаратов с адаптогенным действием (содержание группы фенолгликозидов- 2.49%) [18].
Так же, я думаю, что можно пробовать выращивание родиолы розовой в культуре. Установлено, что в культуре процентное содержание действующих веществ у родиолы снижается, но увеличивается масса корневищ, число закладываемых на корневищах почек возобновления, количество семян [6].
Так что общая биологическая продуктивность родиолы в культуре компенсирует уменьшение процентного содержания действующих веществ.
4. Поиск новых перспективных видов ЛРС, содержащих фенолгликозиды является актуальной задачей современной науки, но это лишь первый шаг.
Следующий шаг должны сделать люди, которые начинают применять ЛРС. Они должны научиться правильно его применять, добиваясь максимальной эффективности. Но для того, чтобы научиться это делать, необходимо знать, как оно будет работать в тех или иных ситуациях. Для этого требуется проводить клинические исследования. Это задача непростая, но она вполне решаемая.
Во-первых, необходимо отслеживать результаты применения ЛРС, фиксируя как положительные, так и отрицательные результаты. Со временем появится информация к размышлению над полученными результатами. Во-вторых, нужно стараться анализировать результаты применения ЛРС, обращая внимание на симптомы или данные анализов, состояние организма до и после применения трав.
5. Необходимо разработать более эффективные методы качественного и количественного определения фенолгликозидов в ЛРС.
Например, анализируя различные методики количественного определения [1, 14, 15, 16, 17] можно придти к выводу, что наименьшую относительную ошибку даёт спектрофотометрический метод определения, который характеризуется точностью и простотой выполнения [14, 15]. Фотоэлектроколориметрический метод даёт большую относительную ошибку, например, в методике предусмотрено применение реосаждения сопутствующих полифенольных соединений, что приводит к соосаждению и арбутина [14]. Йодометрический метод даёт завышенные результаты вследствие неспецифичности используемой реакции [14].
В связи с вышеизложенным, для количественного определения фенолгликозидов рекомендуется использовать спектрофотометрический метод. Но применяя данный метод, исследователи используют в основном токсичный хлороформ.
Перспективными для анализа я считаю, являются гибридные методы химического анализа (гибридные жидкохроматографические системы). Например, для качественного определения возможно применение очень точных методов: жидкостная хроматография-масс-спектрометрия (ЖХ-МС) или жидкостная хроматография - инфракрасное детектирование с фурье-преобразованием (ЖХ-ФПИК), которые сейчас используются в научных лабораториях различных стран мира [20].
Я надеюсь, что многообразный мир растений, преподнесет немало находок и открытий, которые послужат надежным инструментом в борьбе за здоровье человека.
Используемая литература
1. Кретович, В.Л. Биохимия растений/Л.В.Кретович. - М.: Высшая школа,1980.- 445с.
2. [электронный ресурс]. – Режим доступа: htpp://www.phytochemistry.narod.ru – Дата доступа: 23.02.2010
3.Балицкий, К.П. Лекарственные растения в терапии злокачественных опухолей/К.П. Балицкий, А.Л. Воронцова.-Ростов-на Дону: Изд-во Ростовского университета, 1980.- 295 с.
4. [электронный ресурс]. - Режим доступа: www. fito-medic.ru – Дата доступа: 11.03.2010
5. [электронный ресурс]. - Режим доступа: www.fitolekarstvo.ru - Дата доступа: 11.03.2010
6. Ишмуратова, М.М. О фармакологических и экологических свойствах видов рода Rhodiola, определяемых их химическим составом/М.М. Ишмуратова //Вестник Башкирского университета.-2001.- Т.2.- № 2.- С.74-76
7. Костина, В.М. Особенности фенольного метаболизма растений/В.М. Костина– М.: Институт физиологии растений им.К.А.Тимирязева РАН,2009. – 109 стр.
8. Запрометов, М.Н. Фенольные соединения. Распространение, метаболизм и функции в растениях/М.Н. Запрометов - М.: Наука,1993.- 272 стр.
9. Шмерко, Е.П. Лечение и профилактика растительными средствами/ Е.П. Шмерко, И.Ф.Мазан - Баку: Издательство «Азербайджан»,1992.-314 с.
10. [электронный ресурс].- Режим доступа: www. Herbarius.info-Дата доступа: 21.02.2010
11. Халецкий, А.М. Фармацевтическая химия/А.М. Халецкий- Л.: Медицина, 1966.-748 с.
12. Mabry, T.J The systematic identification of Flavonoids / T.J. Mabry, K.R. Markham, M.B. Thomas-New York etc. Springer – Verlag, 1970. - 354 p.
13. Бандюкова, В.А. Применение цветных реакций для обнаружения флавоноидов путем хроматографии на бумаге/В.А. Бандюкова // Растительные ресурсы.-1965.- Т. 1.- Вып. 4.- С. 591–597
14. Охрименко, Л.П., Калинкина Г.И., Дмитрук С.Е. Сравнительное исследование толокнянки, брусники и близких к ним видов, произрастающих в Республике Саха (Якутия)/ Л.П. Охрименко, Г.И. Калинкина, С.Е. Дмитрук // Химия растительного сырья.- 2005.- №1.- С. 31–36
15. Pearl, I.A., Darling S.F. Spectrometry as an aid for determining structures ol naturall glucosides/ I.A. Pearl, S.F. Darling// Phytochem.- 1989.- Vol. 7. - №5. - P. 831–836.
16. Государственная Фармакопея Республики Беларусь/ Центр экспертиз и испытания в здравоохранении// Под общ. ред. А.А. Шерякова - Молодечно: Типография “Победа”, 2006.-2009. - Т.2:Контроль качества вспомогательных веществ и лекарственного растительного сырья.-2008.-472 c.
17. European Pharmacopoeia: 5th Edition / Strasbourg.-2004.-5439 p.
18. Кулак, В.А. Содержание флавоноидов и фенолгликозидов в листьях белорусских видов ив/ В.А. Кулак, Н.А. Кузьмичева//Информационно- маркетинговый центр молодежной науки в Беларуси.- Режим доступа: htpp://www.metolit.by-Дата доступа: 21.02.2010
19. [электронный ресурс]. - Режим доступа www.bitra.ru - Дата доступа: 21.02.2010
20. Niessen, W.M. Liquid Cromatography - Mass Spectrometry/ W.M.Niessen, A. van der Greef-New York: Marcel Dekker, 1992. - 315 p.
| Развитие, становление и основные аспекты фармации | |
|
... Для ветеринарного провизора необходимы знания, с помощью которых можно контролировать качество лекарственных веществ, определять их подлинность, ... Окрашивающиеся соединения с хлоридом железа (III) образуют лекарственные вещества, содержащие в своей молекуле фенольный гидроксил: производные я-аминофенола, сложные эфиры ... Например, действуя окислителями, можно последовательно открывать бромиды и йодиды, раствором хлорида железа (III) - бензоаты и салицилаты и т. д. Можно подобрать реактив, который с ... |
Раздел: Рефераты по медицине Тип: книга |
| Технология лекарственных форм | |
|
Государственное образовательное учреждение Высшего профессионального образования "Самарский Государственный Медицинский Университет Кафедра ... Ее используют для изготовления растворов внутреннего и наружного применения, глазных капель, офтальмологических растворов, лекарственных форм для новорожденных и других ... В процессе жизнедеятельности в растениях синтезируются различные органические вещества, среди которых много физиологически активных соединений - гликозиды, алкалоиды, дубильные ... |
Раздел: Рефераты по медицине Тип: отчет по практике |
| Влияние регуляторов роста растений на физиолого-биохимические ... | |
|
Министерство сельского хозяйства РФ Федеральное государственное образовательное учреждение высшего профессионального образования Кубанский ... Под действием аскорбиновой кислоты раствор 2,6 - дихлорфенолиндофенола, имеющий синюю окраску, восстанавливается в бесцветное соединение. Для титрования из полученного фильтрата берут пипеткой в стакан 2 параллельные порции по 10 мл и титруют из микробюретки 0,001 н. раствором краски Тильманса до появления ясно ... |
Раздел: Рефераты по ботанике и сельскому хозяйству Тип: дипломная работа |
| Неотложная помощь в невропатологии | |
|
Неотложная помощь в невропатологии Часть первая НЕВРОЛОГИЧЕСКИЕ СИНДРОМЫ ГОЛОВНАЯ БОЛЬ Механизмы возникновения. Многие внутричерепные образования ... При острой артериальной гипотензии больному придают полусидячее или сидячее положение, вводят сердечные гликозиды по показаниям (0,25-0,5 мл 0,05% раствора строфантина или 0,5-1 мл ... Лечение выраженного гипертензивного криза целесообразно начинать с применения диуретических препаратов: фуросемида (лазикса) 2 мл 1% раствора внутримышечно, внутривенно 1 раз в ... |
Раздел: Рефераты по медицине Тип: книга |
| Общее содержание воды в листьях калины в условиях биостанции | |
|
Министерство образования Российской Федерации Мичуринский государственный педагогический институт кафедра биологии и основ сельского хозяйства ... С целью ознакомления кадетов в нем выращивали лекарственные и культурные растения, среди последних - большое количество овощных. Коноплю, тополь и иву называют двудомными растениями, так как у них тычиночные цветки расположены на одних растениях, а пестичные - на других. |
Раздел: Рефераты по биологии Тип: реферат |