Реферат: Методы определения ПАУ в объектах окружающей среды
Я. Бартулевич, Г. Ягов
Развитие химико-аналитической аппаратуры не только не снимает проблему качества выполняемых измерений, но, напротив, предъявляет все более высокие требования во всех аспектах проведения измерений. Это относится к процедурам отбора проб, пробоподготовки и, собственно постановки измерений. Особенно это касается выполнения анализов сильно токсичных соединений таких как, например, полиядерные ароматические углеводороды (ПАУ). Многолетние токсикологические исследования позволили обозначить соединения группы ПАУ, которые необходимо постоянно контролировать в окружающей среде, как с точки зрения их собственной токсичности, так и с точки зрения наиболее вероятного поступления в окружающую среду. агентство по охране окружающей среды США (ЕРА US) рекомендует контролировать 16 соединений из группы ПАУ в пробах окружающей среды. нормы, разрабатываемые в рамках ISO и EC, предполагают дополнительное расширение перечня определяемых соединений. Следует отметить, что в России в настоящее время нормируется только одно соединение, относящееся к этому классу - бенз/а/пирен. Очевидно, что со временем перечень контролируемых соединений будет расширяться, поэтому важно заранее проанализировать все возможности, предоставляемые современной аппаратурой, с тем, чтобы правильно подойти к проблеме выбора метода анализа и соответствующего прибора.
Как правило для определения ПАУ используются методы газовой хроматографии (ГХ) и высокоэффективной жидкостной хроматографии (ВЭЖХ). разделение основных 16 ПАУ, достаточное для количественного анализа, достигается применением либо капиллярных колонок в газовой хроматографии, либо высокоэффективных колонок применяемых в ВЭЖХ. Необходимо помнить, что колонка, хорошо разделяющая калибровочные смеси шестнадцати ПАУ не гарантирует, что они также хорошо будут разделяться на фоне сопутствующих органических соединений в исследуемых пробах.
В целях упрощения анализа, а также для достижения высокого качества получаемых результатов, большинство аналитических процедур содержит этап предварительного выделения (сепарации) ПАУ среди иных групп сопутствующих соединений в пробах. Чаще всего в этих целях используются методы жидкостной хроматографии низкого давления в системе жидкость-твердое тело или жидкость-жидкость с использованием механизмов адсорбции, например с использованием силикагеля или окиси алюминия, иногда используются смешанные механизмы, например адсорбции и исключения с применением cефадексов.
Использование предварительной очистки проб позволяет при определении ПАУ избежать влияния:
полностью неполярных соединений, таких, как алифатические углеводороды;
умеренно и сильно полярных соединений, например, фталанов, фенолов, многоатомных спиртов, кислот;
высокомолекулярных соединений таких, как, например, смолы.
В полученных очищенных экстрактах могут содержаться алкилпроизводные ПАУ, бифенилы, ароматические производные дибензодиоксана и дибензофурана, а также много иных соединений. В связи с тем, что разделительный потенциал колонок, используемых в ВЭЖХ и капиллярных колонок, используемых в газовой хроматографии, ограничен, достоверность идентификации соединений может быть дополнительно повышена за счет использования высокоселективных детекторов. Детекторы также должны обеспечивать определение анализируемых соединений с достаточной чувствительностью.
При использовании метода газовой хроматографии в качестве детектора чаще всего используется пламенно-ионизационный детектор (ПИД) или масс-спектрометр (МС). Пламенно-ионизационный детектор является неселективным детектором и может служить только для количественных измерений после идентификации соединения другим, независимым методом. Масс-спектрометр, сопряженный с газовым хроматографом, дает качественную информацию (масс-спектр) для исследуемой субстанции. Однако в большом количестве случаев специфичность этой информации ограничена вследствие совпадения масс некоторых соединений, различающихся строением и токсичностью.
В высокоэффективной жидкостной хроматографии (ВЭЖХ) используются главным образом два типа детекторов: флуориметрический детектор или спектрофотометрический детектор с фотодиодной линейкой. Предел обнаружения ПАУ при флуориметрическом детектировании очень низкий, что делает этот метод особенно пригодным для определения следовых количеств полиароматических соединений. Однако классические флуориметрические детекторы практически не дают информации о строении исследуемого соединения. Современные конструкции делают возможным регистрацию спектров флуоресценции, которые характеристичны для индивидуальных соединений, но они пока не получили широкого распространения в практике рутинных измерений. Спектрофотометрический детектор с фотодиодной линейкой (ФДЛ) дает возможность регистрации спектров поглощения в УФ- и видимом спектральном диапазоне, эти спектры могут использоваться для идентификации. Аналогичная информация может быть получена с использованием быстросканирующих детекторов.
При выборе аналитической техники, предназначенной для разделения, идентификации и количественного анализа упомянутых ПАУ необходимо учитывать следующие условия:
уровень определяемых содержаний в исследуемых пробах;
количество сопутствующих субстанций;
применяемая аналитическая процедура (методика выполнения измерений);
возможности серийной аппаратуры.
В таблице представлены основные характеристики систем, предназначенных для анализа ПАУ:
Характеристики систем ГХ-МС, ГХ-ПИД, ВЭЖХ-флу и ВЭЖХ-ФДЛ, используемых при анализе ПАУ
| характеристика | ГХ-МС | ГХ-ПИД | ВЭЖХ-флу | ВЭЖХ-ФДЛ |
|
разрешение (теор. тарелки) |
100...200 тыс. | 100...200 тыс. | 10...20 тыс. | 10...20 тыс. |
| количество вещества, необходимое для регистрации спектра | --- | 0,1...1,0 нг | 0,01...1,0 нг | 0,1...1,0 нг |
| идентификация изомеров ПАУ | нет | плохая | ? | хорошая или средняя |
| идентификация алкилпроизводных ПАУ | нет | средняя или плохая | нет данных | средняя или плохая |
| концентрация вещества в пробе | 100...1000 нг/мл | 100...1000 нг/мл | 0,05...1,0 нг/мл | 5...50 нг/мл |
| степень концентри-рования, необходимая для определения 1 ppt в пробе | 100...1000 тыс. | 100...1000 тыс. | 50...1000 | 5...50 тыс. |
| смена элюента | не применяется | не применяется | применяется | применяется |
| разложение пробы при анализе | возможно | возможно | маловероятно | маловероятно |
|
возможность анализа изотопного |
нет | да | нет | нет |
| стоимость текущей эксплуатации | низкая | средняя | высокая | высокая |
С точки зрения разделительного потенциала наиболее выгодно использование метода капиллярной газовой хроматографии. Количество соединений, которое теоретически может быть разделено в единицу времени в капиллярной газовой хроматографии в 5, а может быть и в 10 раз больше, чем с использованием ВЭЖХ. Это не означает однозначного преимущества анализа методом ГХ над ВЭЖХ так, например, разделение таких пар соединений как бензо/б/флуорантрен-бензо/к/флуорантрен, а также (1.2.3-с.д)пирен-дибензо(а,х)антрацен легче осуществляются методом ВЭЖХ, нежели капиллярной ГХ.
Количество вещества, вводимого в детектор МС или ФДЛ и дающее возможность получения спектров, должно быть как правило, в 5...10 раз выше уровня обнаружения детектора. Спектры получаемые для проб природных объектов могут быть дополнительно деформированы в зависимости от количества и состава сопутствующих субстанций.
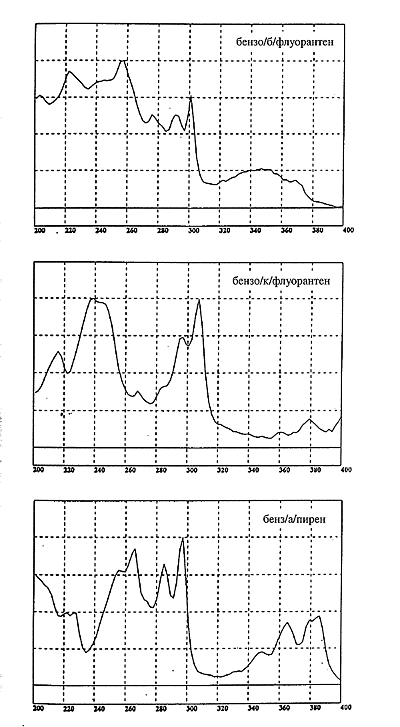
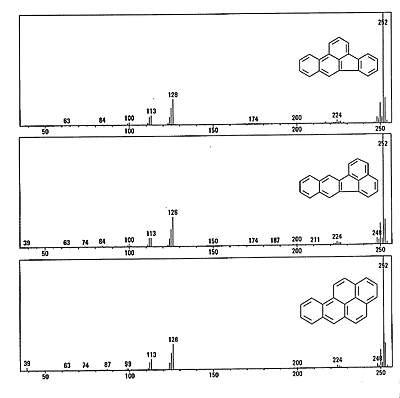
Масс-спектры ПАУ с данной массой молекулы мало характеристичны. На рис. 1 [1], представлены масс-спектры трех соединений с массой молекулы 252: бензо/б/флуорантена, бензо/к/флуорантена, а также бензо/а/пирена. Спектры практически идентичны несмотря на то, что соединения принципиально отличаются строением. Идентификация отдельных ПАУ в технике ГХ-МС требует соответствия масс-спектра и времени выхода. Попытка однозначной идентификации соединений, опирающаяся только на масс-спектры, может оказаться ошибочной. В то же время оптические спектры поглощения представленных соединений имеют существенные различия. По-видимому "незначительная" разница в расположении одного кольца наблюдаемая между бензо/б/флуорантеном и бензо/к/флуорантеном сильно влияет на вид спектра поглощения (рис. 2 [1]).
 Предел
обнаружения того или иного соединения в растворе зависит от объема пробы,
который может быть введен в систему. В случае стандартных систем ГХ-МС с
дозаторами типа сплит-сплитнесс, объем вводимой пробы не превышает 1...2 мкл.,
в то время как для систем ВЭЖХ количество вводимой пробы составляет от 10 до 20
мкл - отсюда становится понятной разница определительной способности в
растворе, а также в степени концентрирования необходимого для определения,
например, минимального количества на уровне 1 ppt. Уровень обнаружения системы
ГХ-МС может быть повышен за счет управления величиной вводимой пробы при
использовании дозаторов делающих возможным ввод пробы с объемом в несколько
десятков микролитров например, дозаторов типа PTV.
Предел
обнаружения того или иного соединения в растворе зависит от объема пробы,
который может быть введен в систему. В случае стандартных систем ГХ-МС с
дозаторами типа сплит-сплитнесс, объем вводимой пробы не превышает 1...2 мкл.,
в то время как для систем ВЭЖХ количество вводимой пробы составляет от 10 до 20
мкл - отсюда становится понятной разница определительной способности в
растворе, а также в степени концентрирования необходимого для определения,
например, минимального количества на уровне 1 ppt. Уровень обнаружения системы
ГХ-МС может быть повышен за счет управления величиной вводимой пробы при
использовании дозаторов делающих возможным ввод пробы с объемом в несколько
десятков микролитров например, дозаторов типа PTV.
Неочищенные экстракты ПАУ из природных проб и фракции, содержащие ПАУ после очистки методом колоночной жидкостной хроматографии, как правило, растворяются в известном количестве полярных растворителей например, в метиленхлориде. При использовании техники ВЭЖХ с обращенной фазой, когда проба вводится в полярном растворителе (метанол, ацетонитрил, THF) как правило, конечной является так называемая операция смены растворителя, которая может быть основным источником ошибки. Этих проблем нет в случае газовой хроматографии.
Полициклические ароматические соединения являются термически неустойчивыми соединениями и результат их разделения в системах ГХ не всегда адекватен исходному состоянию. В исследованных пробах могут сопутствовать как соединения термически лабильные, так и термически разлагающиеся при повышенной температуре. В случае разложения, протекающего в дозаторе и колонке, могут возникать иные соединения, регистрирующиеся в анализах. В крайних случаях дело может доходить до полного искажения хроматограммы. Эта проблема является главной в газовой хроматографии, где температура дозатора и колонки доходит до 300-350 оС.
Последовательные этапы анализа, а именно экстракция, очистка, концентрирование проб сопровождаются ошибками, влияющими на конечный результат количественных определений. Особенно важный этап - экстракция аналита из матрицы. Изменчивость состава почв, аэрозолей или осадков затрудняет установление однозначных условий экстракции ПАУ этого типа проб и установление однозначного выхода экстракции. Контроль этапа экстракции и других аналитических этапов проводится методом добавок внутреннего стандарта. внутренним стандартом может быть определяемая субстанция либо иная с подобными свойствами.
В случае добавки известного количества определяемой субстанции появляется проблема идентичности отбора и определения нескольких проб при одновременной обработке, состоящая в том, что состав одинаково отобранных и обработанных проб будет адекватен. Во многих случаях выполнение этого постулата невозможно.
Дополнение в качестве эталонной субстанции иной, нежели определяемая требует, чтобы в пробе не присутствовали вещества с тем же временем выхода, что и внутренний стандарт. Для проб сложного состава, как например, почва, сточные воды, промвыбросы выполнение этого условия может быть затруднено, исключая добавки с использованием изотопных образцов. Для однозначного определения изотопного состава добавленного образца желательно одновременное использование масс-спектрометрии.
Все представленные выше методы имеют свои достоинства и недостатки, которые надлежит досконально обдумать перед принятием решения, например о приобретении данной системы, и применении ее для определенного круга исследований.
Принимая во внимание возможности разделения, однозначность качественного анализа, возможность контроля аналитического процесса через соотношение внешнего изотопного спектра, оптимальной техникой для исследования ПАУ будет капиллярная газовая хроматография, сопряженная с масс-спектрометром.
ВЭЖХ с детектором, регистрирующим спектры в УФ и видимой части спектра делает возможным идентификацию исследуемого соединения. Однако вообще-то возможности разделения и идентификации этой аппаратуры значительно ниже, чем у ГХ-МС.
Идентификация ПАУ, основанная только на совпадении времени выхода может быть ошибочной. Таким образом, использование даже очень селективного флуориметрического детектора может приводить к получению неоднозначных результатов.
Использование техники ГХ-ПИД может допускаться только для количественного анализа проб с хорошо известным составом (предварительно установленным при помощи других методов анализа). В сомнительных случаях результаты анализов (ГХ-ПИД) могут быть сравнительно легко оспорены.
Список литературы
1. Bartulewicz J., Bartulewicz E., Gawłowski J. "GC-MS i HPLC z detektorem diodowym w analizie wielopierścieniowych węglowodorów aromatycznych w próbkach środowiskowych". Biblioteka Monitoringu Środowiska, Warszawa, 1997.
 состава
состава