Реферат: Апоптоз
Содержание
Апоптоз. 2
Морфологические проявления апоптоза. 2
Сжатие клетки. 4
Конденсация хроматина. 5
Формирование в цитоплазме полостей и апоптотических телец. 5
Механизм апоптоза. 7
Регуляция апоптоза. 10
Автономный механизм апоптоза. 12
Снижение апоптоза. 14
Ускорение апоптоза. 15
Значение апоптоза в развитии организма и патологических процессах. 15
Апоптоз
Источник информации:
В организме здорового человека клеточный гомеостаз определяется балансом между гибелью и пролиферацией клеток. Апоптоз - программированная клеточная гибель, энергетически зависимый, генетически контролируемый процесс, который запускается специфическими сигналами и избавляет организм от ослабленных, ненужных или повреждённых клеток. Ежедневно, примерно около 5% клеток организма подвергаются апоптозу, а их место занимают новые клетки. В процессе апоптоза клетка исчезает бесследно в течение 15-120 минут.
Апоптоз - это биохимически специфический тип гибели клетки, который характеризуется активацией нелизосомных эндогенных эндонуклеаз, которые расщепляют ядерную ДНК на маленькие фрагменты. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток, пример - опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример - атрофия.
Морфологические проявления апоптоза
Апоптоз имеет свои отличительные морфологические признаки, как на светооптическом, так и на ультраструктурном уровне. При окраске гематоксилином и эозином апоптоз определяется в единичных клетках или небольших группах клеток. Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз - в отличие от некроза - никогда не сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление.
Таблица 1. Сравнительная характеристика некроза и апоптоза
|
Апоптоз - это механизм гибели клеток, который имеет ряд биохимических и морфологических отличий от некроза.
Наиболее четко морфологические признаки выявляются при электронной микроскопии. Для клетки, подвергающейся апоптозу характерно (рис.1):
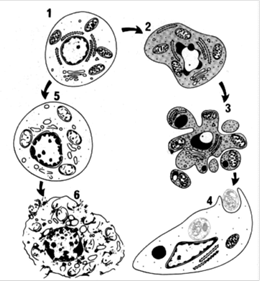
Рис.1. Последовательность ультраструктурных изменений при апоптозе (справа) и некрозе (слева): 1 - нормальная клетка; 2 - начало апоптоза; 3 - фрагментация апоптотической клетки; 4 - фагоцитоз апоптотических телец окружающими клетками; 5 - гибель внутриклеточных структур при некрозе; 6 - разрушение клеточной мембраны.
Сжатие клетки
Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, которые выглядят относительно нормальными, располагаются более компактно.
Предполагается, что нарушение формы и объема клетки происходит в результате активации в апоптотических клетках трансглютаминазы. Этот фермент вызывает прогрессивное образование перекрестных связей в цитоплазматических белках, что приводит к формированию своеобразной оболочки под клеточной мембраной, подобно ороговевающим клеткам эпителия.
Конденсация хроматина
Это наиболее характерное проявление апоптоза. Хроматин конденсируется по периферии, под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро же может разрываться на два или несколько фрагментов.
Механизм конденсации хроматина изучен достаточно хорошо. Он обусловлен расщеплением ядерной ДНК в местах, связывающих отдельные нуклеосомы, что приводит к развитию большого количества фрагментов, в которых число пар оснований делится на 180-200. При электрофорезе фрагменты дают характерную картину лестницы. Эта картина отличается от таковой при некрозе клеток, где длина фрагментов ДНК варьирует. Фрагментация ДНК в нуклеосомах происходит под действием кальций чувствительной эндонуклеазы. Эндонуклеаза в некоторых клетках находится постоянно (например, в тимоцитах), где она активируется появлением в цитоплазме свободного кальция, а в других клетках синтезируется перед началом апоптоза. Однако еще не установлено, каким образом после расщепления ДНК эндонуклеазой происходит конденсация хроматина.
Формирование в цитоплазме полостей и апоптотических телец
В апоптотической клетке первоначально формируются глубокие впячивания поверхности с образованием полостей, что приводит к фрагментации клетки и формированию окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с или без фрагментов ядра.
Фагоцитоз апоптотических клеток или телец
Фагоцитоз апоптотических клеток или телец осуществляется окружающими здоровыми клетками, или паренхиматозными, или макрофагами. Апоптотические тельца быстро разрушаются в лизосомах, а окружающие клетки либо мигрируют, либо делятся, чтобы заполнить освободившееся после гибели клетки пространство.
Фагоцитоз апоптотических телец макрофагами или другими клетками активируется рецепторами на этих клетках: они захватывают и поглощают апоптотические клетки. Один из таких рецепторов на макрофагах - рецептор витронектина, который является β3-интегрином и активирует фагоцитоз апоптотических нейтрофилов.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез). Несмотря на то, что при эмбриогенезе апоптоз не всегда является отражением “запрограммированной смерти клетки”, это определение апоптоза широко используют различные исследователи.
Гормон-зависимой инволюции органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации.
Удалении некоторых клеток при пролиферации клеточной популяции.
Гибели отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли.
Гибели клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибели аутореактивных Т-клеток при развитии в тимусе.
Патологической атрофии гормон-зависимых органов, например, атрофии предстательной железы после кастрации и истощении лимфоцитов в тимусе при терапии глюкокортикоидами.
Патологической атрофии паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках.
Гибели клеток, вызванных действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”.
Повреждении клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени, как тельца Каунсильмана.
Гибели клеток при действии различных повреждающих факторов, которые способны вызвать некроз, но действующих в небольших дозах, например, при действии высокой температуры, ионизирующего излучения, противоопухолевых препаратов.
Механизм апоптоза
TNF-α и Fas-лиганд (CD178) запускают каскад биохимических реакций, финальным этапом которых является дефрагментация хромосом и гибель клетки. На поверхности клеток организма имеются специальные рецепторы для TNF-α, это TNF-RI (с молекулярной массой 55-60 кДа) и TNF-RII (с молекулярной массой 75-80 кДа), а для Fas-лиганда рецептор Fas / APO-1 (CD95).
TNF-R и Fas / APO-1(CD95) имеют гомологию в экстрацеллюлярных доменах, представленную в виде цистеин богатых доменов и гомологичную последовательность в интрацеллюлярной части рецептора.
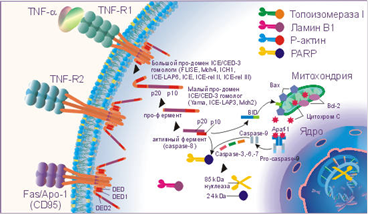
Рис.2. Апоптоз
Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные "домены смерти" (DED - death effector domain) этих рецепторов: DED, DED1 и DED2 и ряд посредников, включая церамиды, ras, SAPK / JNK, протеиновые тирозинкиназы, катепсин D и протеазы ICE / CED-3 семейства, которые каскадно проводят смертельный сигнал. Цистеиновые протеазы ICE / CED-3 семейства находятся в составе интрацеллюлярной части рецептора апоптоза в неактивной форме, они относятся к интерлейкин-lβ расщепляющим ферментам (ICE). Это семейство включает ряд различных типов протеаз, многие протеазы имеют несколько обозначений. Семейство цистеин-аспартат протеаз ещё называют каспазами.
Кроме семейства каспаз, в регуляции апоптоза принимает участие семейство Bcl-2 белков, в котором Bcl-2, Bcl-XL, Ced-9, Bcl-w, и Mcl-1 белки ингибируют апоптоз, а Bcl-2 гомологи (BH) 1-3, Bax подобный белок, Bak, Bok, и состоящие только из BH3 региона, Bad подобный белок, Bid, Bik, Bim, и Hrk выполняют проапоптозную функцию.
Активация DED, DED1 и DED2 вызывает каскадную перестройку и активацию протеаз ICE / CED-3 семейства. Первым этапом является превращение не активной про-каспазы-8 в активную каспазу-8. Каспаза-8 активирует каспазу-3 и Bid. Bid взаимодействуя с Bax способствует выходу из митохондрий цитохрома C, который активизирует каспазу-9. В свою очередь активная каспаза-9 приводит к появлению активных каспаз-3, - 6, - 7. В свою очередь активные ICE начинают взаимодействовать с рядом внутриклеточных субстратов: поли-(АДФ-рибозо) полимеразой (PARP), участвующей в репарации ДНК и модификации активности некоторых ядерных белков, ламином В1, топоизомеразой I и Р-актином. Все члены семейства ICE / CED-3 протеаз содержат каталитический остаток цистеина и расщепляют субстраты после аспарагиновой кислоты. Специфическое расщепление PARP, ламина В1, топоизомеразы I и Р-актина под действием ICE-подобных протеаз на большие и малые фрагменты приводит клетку к гибели, так как большие фрагменты этих субстратов и являются активными нуклеазами, которые разрезают хромосомы на фрагменты. Например, PARP расщепляется CPP32 / Yama на два фрагмента 85 и 24 кДа, из которых апоптоз-специфическим является фрагмент 85 кДа. Активация протеаз ICE / CED-3 семейства может происходить и под действием фосфолипидов, например, церамидов, которые способны активировать CPP32 / Yama.
Свободный сфингозин образуемый из церамидов в результате его гидролиза церамидазой так же активирует ICE-подобные протеазы и ускоряет апоптоз.
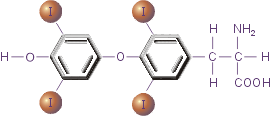
Рис.3. Тироксин
Важная роль в осуществлении апоптоза принадлежит тироксину (Т4).
Он регулирует функционирование протеиновой тирозинкиназы, важного элемента реализации сигнала смерти. При недостатке этого гормона щитовидной железы происходит подавление апоптоза.
IL-lβ блокирует апоптоз. ICE-подобные протеазы взаимодействуют с IL-lβ, а не с PARP, ламином В1, топоизомеразой I и Р-актином. В результате чего не происходит образования активных нуклеаз, и клетка избегает апоптоза.
На взаимодействие TNF-α и Fas-лигандов с TNF-R и Fas / APO-1(CD95) и проведение апоптотического сигнала оказывают влияние Bcl и Bax белки. Так белки Bcl семейства: Bcl-2, Bcl-xL и Bcl-xS блокируют выход цитохрома С из митохондрий и таким образом предотвращают превращение про-каспазы-9 в активную форму, отменяют атоптотический сигнал. В свою очередь Bax белки способствуют выходу цитохрома С из митохондрий и образованию активной каспазы-9, которая инициирует продолжение и активацию апоптотическог каскада, начавшегося с присоединения TNF-α или Fas-лигандов к TNF-R и Fas / APO-1(CD95). Быть или не быть апоптозу зависит от соотношения Bcl и Bax белков в митохондриях. Преобладание экспрессии белков Bcl семейства блокирует запуск апоптоза, а преобладание экспрессии Bax белков способствует реализации сигнала смерти.
Регуляция апоптоза
Апоптоз - это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза. Многие из этих генов сохранились в ходе эволюции - от круглых червей до насекомых и млекопитающих. Некоторые из них обнаруживаются также в геноме вирусов. Таким образом, основные биохимические процессы апоптоза в разных экспериментальных системах (исследования ведутся на круглых червях и мухах) являются идентичными, поэтому результаты исследований можно прямо переносить на другие системы (например, организм человека).
Апоптоз может регулироваться:
внешними факторами,
автономными механизмами.
Воздействие внешних факторов
Апоптоз может регулироваться действием многих внешних факторов, которые ведут к повреждению ДНК. При невосстановимом повреждении ДНК путем апоптоза происходит элиминация потенциально опасных для организма клеток. В данном процессе большую роль играет ген супрессии опухолей р53. К активации апоптоза также приводят вирусные инфекции, нарушение регуляции клеточного роста, повреждение клетки и потеря контакта с окружающими или основным веществом ткани. Апоптоз - это защита организма от персистенции поврежденных клеток, которые могут оказаться потенциально опасными для многоклеточного организма.
При стимуляции тканей каким-либо митогеном ее клетки переходят в состояние повышенной митотической активности, которая обязательно сопровождается некоторой активацией апоптоза. Судьба дочерних клеток (выживут они или подвергнутся апоптозу) зависит от соотношения активаторов и ингибиторов апоптоза:
ингибиторы включают факторы роста, клеточный матрикс, половые стероиды, некоторые вирусные белки;
активаторы включают недостаток факторов роста, потерю связи с матриксом, глюкокортикоиды, некоторые вирусы, свободные радикалы, ионизирующую радиацию.
При воздействии активаторов или отсутствии ингибиторов происходит активация эндогенных протеаз и эндонуклеаз. Это приводит к разрушению цитоскелета, фрагментации ДНК и нарушению функционирования митохондрий. Клетка сморщивается, но клеточная мембрана остается интактной, однако повреждение ее приводит к активации фагоцитоза. Погибшие клетки распадаются на небольшие, окруженные мембраной, фрагменты, которые обозначаются как апоптотические тельца. Воспалительная реакция на апоптотические клетки не возникает.
Автономный механизм апоптоза
При развитии эмбриона различают три категории автономного апоптоза: морфогенетический, гистогенетический и филогенетический.
Морфогенетический апоптоз участвует в разрушении различных тканевых зачатков. Примерами являются:
разрушение клеток в межпальцевых промежутках;
гибель клеток приводит к разрушению избыточного эпителия при слиянии небных отростков, когда формируется твердое небо.
гибель клеток в дорсальной части нервной трубки во время смыкания, что необходимо для достижения единства эпителия двух сторон нервной трубки и связанной с ними мезодермы.
Гистогенетический апоптоз наблюдается при дифференцировке тканей и органов, что наблюдается, например, при гормональнозависимой дифференцировке половых органов из тканевых зачатков. Так, у мужчин клетками Сертоли в яичках плода синтезируется гормон, который вызывает регрессию протоков Мюллера (из которых у женщин формируются маточные трубы, матка и верхняя часть влагалища) путем апоптоза.
Филогенетический апоптоз участвует в удалении рудиментарных структур у эмбриона, например, пронефроса.
При различных состояниях может наблюдаться как ускорение, так и замедление апоптоза. Несмотря на то, что апоптоз могут активировать различные факторы, характерные для определенных типов клеток, однако конечный путь апоптоза регулируется точно установленными генами и является общим, независимо от причины активации апоптоза.
Все факторы, усиливающие или ослабляющие апоптоз, могут действовать прямо на механизм гибели клетки или опосредованно, путем влияния на регуляцию транскрипции.
В некоторых случаях влияние этих факторов на апоптоз является решающим (например, при глюкокортикоид-зависимом апоптозе тимоцитов), а в других не имеет особой важности (например, при Fas - и TNF-зависимом апоптозе). В процессе регуляции принимает участие большое количество веществ. Наиболее изученными из них являются вещества из семейства bcl-2.
Bcl-2 ген впервые был описан как ген, который транслоцируется в клетках фолликулярной лимфомы и ингибирует апоптоз. При дальнейших исследованиях оказалось, что Bcl-2 является мультигеном, который обнаруживается даже у круглых червей. Гомологичные гены были также обнаружены в некоторых вирусах. Все вещества, относящиеся к данному классу делятся на активаторы и ингибиторы апоптоза.
К ингибиторам относятся: bcl-2, bcl-xL, Mcl-1, bcl-w, аденовирусный E1B 19K, Эпштейн-Барр-вирусный BHRF1.
К активаторам относятся bax, bak, Nbk / Bik1, Bad, bcl-xS.
Члены этого семейства взаимодействуют друг с другом. Одним из уровней регуляции апоптоза является взаимодействие белок-белок. Белки семейства bcl-2 формируют как гомо - так и гетеродимеры. Например, bcl-2-ингибиторы могут образовать димеры bcl-2-активаторами. Таким образом, жизнеспособность клеток зависит от соотношения активаторов и ингибиторов апоптоза. Например, bcl-2 взаимодействует с bax; при преобладании первого жизнеспособность клетки повышается, при избытке второго - уменьшается. К тому же белки семейства bcl-2 могут взаимодействовать с белками, не относящимися к этой системе. Например, bcl-2 может соединятся с R-ras, который активирует апоптоз. Другой белок, Bag-1, усиливает способность bcl-2 ингибировать апоптоз.
В настоящее время принято считать, что гены, участвующие в регуляции роста и развития опухолей (онкогены и гены-супрессоры опухолей), играют регулирующую роль в индукции апоптоза. К ним относятся:
bcl-2 онкоген, который ингибирует апоптоз, вызванный гормонами и цитокинами, что приводит к повышению жизнеспособности клетки;
Белок bax (также из семейства bcl-2) формирует димеры bax-bax, которые усиливают действие активаторов апоптоза. Отношение bcl-2 и bax определяет чувствительность клеток к апоптотическим факторам и является “молекулярным переключателем”, который определяет, будет ли происходить рост или атрофия ткани.
c-myc онкоген, чей белковый продукт может стимулировать либо апоптоз, либо рост клеток (при наличии других сигналов выживания, например, bcl-2)
Ген р53, который в норме активирует апоптоз, но при мутации или отсутствии (что обнаружено в некоторых опухолях) повышает выживаемость клеток. Установлено, что р53 необходим для апоптоза при повреждении клетки ионизирующим излучением, однако при апоптозе, вызванном глюкокортикоидами и при старении, он не требуется.
Снижение апоптоза
Продукт р53 гена следит за целостностью генома при митозе. При нарушении целостности генома клетка переключается на апоптоз. Наоборот, белок bcl-2 ингибирует апоптоз. Таким образом, недостаток р53 или избыток bcl-2 приводит к накоплению клеток: эти нарушения наблюдаются в различных опухолях. Изучение факторов регулирующих апоптоз имеет важное значение в разработке лекарственных препаратов, усиливающих гибель клеток злокачественных новообразований.
Аутоиммунные заболевания могут отражать нарушения в индукции апоптоза лимфоидных клеток, способных реагировать с собственными антигенами. Например, при системной красной волчанке наблюдается нарушение Fas-рецепторов на клеточной поверхности лимфоцитов, что ведет к активации апоптоза. Некоторые вирусы повышают свою выживаемость путем ингибирования апоптоза инфицированных клеток, например, вирус Эпштейна-Барра может воздействовать на обмен bcl-2.
Ускорение апоптоза
Ускорение апоптоза доказано при синдроме приобретенного иммунодефицита (СПИД), нейротрофических заболеваниях и некоторых заболеваниях крови, при которых наблюдается дефицит каких-либо форменных элементов. При СПИДе вирус иммунодефицита может активировать CD4 рецептор на неинфицированных Т-лимфоцитах, ускоряя, таким образом, апоптоз, что приводит к истощению клеток данного типа.
Значение апоптоза в развитии организма и патологических процессах
Апоптоз играет важную роль в развитии млекопитающих и в различных патологических процессах. Функционирование bcl-2 требуется для поддержания жизнеспособности лимфоцитов, меланоцитов, эпителия кишечника и клеток почек во время развития эмбриона. bcl-x необходим для ингибирования смерти клеток в эмбриогенезе, особенно в нервной системе. Bax необходим для апоптоза тимоцитов и поддержания жизнеспособности сперматозоидов во время их развития. р53 является геном супрессии опухолей, поэтому в эмбриогенезе особой роли не играет, но обязательно необходим для супрессии опухолевого роста. Мыши, у которых отсутствовали оба р53 гена, проявляли чрезвычайно высокую склонность к развитию злокачественных опухолей в результате полного или частичного нарушения апоптоза предопухолевых клеток. Усиленный синтез белка, кодируемого bcl-2 геном, приводит к подавлению апоптоза и, соответственно, развитию опухолей; данный феномен обнаружен в клетках В-клеточной фолликулярной лимфомы.
При лимфопролиферативных заболеваниях и похожей на системную красную волчанку болезни у мышей наблюдается нарушение функции Fas-лиганда или Fas-рецептора. Повышенный синтез Fas-лиганда может предупреждать отторжение трансплантата. Апоптоз является частью патологического процесса при инфицировании клетки аденовирусами, бакуловирусами, ВИЧ и вирусами гриппа. Ингибирование апоптоза наблюдается при персистировании инфекции, в латентном периоде, а при усиленной репликации аденовирусов, бакуловирусов, возможно герпесвирусов, вируса Эпштейн-Барра и ВИЧ наблюдается активация апоптоза, что способствует широкому распространению вируса. При нейродистрофических заболеваниях отмечается нарушение функции гена (iap-гена), сходного с ингибитором апоптоза бакуловирусов.
| Программируемая клеточная смерть | |
|
Кратко рассмотрены сведения о программируемой клеточной смерти (апоптозе) у животных и растений. Патологический вариант клеточной гибели - некроз ... Применительно к клеткам животных и человека апоптоз в большинстве случаев связан с протеолитической активацией каскада каспаз - семейства эволюционно консервативных цистеиновых ... В некоторых случаях зависимый от рецепторов путь ведет к малоэффективной активации прокаспазы-8. В этом случае подключается зависимый от митохондрий путь апоптоза: каспаза-8 ... |
Раздел: Рефераты по науке и технике Тип: реферат |
| Апоптоз как регулятор иммунной системы | |
|
Реферат на тему: "Апоптоз, как регулятор иммунной системы" Введение Апоптоз - уникальный механизм сигналиндуцированной запрограммированной гибели ... Белок Bcl-2 тоже образовывает димеры, но он может соединяться с белком Вах, образуя гетеродимер Вах/Bcl-2, и апоптоз задерживается, т.е. увеличение содержания белка Вах ... Гены семейства Bcl-2 контролируются геном р53, но эффект последнего неоднозначен, он может стимулировать и пролиферацию, и апоптоз, поэтому исход зависит от особенности программы ... |
Раздел: Рефераты по медицине Тип: реферат |
| Одноклеточные альтруисты | |
|
А.В.Гордеева, Ю.А.Лабас Альтруизм (от лат. аlter - другой) - нравственный принцип, заключающийся в бескорыстном служении другим людям, в готовности ... В запуске апоптоза, вызванного повреждениями ДНК, активацией онкогенов и гипоксией, принимает участие белок-53 (р53), взаимодействуя с Вах, стимулируя "рецепторы смерти" и ... У дрожжей найдены практически все орудия суицида, имеющиеся у многоклеточных, кроме лизосомальных катепсинов и представителей семейства Bcl-2. Тем не менее, гены проапоптозных ... |
Раздел: Рефераты по биологии Тип: реферат |
| Цели регенеративной медицины. Терапия стволовыми клетками | |
|
Содержание 1. Терапия стволовыми клетками 2. Типы стволовых клеток 2.1 Эмбриональные стволовые клетки 2.2 Гемопоэтические стволовые клетки 2.3 ... Более того, рецепторы адгезии играют важную роль в регуляции поведения клеток, либо через прямую активацию сигнальных путей, важных для выживания клеток, клеточного роста и судьбы ... Вирусные векторы могут интегрировать гены в неделящиеся клетки, но возрастает эффективность трансдукции, если ГСК активированы в G1-фазу клеточного цикла. |
Раздел: Рефераты по медицине Тип: курсовая работа |
| ... к бронхиальной астме и туберкулезу по генам ферментов метаболизма ... | |
|
РОССИЙСКАЯ АКАДЕМИЯ МЕДИЦИНСКИХ НАУК СИБИРСКОЕ ОТДЕЛЕНИЕ ТОМСКИЙ НАУЧНЫЙ ЦЕНТР ГОСУДАРСТВЕННОЕ УЧРЕЖДЕНИЕ НАУЧНО-ИССЛЕДОВАТЕЛЬСКИЙ ИНСТИТУТ ... Белок входит в семейство функционально связанных мембранных белков (к этому семейству относят также Nramp2), ответственных за транспорт двухвалентных катионов, таких как Fe2+, Mn2 ... Депримирующее воздействие на цитохром Р450-зависимые монооксигеназы обнаружено у IFNa, IFNb, IFNg, IL-1 и TNF, IL-6, IL-11, IL-2. Цитокины угнетают транскрипцию генов и накопление ... |
Раздел: Рефераты по медицине Тип: дипломная работа |