Статья: Исследование механизма синергического действия смесей цинковых солей органических кислот и полиолов при термическом распаде поливинилхлорида (ПВХ)
ИССЛЕДОВАНИЕ МЕХАНИЗМА СИНЕРГИЧЕСКОГО ДЕЙСТВИЯ СМЕСЕЙ ЦИНКОВЫХ СОЛЕЙ ОРГАНИЧЕСКИХ КИСЛОТ И ПОЛИОЛОВ ПРИ ТЕРМИЧЕСКОМ РАСПАДЕ ПОЛИВИНИЛХЛОРИДА (ПВХ)
Термический распад ПВХ является последовательной ионно-молекулярной реакцией, осложненной каталитическим влиянием НС1 [1]. Для замедления скорости термораспада полимера необходимо связывать НС1 и понижать скорость последовательной реакции путем взаимодействия различных соединений с сопряженными двойными связями или путем обмена подвижных атомов хлора, находящихся в положении к двойным связям, на группы, более прочно связанные с полимерной цепочкой.
В работах [2] установлено, что стабилизирующая функция ряда соединений при термораспаде ПВХ, в том числе солей цинка органических кислот, связана с реакцией обмена между хлораллильными фрагментами и стабилизатором. Соли цинка не используются сами по себе в качестве стабилизаторов, так как время их действия очень мало. В практике стабилизации ПВХ их применяют часто с полиолами. Механизм действия этих смесей при термораспаде ПВХ неизвестен.
В работе [3] при изучении термораспада ПВХ в растворе ди-(2-этил-гексил) фталата в токе азота с добавками лаурата цинка показано, что пентаэритрит, маннит, сорбит заметно увеличивают индукционный период до начала выделения НС1 в свободном состоянии, скорость дегидрохлори-рования после индукционного периода не изменяется. Высказано предположение, что полиолы образуют комплексы с хлоридом цинка, предотвращая его каталитическое влияние на термораспад ПВХ. Однако при введении в ПВХ хлорида цинка и полиолов авторы работы [3] не наблюдали синергического эффекта.
В данной работе изучены кинетические закономерности реакции термического дегидрохлорирования ПВХ, сшивки макромолекул, электронные спектры поглощения образцов полимера при термораспаде ПВХ в присутствии добавок цинковых солей различных органических кислот, полиолов и их бинарных смесей.
В работе использовали ПВХ, полученный суспензионной полимеризацией винилхлорида в присутствии дициклогексилпероксидикарбоната (0,1%) в качестве инициатора, эмульгатор — метилцеллюлоза (0,035%), отношение мономер: вода=1 : 2, температура полимеризации 309 К.
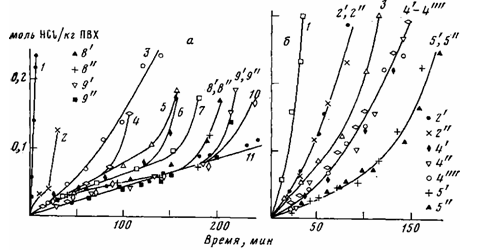
Рис. 1. Дегидрохлорирование ПВХ при 453 К в вакуумированных ампулах ~10-г Па с добавками (моль/кг ПВХ) смесей солей цинка с полиолами (о) или полиолов (<5). а: 1- 0,11, II; 2 - 0,11+0,14 ТЭГ; 3 - без добавки; 4 - 0,11+0,56 ТЭГ; 5 - 0,1 1+1,4 ТЭГ; 6 — ОД 1+0,7 ПЭГ; 7 - 0,11+1,12 ДЭГ; 8' — 0,11+0,15 пентаэритрита; 8" — 0,1 Н+0,93 ЭГ; 9' - 0,1 1+0,93 ЭГ; 9" - 0,1 Ш+0,15 пентаэритрита; 10 - 0,1 1+0,31 глицерина; 11 - без добавки в вакууме ~10-2 Па при постоянном вымораживании летучих продуктов; б: 1 - 0,2 ПЭГ; 2' - 0,15 ТЭГ; 2" - 0,28 ДЭГ; 3 - 0,47 ЭГ; 4' - 0,2 маннита; 4" - 0,2 СТО. 4"' - 0,25 БГ; 4"" — без добавки; 5' - 0,22 глицерина; 5" — 0,2 пентаэритрита
На рис. 1, а представлены кинетические кривые дегидрохлорирования ПВХ в присутствии солей цинка и смесей их с полиолами. При введении в полимер соли цинка скорость образования ионного хлора резко возрастает (кривая 1). Как было показано ранее [8], спирты увеличивают скорость дегидрохлорирования ПВХ. Из рис. 1, б видно, что полиолы или увеличивают (ЭГ, ДЭГ, ТЭГ, ПЭГ), или не влияют (БГ, маннит, GTC) на скорость распада полимера, лишь глицерин и пентаэритрит несколько замедляют ее.
Полиолы и спирты значительно понижают скорость дегидрохлорировавия полимера в присутствии солей цинка в течение периода Т (период Г-время от начала распада до резкого увеличения скорости дегидрохлорирования ПВХ в присутствии стабилизатора). В течение периода Т НС1 в свободном состоянии не обнаружен. При увеличении концентрации полиола в смеси соль цинка — полиол наблюдали большее понижение скорости дегидрохлорирования (рис. 1,а, кривые 2,4,5). При введении в ПВХ смеси соли цинка с пентаэритритом, глицерином или ЭГ скорость дегидрохлорирования совпадает со скоростью термораспада полимера в вакууме при постоянном удалении НС1 (кривые 8—10).
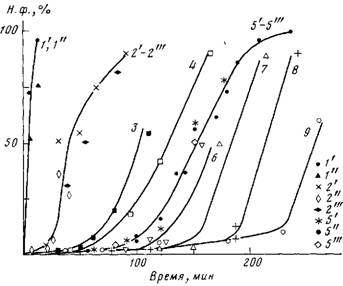
Рис. 2. Образование нерастворимой фракции (н.ф.) при термораспаде ПВХ при 453 К в вакуумированных до ~10-2 Па ампулах в присутствии смесей солей цинка с полиолами (моль/кг ПВХ): Г -0,11; 1" - 0,1 II; 2' - 0,28 ДЭГ; 2" — 0,56 ТЭГ; 2"' -0,93 ЭГ; 3 - 0,1 Ш+0,56 ТЭГ; 4 - 0,1 Ш+0,15 пентаэритрита; 5' - 0,1 Н+0,15 пентаэритрита; 5" - ПВХ без добавки; 5"' -0,15 пентаэритрита; 6 — 0,11+0,56 ТЭГ; 7-0,111+ +0,94 ЭГ; 8 - 0,11+0,15 пентаэритрита; 9 - 0,11+0,94 ЭГ
При термораспаде ПВХ в присутствии смесей карбоксилатов цинка с полиолами наблюдали большой индукционный период, в течение которого не образуется нерастворимая фракция (рис. 2, кривые 3—9), причем для смесей I с полиолами этот индукционный период совпадает с периодом Т (кривые 6,8,9). При раздельном введении в полимер полиолов (кривая 2) и карбоксилатов цинка (кривая 1) нерастворимая фракция появляется практически без индукционного периода.
За период Т при распаде ПВХ с добавками смесей солей цинка с полиолами практически не появляется окраска полимера, что подтверждают электронные спектры поглощения, в которых поглощение в видимой области спектра незначительно (рис. 3). В присутствии карбоксилатов цинка полимер при 453 К чернеет через ~2 мин. При распаде ПВХ с добавками полиолов сразу же появляется окраска полимера, углубляющаяся со временем (кривая S).
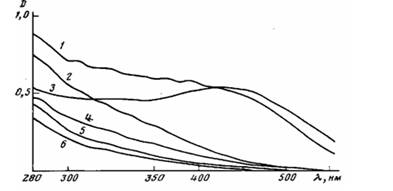
Рис. 3. Электронные спектры поглощения 0,8%-ных растворов в ТГФ образцов ПВХ, подвергнутых распаду при 453 К в вакуумированных до ~10-2 Па ампулах без добавок 60 мин (i) и с добавками (моль/кг ПВХ) в течение разного времени (указано в скобках в мин): 2 - 0,11+0,15 ПЭ (175); 3 — 0,2ТЭГ (20); 4 - 0,11+0,93 ЭГ (230); 5-0,1 Ш+0,56ТЭГ (60); 0,1 1+0,56 ТЭГ (110); 6-0,1 Н+0,93ЭГ (150)
Итак, соли цинка органических кислот со спиртами и полиолами образуют смеси, обладающие значительным синергическим действием на скорость дегидрохлорирования ПВХ, сшивку макроцепей, изменение цвета полимера.
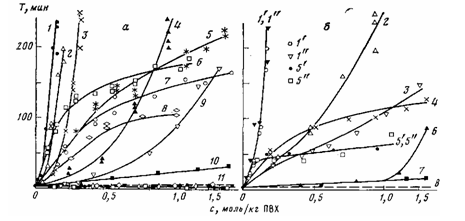
Рис. 4. Зависимость периода Т от концентрации полиолов при термораспаде ПВХ при 453 К в присутствии (моль/кг ПВХ) 0,1 I (в), 0,1 II {б, Г, 2, 3, 5) и 0,1 III (б, 1", 4, 6, 7). а: 1 - пентаэритрит, 2 — маннит, 3 — глицерин, 4 — ЭГ, 5 - ДЭГ, 6 - ПЭГ, 7 — ТЭГ, S-БГ, 9-СТС, 10 — ОКС. б: 1 - пентаэритрит, 2 — ЭГ, 3 - СТС, 4 — ТЭГ, 5'-ТЭГ, 5"- ПЭГ, 6 — СТС, 7 — ОКС. {11 (о), 8 (б)- теоретические кривые, построенные из условия аддитивности действия карбоксилатов цинка и кислородсодержащих соединений на период Т)
На рис. 4 представлена зависимость периода Т, характеризующего эффективность стабилизирующего действия смесей, от концентрации полиолов. Для солей цинка различных органических кислот общий вид кривых идентичен (рис. 4). Больший синергический эффект на процесс образования нерастворимой фракции (рис. 2), появления окраски полимера (рис. 3) и в ряде случаев по периоду Т (рис. 4) при использовании смесей I с полиолами обусловлен тем, что при взаимодействии с НС1 данной соли цинка образуется MOM, являющийся диенофилом, присоединяющимся к сопряженным двойным связям, ответственным за каталитическое действие НС1, сшивку макроцепей и появление окраски полимера [1].
По эффективности синергического действия в смеси с солями цинка изученные полиолы можно расположить в ряд: полиолы > диолы > алифатические спирты. Интересно отметить, что период Т значительно увеличивается, если смесь соли цинка с некоторыми диолами (ДЭГ, ТЭГ, ПЭГ) предварительно прогреть при 453 К в течение 10—20 мин, что не наблюдали для смесей с другими полиолами.
Соли цинка органических кислот — эффективные акцепторы НС1, однако при этом образуется ZnCl2, являющийся сильным катализатором дегидрохлорирования полимера.
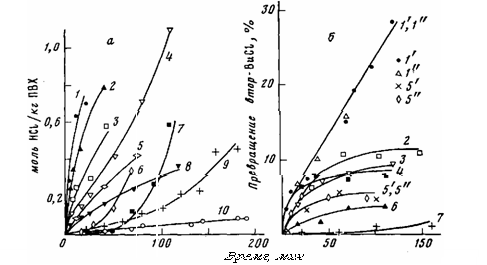
Рис. 5. Влияние полиолов, сложных эфиров на дегидрохлорирование ПВХ при 453 К (а) и втор-BuCl (2-Ю-3 моля) при 393 К (б) в присутствии ZnCl2, а - ПВХ в вакуумированных ампулах в присутствии (моль/кг ПВХ) 0,025 ZnCl2 (2); 0,025 ZnCl2 (1, 3-8) я добавок: 0,1 MOM (1), 0,87 ДОФ (3); 0,86 ОКС (4); 0,1 ДОМ (5); 0,2 ман-нита (б); 0,15 пентаэритрита (7); 0,8 ТЭГ (8). ПВХ без добавок в вакуумированных до ~10-2 Па ампулах (9); в вакууме ~10-2 Па при вымораживании летучих продуктов (10). б: Г— 10~4 моля ZnCl2 1—7 - смеси Ю-4 моля ZnCl2 с добавками (моль-104): Г'-MOM; 2-9,4 ЭГ; 3-2,4 вт-ор-бутилоктилмалеината; 4-8,8 ДОФ; 5'-7,9 ТЭГ; 5"- 6 ВС; 6 - 13 ОКС; 7 - 1,5 пентаэритрита
Для выяснения причин синергизма смеси соль цинка органической кислоты — полиол мы исследовали влияние полиолов на термораспад ПВХ в присутствии ZnCl2 (рис. 5, а). Как видно из рис. 5, а, спирты и полиолы замедляют каталитическое влияние ZnCl2 на термораспад полимера, а пентаэритрит и маннит полностью снимают каталитическое дегидрохлориро-вание ПВХ в присутствии ZnCl2 в течение определенного периода Т, затем скорость распада полимера резко возрастает, причем в течение периода Т скорость дегидрохлорирования ПВХ становится ниже, чем при распаде в вакууме при постоянном удалении НС1 (рис. 5, а, кривые 6,7), не меняется и окраска полимера. Как было показано выше, данные полиолы (пентаэритрит, маннит и другие) образуют с солями цинка органических кислот более эффективные синергические смеси, чем диолы и спирты (рис. 4).
Подобные закономерности получены и при изучении влияния полиолов на термораспад втор-BuCl (низкомолекулярная модель нормальных звеньев ПВХ) в присутствии ZnCl2 (рис. 5,6).
Полученные результаты подтверждают ранее высказанное предположение [3,9], что полиолы уменьшают каталитическое влияние ZnCl2 на распад ПВХ, образуя с ZnCl2 комплексы.
Однако только комплексообразованием ZnCl2 с полиолами нельзя объяснить синергизм действия смеси соль цинка органической кислоты — по-лиол при термораспаде ПВХ.
Достаточно прочные комплексы типа nv с хлоридами металлов (элек-трофильными катализаторами) II—V групп образуют не только полиолы, но и другие кислородсодержащие соединения: простые и сложные эфиры, кетоны, альдегиды, ангидриды кислот и другие [10]. Как видно из рис. 5, сложные эфиры замедляют скорость каталитического дегидрохлорирования ПВХ и низкомолекулярного модельного соединения под влиянием ZnCl2r очевидно, благодаря образованию комплексов с последним. Но сложные-и простые эфиры, альдегиды, ангидриды кислот и другие кислородсодержащие соединения не образуют с солями цинка смесей, синергически действующих при термораспаде ПВХ. (Зависимости периода Т от концентраций дибутилового эфира, бутилстеарата, дибутил-, диоктилфталата, ди-оксана, ацетилацетона, фталевого ангидрида, валерьянового альдегида, бензальдегида совпадают с теоретической кривой 11 рис. 4, а.) Они не понижают и скорость взаимодействия соли цинка органической кислоты с erop-BuCl (рис. 6). Спирты и полиолы значительно снижают ее (рис. 6), т. е. наблюдается разница в поведении полиолов и других кислородсодержащих соединений.
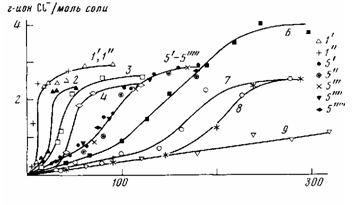
Рис. 6. Взаимодействие карбоксилатов цинка (Ю-4 моля) с втор-BuCl (210-3 моля) при 393 К в присутствии полиолов: Г—1; 4-11; 1 — 3; 5 — 9 — смеси I с добавками (моль-104): Г'-11,6 бензальдегида; 2-8,8 ДОФ; 3-2 СТС; 5'-1,6-7,9 ТЭГ; 5"-5 СТС; 5"'-5,6 ДЭГ; 5""- 3,6 ПЭГ; 5""'- 6,4 ВС; 6 - 9,4 ЭГ; 7-10 СТС; 8 - 13 ОКС; 9 - 2,5 глицерина
На низкомолекулярных модельных соединениях показано, что соли цинка органических кислот легко вступают в реакцию обмена с атомами хлора, находящимися в положении к двойной связи, параллельно катализируя распад низкомолекулярной модели [11,12]. Как отмечалось выше, эта реакция имеет большое значение в стабилизации ПВХ.
Мы исследовали взаимодействие солей цинка органических кислот с моделью нормальных звеньев ПВХ, втор-BuCl, при 393—453 К. В этом температурном интервале термораспада одного eгo BuCl не наблюдали. Как видно из рис. 6, кинетические кривые накопления ионного хлора при нагревании erop-BuGl в присутствии солей цинка имеют S-образный вид.
Методом газожидкостной хроматографии по накоплению соответствующего сложного эфира и бутена показано, что при 393 К в присутствии I или II протекает реакция обмена (за 40 мин на ~10% по отношению к количеству соли цинка) и реакция дегидрохлорирования. Из этого следует, что соли цинка органических кислот легко реагируют с нормальными звеньями макромолекул ПВХ, значительно ускоряя их распад. Реакция обмена солей цинка органических кислот с атомами хлора нормальных звеньев полимера не играет определяющей роли в процессе стабилизации, кроме того, она приводит к преждевременному расходованию исходной соли и накоплению ZnCl2 — более сильного катализатора термического дегидрохлорирования ПВХ.
Добавки полиолов приводят к снижению скорости взаимодействия солей цинка с втор-BuCl. При увеличении концентрации спирта (СТС) наблюдается усиление эффекта замедления скорости (рис. 6, кривые 3,5", 7). В случае диола (ТЭГ) в исследованном интервале концентраций этого не наблюдается (рис. 6, кривая 5). Наибольший эффект виден с глицерином (рис. 6, кривая 9), который является и одним из наиболее эффективных синергистов при термораспаде ПВХ в присутствии солей цинка (рис. 4).
Полученные данные свидетельствуют о том, что синергизм действия смеси соль цинка органической кислоты — полиол при термораспаде ПВХ обусловлен также снижением в присутствии полиолов скорости взаимодействия нормальных звеньев ПВХ с солями цинка, очевидно, благодаря образованию комплексов полиолов с солями цинка органических кислот.
При проведении термораспада втор-BuCl в присутствии БС и ZnCl2 в продуктах в небольших количествах обнаружен втор-бутил-бутиловый эфир. Образование его, очевидно, происходит по реакции втор-BuCl с нормальным БС при каталитическом действии ZnCl2. Известно о протекании подобных реакций с другими катализаторами [13]. Эти реакции идут легче с низкомолекулярными моделями лабильных структур ПВХ [13].
Реакция образования простых эфиров вносит определенный вклад в синергизм действия смеси соль цинка органической кислоты — полиол при термораспаде ПВХ, так как приводит к замене атомов хлора в положении к двойным связям на более прочно связанные с полимером группы.
Соли цинка катализируют также реакцию присоединения полиолов к двойным (сопряженным двойным) связям, образующимся при термораспаде ПВХ. Это подтверждается опытами по обесцвечиванию частично дегид-рохлорированного ПВХ. Если в ПВХ, подвергнутый термораспаду в вакууме при 453 К в течение 30 мин, ввести смесь I или II с полиолами (ЭГ, ТЭГ, пентаэритритом и др.) и затем прогреть еще 30 мин в вакуумирован ных ампулах, то полимер обесцвечивается. Уменьшение поглощения в видимой области спектра подтверждается электронными спектрами.
Каталитическое присоединение спиртов к непредельным соединениям описано в литературе [13]. Реакцию присоединения полиолов к двойным связям также необходимо учитывать при выяснении причин синергизма действия смеси соль цинка органической кислоты — полиол при термораспаде ПВХ.
Особое поведение спиртов и полиолов в смеси с карбоксилатами цинка при термораспаде ПВХ по сравнению с другими изученными кислородсодержащими соединениями связано, очевидно, с особенностями их комп-лексообразования, а также с реакционной способностью комплексов по отношению к нормальным и разрушенным звеньям макромолекул.
Из исследованных кислородсодержащих соединений только спирты и полиолы способны образовывать хелатные комплексные соединения с солями цинка органических кислот
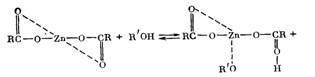
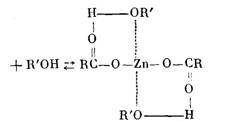
Известно [14], что хелатные комплексные соединения отличаются по химическому поведению от других типов комплексных соединений значительно повышенной термической стабильностью и пониженной реакционной способностью. Наиболее устойчивыми являются пяти- и шести-членные циклы.
Образование хелатов между карбоксилатами цинка и полиолами приводит к повышению термической стабильности соли и значительному понижению скоростей реакций взаимодействия карбоксилатов цинка с нормальными звеньями макромолекул, что наблюдается экспериментально (рис. 6). Приведенные ниже реакции с нестабильными фрагментами макромолекул ведут к образованию участков, распадающихся под влиянием тепла со значительно меньшей скоростью
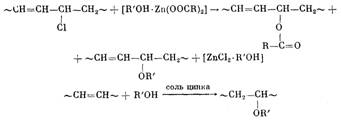
Определенный вклад в синергизм действия смеси карбоксилат цинка — полиол вносит и образование комплексов полиолов с ZnCl2.
Ранее было показано [1], что эффективный стабилизатор ПВХ должен обладать оптимальной реакционной способностью по отношению к хлорсодержащим фрагментам макромолекул полимера: обладать высокой активностью по отношению к хлораллильным группам, но не настолько большой, чтобы реагировать в заметной степени с нормальными фрагментами макромолекул. Полиолы в синергических смесях с солями цинка органических кислот, образуя с ними комплексы, понижают их реакционную способность в реакциях обмена и дегидрохлорирования нормальных звеньев макромолекул IIВХ, но вместе с тем комплексы достаточно реакционноспособны в реакциях обмена с лабильными хлораллильными фрагментами макромолекул и в реакциях присоединения к двойным (сопряженным двойным) связям.
Литература
1. Троицкий Б. Б., Троицкая Л. С. Высокомолек. соед. А, 1978, т. 20, № 7, с. 1443.
2. Frye А. Н., Horst R. W. J. Polymer Sci., 1959, v. 40, № 137, p. 419; 1960, v. 45, № 145, p. 1.
3. Briggs G., Wood N. F. J. Appl. Polymer Sci., 1971, v. 15, № 1, p. 25.
4. Kinney P. V. J. Appl. Polymer Sci., 1965, v. 9, № 6, p. 583.
5. Pilpel N. Chem. Revs, 1963, v. 63, № 3, p. 221.
6. Справочник химика. 3-е изд. испр. Л.: Химия, 1971.
7. Troitskii В. В., Troltskaya L. S., Denisova V. N., Novikova V. N., Luzinova Z. B. Europ. Polymer J., 1977, v. 13, p. 1033.
8. Троицкая Л. С, Мяков В. Н., Троицкий Б. В., Разуваев Г. А. Высокомолек. соед. А 1967 т. 9 № 10 с. 2119.
9. Wirth Н. О., Andreas Н. Pure Appl. Chem., 1977, v. 49, p. 627.
10. Гурьянова E. H., Голъдштейн И. П., Ромм И. П. Донорно-акцепторная связь. М.: Химия, 1973.
11. Klemchuk P. P. Advances Chem. Ser., 1968, № 85, p. 1.
12. Houng Т. V., Michel A. Europ. Polymer J., 1976, v. 2, № 6, p. 337.
13. Фурукава Дж., Саегуса Т. Полимеризация альдегидов и окисей. М.: Мир, 1965, с. 411.
14. Янсон Э. Ю. Комплексные соединения. М.: Высшая школа, 1968, с. 138.