Реферат: Технология получения и свойства мочевино-формальдегидных смол
Содержание
Введение
1 Исходное сырьё для получения МФС
2 Получение МФС
3 Технология производства
4 Свойства мочевино-формальдегидных смол
5 Применение
Заключение
Список литературы
Введение
Первые продукты конденсации мочевины с формальдегидом (карбамидные смолы) были получены еще в 1896 г., но производство мочевино-альдегидных смол налажено лишь в 1920—1921 гг.
Мочевино-формальдегидные смолы выпускались в виде литых прозрачных органических стекол (например, поллопаса) или прессованных изделий различной формы, но оказалось, что они недолговечны из-за недостаточной водостойкости и растрескивания. Поэтому эти смолы до введения в них наполнителя (целлюлозы, древесной муки, хлопкового волокна) в технике не использовались. Применение наполнителей уменьшило чувствительность изделий к изменению климатических условий. Хотя при этом прозрачность отчасти и терялась, но сохранялась светостойкость и возможность окрашивать изделия в светлые тона, а в ряде случаев получали также и просвечивающие изделия. Эти свойства позволили применять мочевино-формальдегидные смолы в декоративной технике, в которой феноло-формальдегидные смолы непригодны из-за темного цвета. Смолы совместной конденсации мочевины, тиомочевины и формальдегида отверждаются быстрее и водостойкость их лучше, чем мочевино-формальдегидных смол. Но они постепенно окрашиваются, что также ограничивает их применение.
В 1929 г. было впервые налажено производство пресс-порошков на основе мочевино-формальдегидных смол и целлюлозного волокна, а несколько позже (в 1934 - 1936 гг.) — слоистых пластиков на основе смолы и бумаги. Одновременно изучались возможности применения смол для изготовления лаков.
В настоящее время производство лаков и эмалей основано на использовании этерифицированных мочевино-формальдегидных смол и совмещенных продуктов.
В СССР производство мочевино-формальдегидных смол осуществлено на основе работ Г. С. Петрова и А. А. Ваншейдта с сотрудниками.
В настоящее время из мочевино-формальдегидных смол производят пресс-порошки, слоистые материалы, пенопласт, лаки и клеи. Смолы применяют для обработки тканей, бумаги, в производстве древесноволокнистых плит, в качестве связующего для изготовления формовочных смесей при литье металла и т. п.
1 Исходное сырьё для производства МФС
Мочевина. В чистом виде мочевина представляет собой бесцветные длинные иглы или белые призматические кристаллы. Она является диамидом угольной кислоты (карбамидом):
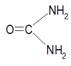
Мочевина –
это бесцветный кристалл с молекулярной массой 60.06 г/моль, плотностью 1.335
г/см3, показателем преломления 1.484, температурой плавления 132.7 ![]() и температурой
возгонки в вакууме 120 – 130
и температурой
возгонки в вакууме 120 – 130 ![]() .
.
Функциональность мочевины до настоящего времени является спорной. Хотя в некоторых реакциях все атомы водорода при атомах азота могут быть замещены, но, как указывает Марвел с сотрудниками, при образовании мочевино-формальдегидных смол она является трифункциональным соединением. Поэтому мочевину правильнее рассматривать как амид аминомуравьиной кислоты.
Водные
растворы мочевины имеют нейтральную реакцию на лакмус, - но наличие NH![]() - групп обуславливает
слабый основной характер. Константа ионизации мочевины в воде при 25 °С, равная
- групп обуславливает
слабый основной характер. Константа ионизации мочевины в воде при 25 °С, равная
![]() , указывает на ее слабое
сродство к протону воды.
, указывает на ее слабое
сродство к протону воды.
Несмотря на недостаточно выраженные свойства мочевины как основания, органические и неорганические кислоты образуют с ней соли. Сильные кислоты (азотная, серная и соляная) дают продукты присоединения в молярном соотношении 1:1, а более слабые органические кислоты (муравьиная, уксусная, пропионовая) — 1:2.
Мочевина достаточно устойчива при температуре плавления (133° С), но при более высокой температуре разлагается, выделяя аммиак и образуя биурет с температурой плавления 193° С:
2CO(NH![]() )
)![]()
![]() NH
NH![]() +
+![]()
Нагревание в вакууме до 120—130 °С приводит к возгонке мочевины. В разбавленных водных растворах кислот и щелочей, а также в воде мочевина менее устойчива и начинает разлагаться при нагревании выше 50 °С на аммиак и двуокись углерода.
Мочевина хорошо растворяется в воде, хуже в спирте.
Все современные методы производства мочевины основаны на химическом взаимодействии аммиака с двуокисью углерода и разложении полученных карбаматов аммония на мочевину и воду:
1. CО![]() +2NH
+2NH![]()
![]() H2N-COONH
H2N-COONH![]()
2. H2N-COONH4 ![]() H2O+H
H2O+H![]() NCONH
NCONH![]()
Обе реакции протекают в автоклаве при 160—200 °С и давлении 120—200 am, с большим выделением тепла. Продукты реакции (вода, мочевина, непрореагировавший карбамат аммония и аммиак, который в ряде процессов берется с большим избытком для повышения выхода мочевины с 40—50 до 75%) под уменьшенным давлением вводятся в другой аппарат. В нем происходит отделение водного раствора мочевины, разложение карбамата аммония на исходные продукты и вывод аммиака и двуокиси углерода для дальнейшего их разделения и рекуперации с целью возврата в производство.
Мочевина применяется в производстве пластмасс, в медицине, используется для разделения органических соединений, стабилизации поливинилхлорида и сополимеров винилхлорида с винилацетатом, как удобрение и в качестве растворителя.
Формальдегид (муравьиный альдегид) — бесцветное газообразное вещество со своеобразным острым запахом; температура кипения -19,2 °С; температура плавления -92 °С; плотность при —20 °С равна 0,8153 г/см3.
Газообразный формальдегид самопроизвольно полимеризуется при комнатной температуре и очень быстро — в присутствии небольших количеств хлористого водорода, фтористого бора и хлористого олова и температуре 90 °С; при этом образуется белый высокоплавкий порошок — параформальдегид — с температурой плавления 164—172 °С.
Параформ, или параформальдегид (СН2О)n, является аморфным полимером формальдегида.
Формальдегид легко растворяется в воде или в водном метаноле. Вода поглощает до 50% СН2О. Большинство исследователей считает, что в водных растворах формальдегид находится почти исключительно в гидратированной форме — в виде метиленгликоля.
СН2О
+ Н2О ![]() HOCH2OH
HOCH2OH
Этот вывод основан на том, что водные растворы формальдегида кипят при 100 °С, и что дистиллат при перегонке содержит формальдегида меньше, чем кубовый остаток. Если бы растворенный формальдегид не был в виде гидрата, он должен был бы отгоняться даже при слабом нагревании.
Формальдегид в водных растворах любой концентрации склонен к уплотнению с образованием полиоксиметиленгликолей. При этом происходят следующие реакции:
1) Образование димера:
НОСН2ОН
+ НОСН2ОН ![]() HOCH2OCH2OH + Н2О
HOCH2OCH2OH + Н2О
2) Удлинение цепи:
НОСН2ОСН2ОН + nНОСН2ОН ![]() HO(CH
HO(CH![]() O)n+1CH
O)n+1CH![]() OH + nH2O,
OH + nH2O,
где n = 3 - 4.
Таким образом, водные растворы формальдегида, называемые формалином, всегда содержат растворимые полиоксиметиленгликоли.
Формалин всегда содержит немного муравьиной кислоты, количество которой увеличивается при длительном хранении вследствие окисления формальдегида:
2СН2О
+ О2 ![]() 2НСООН
2НСООН
Из других свойств этого простейшего альдегида отмечаются те, которые необходимы для понимания закономерностей образования смол:
1) одновременное самоокисление и самовосстановление альдегидной группы в присутствии водного раствора щелочи, сопровождающееся образованием метилового спирта и муравьиной кислоты;
2) образование ацеталей при нагревании формальдегида сo спиртами (например, бутиловым):
СН2О
+ 2С4Н9ОН ![]() С4Н9ОCН2ОC4Н9 + Н2О;
С4Н9ОCН2ОC4Н9 + Н2О;
3) образование гексаметилентетрамина (уротропина) при действии аммиака на формальдегид:
6CH2O + 4NH3 ![]() (CH2)6N4 + 6H2O;
(CH2)6N4 + 6H2O;
Основным промышленным способом получения формальдегида является окисление метилового спирта кислородом воздуха при 400—600 °С в присутствии катализатора. Одновременно протекают две реакции — окисление и дегидрирование:
СН3ОН
+ ![]() О2
О2 ![]() СН2О + Н2О + 36,8 ккал/моль;
СН2О + Н2О + 36,8 ккал/моль;
СН3ОН
![]() СН2О + Н2
- 28,8 ккал/моль;
СН2О + Н2
- 28,8 ккал/моль;
Катализаторами процесса служат серебро, медь, окись молибдена (промотированная железом), фосфат марганца (промотированный молибденом) и др.
В последние годы формальдегид получают также окислением метана кислородом воздуха в присутствии окислов азота при 400—600 °С. Окисление протекает по схеме:
CН4
+ O2 ![]() CH2O + H2O (основная реакция)
CH2O + H2O (основная реакция)
2СН4
+ О2![]() 2СН3ОН
(побочная реакция)
2СН3ОН
(побочная реакция)
Разработаны способы получения формальдегида в смеси с другими продуктами реакции окислением кислородом воздуха некоторых углеводородов (пропана, н-бутана, изобутана при 400-500 °С).
2 Получение МФС
Механизм образования мочевино-формальдегидных смол детально не выяснен. Однако установлено, что при поликонденсации мочевины с формальдегидом в водном растворе в зависимости от рН среды, соотношения исходных компонентов, продолжительности реакции и температуры могут быть получены различные продукты. Так, в щелочной среде (рН 11–13) даже в разбавленных растворах образуется монометилолмочевина H2N-CO-NH-CH2-OH; в нейтральных и слабощелочных средах (рН 7–8) в зависимости от соотношения исходных компонентов – моно- и диметилолмочевины OC(NHCH2OH)2. Последняя образуется также при взаимодействии монометилолмочевины с формальдегидом. Положение равновесия этих реакций не зависит от рН среды, а определяется концентрацией реагирующих веществ и температурой.
При взаимодействии мочевины с формальдегидом в сильнокислой среде (рН<3) образующиеся метилолмочевины сразу же подвергаются дегидратации, давая метиленмочевины, например,
![]()
которые в условиях реакции быстро превращаются в полиметиленмочевины общей формулы (С2Н4N2O)n - неплавкие и нерастворимые аморфные продукты, не имеющие практического значения. Поэтому для получения мочевино-формальдегидных смол процесс следует проводить в условиях, способствующих образованию метилольных производных мочевины.
Моно- и диметилолмочевины – белые кристаллические продукты, растворимые в воде и метаноле; первый плавится при 111 °С (из этанола), второй – при 121 – 126 °С (из 80%-ного этанола); диметилолмочевина при нагревании растворяется также в этаноле. При нагревании безводные моно- и диметилолмочевины превращаются в полиметиленмочевины; первая полностью переходит в нерастворимый продукт при 100 °С, вторая – выше 140 °С. В водных кислых растворах (рН 4.5–6.0) метилолмочевина способна к дальнейшим превращениям с образованием, вероятно, метилен-бис-амида (I), метилолметилен-бис-амида (II) или простого эфира (III) и азометилена (IV), который сразу же тримеризуется:
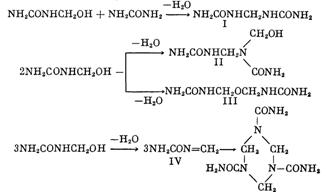
В аналогичных условиях скорость гомополиконденсации диметилолмочевины очень низка. Она также взаимодействует с мочевиной и монометилолмочевиной.
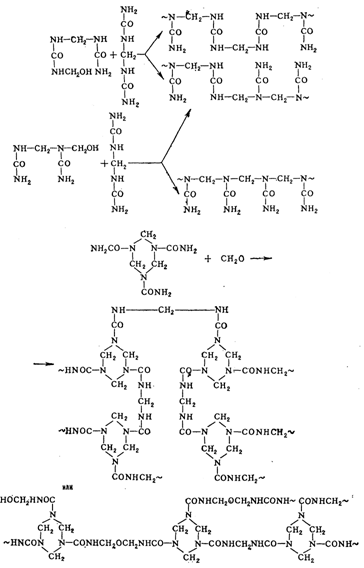
Предполагается, что основная реакция, приводящая к мочевино-формальдегидным смолам, – бимолекулярная, и скорость её пропорциональна концентрации водородных ионов. Далее приведены вероятные схемы образования мочевино-формальдегидных смол.
По-видимому, наиболее вероятна последняя схема, предусматривающая наличие в структуре полимера кислородных мостиков, присутствием которых можно объяснить выделение формальдегида при хранении и эксплуатации изделий из мочевино-формальдегидных смол.
Направление
реакции мочевины с формальдегидом зависит также от температуры. Повышение её
выше 40![]() (оптимальная
температура для получения метилол-мочевины) способствует образованию
нежелательных продуктов – метиленмочевин. Вероятность получения последних
существует и в том случае, когда процесс начинают в условиях, благоприятных для
синтеза метилолмочевин; это связано с изменением рН среды в ходе реакции. Так,
мочевина, способная образовывать с кислотами нестойкие соли, связывает
муравьиную кислоту, всегда содержащуюся в формалине. В результате этого при
добавлении мочевины в раствор формалина рН реакционной смеси повышается. Однако
по мере расходования мочевины кислота высвобождается и рН понижается. Кроме
того, в условиях реакции муравьиная кислота образуется из формальдегида
(реакция Канниццаро – Тищенко):
(оптимальная
температура для получения метилол-мочевины) способствует образованию
нежелательных продуктов – метиленмочевин. Вероятность получения последних
существует и в том случае, когда процесс начинают в условиях, благоприятных для
синтеза метилолмочевин; это связано с изменением рН среды в ходе реакции. Так,
мочевина, способная образовывать с кислотами нестойкие соли, связывает
муравьиную кислоту, всегда содержащуюся в формалине. В результате этого при
добавлении мочевины в раствор формалина рН реакционной смеси повышается. Однако
по мере расходования мочевины кислота высвобождается и рН понижается. Кроме
того, в условиях реакции муравьиная кислота образуется из формальдегида
(реакция Канниццаро – Тищенко):
2СН2О
+ NaOH ![]() CH3OH + HCOONa
CH3OH + HCOONa
По этой причине сначала получают метилольные производные мочевины, поддерживая нейтральную или слабощелочную среду (рН 7–8), а затем, не выделяя метилолмочевины из раствора, в слабокислой среде (рН 3–6,5) осуществляют их поликонденсацию. Слабокислая среда предотвращает чрезмерное нарастание вязкости смолы и преждевременное гелеобразование (особенно на стадии сушки). Для регулирования рН среды используют буферные вещества (ацетат натрия и его смесь с лимонной кислотой, карбонат аммония и другие), а также уротропин. При нагревании мочевины и формальдегида в присутствии последнего раствор с течением времени приобретает ту кислотность, которую он имел до прибавления уротропина. По-видимому, уротропин образует с муравьиной кислотой буферные соли, разрушающиеся при нагревании. Проведение реакции в водных средах препятствует отщеплению воды от метилолмочевин, что предотвращает их переход в метиленмочевины.
3 Технология производства
Механизм образования мочевино-формальдегидных смол сложен. Всегда в качестве начального продукта образуется моно- и диметилолмочевина, которые при дальнейшей поликонденсации в слабокислой среде дают линейные полимеры.
Суммарно реакцию можно представить так:
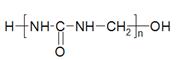
СН2О+nCO(NH2)2![]() +(n+1)H2O
+(n+1)H2O
Технологический процесс производства мочевино-формальдегидной смолы осуществляется жидкофазным непрерывным методом и состоит из следующих основных стадий: подготовка сырья; приготовление реакционного раствора; конденсация в щелочной и кислой средах; нейтрализация и сушка смолы; доконденсация смолы с мочевиной; охлаждение, стабилизация и стандартизация смолы.
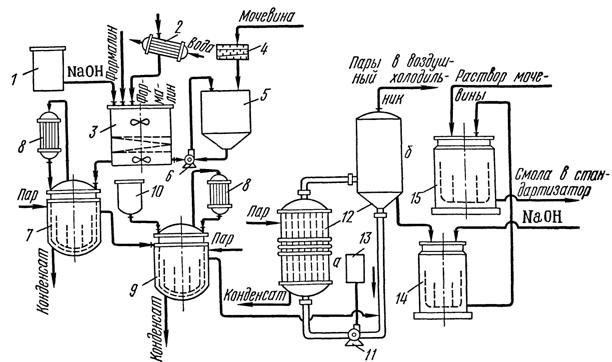
1, 13 — мерники едкого натра, 2 — теплообменник для формалина, 3—смеситель, 4—зубчатая дробилка, 5—емкость, 6, 11—циркуляционные насосы, 7 — первый реактор, 8 — холодильник, 9—второй реактор, 10—мерник кислоты, 12—выпарной аппарат (а—кипятильник, б—сепаратор), 14—сборник смолы, 15—реактор.
В смеситель 3 подаются 2%-ный раствор едкого натра из мерника 1 и формалин из прицеховой ёмкости. Формалин может охлаждаться в теплообменнике 2. Едкий натр загружается из расчёта получения в растворе рН 4,8 – 6,5. Мочевина измельчается на зубчатой дробилке 4 и подаётся в ёмкость 5, через которую прокачивается смесь формалина с едким натром из смесителя 3 циркуляционным насосом 6. Циркуляция ведётся до полного растворения мочевины, после чего определяется рН раствора, которая должна быть в пределах 7,5 – 8,5. Коэффициент рефракции должен быть 1,409 – 1,412. В реакционной смеси поддерживается температура 20 – 35 °C за счёт подачи воды или пара в змеевики смесителя 3.
Каждый агрегат для получения смолы имеет два смесителя: в одном готовится конденсационный раствор, а из другого раствор непрерывно расходуется.
Из смесителя 3 конденсационный раствор непрерывно подаётся в реактор 7 со скоростью, зависящей от производительности агрегата. Реактор снабжён рубашкой для нагрева и охлаждения, якорной мешалкой и холодильником 8. В реакторе 7 проводится конденсация в щелочной среде при 90 – 98 °C и непрерывном перемешивании. Пары конденсируются в холодильнике 8 и стекают обратно в реактор. При конденсации рН раствора снижается до 6,0 – 7,0. В начальной стадии процесса в нейтральной или слабощелочной среде образуется смесь моно- и диметилолмочевин, растворимых в воде. При дальнейшем нагреве происходит поликонденсация метилолмочевин, в результате образуется линейный полимер с метиленовыми связями и выделяется вода.
Из реактора 7
реакционный раствор непрерывно перетекает в реактор 9, в который также
непрерывно поступает из мерника 10 серная кислота (0,5 – 1,0%-ный раствор). В
реакторе поддерживается рН смеси 5,0 – 5,4 и температура 94 – 98 ![]() . Поликонденсация при
непрерывном перемешивании продолжается до достижения вязкости смолы 14 – 15 по
вискозиметру ВЗ-1. Образовавшиеся пары конденсируются в холодильнике 8 и
стекают обратно в реактор 9.
. Поликонденсация при
непрерывном перемешивании продолжается до достижения вязкости смолы 14 – 15 по
вискозиметру ВЗ-1. Образовавшиеся пары конденсируются в холодильнике 8 и
стекают обратно в реактор 9.
Сконденсировавшаяся смола подаётся непрерывно из реактора 9 циркуляционным насосом 11 в выпарной аппарат 12, состоящий из кипятильника кожухотрубного а и сепаратора б. Для нейтрализации смолы и поддержания рН в пределах 7,0 – 8,0 в насос из мерника 13 непрерывно поступает 2%-ный раствор едкого натра. Кипятильник представляет собой трубчатый теплообменник, в трубках которого циркулирует смола, а в межтрубном пространстве – пар давлением 4 кгс/см2. Сепаратор – цилиндрический аппарат с коническим днищем и крышкой.
Сушка смолы
проводится при рН 7,0 – 7,8, температуре 96 – 100 ![]() до достижения вязкости от 50 – 60
до 110 – 120 (по вискозиметру ВЗ-1). Пары, получаемые при сушке смолы,
поступают в воздушный холодильник, конденсируются; надсмольная вода собирается
в ёмкость, откуда перекачивается для дальнейшей обработки (выделения метанола и
очистки воды от остатков формальдегида).
до достижения вязкости от 50 – 60
до 110 – 120 (по вискозиметру ВЗ-1). Пары, получаемые при сушке смолы,
поступают в воздушный холодильник, конденсируются; надсмольная вода собирается
в ёмкость, откуда перекачивается для дальнейшей обработки (выделения метанола и
очистки воды от остатков формальдегида).
Упаренная
смола поступает из сепаратора в сборник 14, в который подаётся 2%-ный раствор
едкого натра для поддержания рН смолы в пределах 7,0 – 8,0. Из сборника 14
смола подаётся в реактор 15, в который поступает расчётное количество 64 –
67%-ного водного раствора мочевины, и при 60 – 85 ![]() происходит доконденсация смолы до
достижения содержания формальдегида ниже 1,2%.
происходит доконденсация смолы до
достижения содержания формальдегида ниже 1,2%.
Из реактора 15 смола перекачивается в стандартизатор, где она стабилизируется 25%-ной аммиачной водой для повышения рН до 7,5–9,0 и увеличения жизнеспособности, и стандартизируется в результате перемешивания.
Из стандартизатора смола перекачивается насосами в складские ёмкости, из которых она поступает в железнодорожные цистерны и бочки.
4 Свойства мочевино-формальдегидных смол
Мочевино-формальдегидные смолы – твёрдые
продукты белого цвета, легко растворимые в воде и нерастворимые в
неорганических растворителях. Отверждение мочевино-формальдегидных смол
ускоряется в присутствии кислотных катализаторов и с повышением температуры. В
качестве катализаторов используют как органические (щавелевая, фталевая), так и
минеральные (фосфорная, соляная) кислоты и некоторые соли (AlCl3, ZnCl2). Продукты отверждения
– бесцветные, светостойкие, легко окрашивающиеся полимеры. Смолы, отверждённые
при низких температурах даже в присутствии больших количеств катализатора,
имеют пониженную водостойкость. При повышении температуры отверждения
водостойкость возрастает. Однако продукты, полученные в оптимальном режиме (120
– 140 ![]() ,
катализатор), всё же частично разлагаются под действием горячей воды или водных
растворов солей. Это обусловлено недостаточной разветвлённостью цепей и малым
количеством поперечных связей, о чём свидетельствует низкое коксовое число
продуктов отверждения (14 – 21,5%) и их быстрая деструкция при нагревании без
доступа воздуха.
,
катализатор), всё же частично разлагаются под действием горячей воды или водных
растворов солей. Это обусловлено недостаточной разветвлённостью цепей и малым
количеством поперечных связей, о чём свидетельствует низкое коксовое число
продуктов отверждения (14 – 21,5%) и их быстрая деструкция при нагревании без
доступа воздуха.
Существенный недостаток мочевино-формальдегидных смол – выделение формальдегида в процессе переработки и при эксплуатации отверждённых смол. Это объясняется наличием в материале формальдегида, не прореагировавшего при поликонденсации, а также образованием его вследствие наличия в полимере метилольных групп и метиленэфирных связей, превращающихся в метиленовые. Формальдегид оказывает токсичное действие на организм человека и вызывает растрескивание изделий.
Отверждённые мочевино-формальдегидные смолы (в отличие от феноло-формальдегидных) прозрачны даже тогда, когда в них содержится 10 – 15% воды. Вода находится в полимере в диспергированном состоянии и химически не связана с ним. Она постепенно испаряется даже при комнатной температуре, причём происходит усадка и растрескивание материала. Поэтому для удержания некоторого количества воды в мочевино-формальдегидные смолы иногда вводят гидрофильные добавки (поливиниловый спирт, крахмал, белковые вещества) и твёрдые наполнители (например, древесную муку), препятствующие усадке полимера.
5 Применение
Мочевино-формальдегидные смолы применяют в качестве связующих в производстве аминопластов, слоистых пластиков и для изготовления клеев. Мочевино-формальдегидные смолы, модифицированные бутиловым спиртом, используют в смеси с другими плёнкообразующими для приготовления электроизоляционных, декоративных, антикоррозионных лакокрасочных материалов.
Мочевино-формальдегидные смолы, модифицированные фуриловым спиртом, используют для изготовления литейных стержней для алюминиевого и чугунного литья. Они экономически выгодны в высокопроизводительном литейном производстве.
Мочевино-формальдегидные смолы, модифицированные поливинилацетатной эмульсией, используют в производстве карбамидных клеев и в качестве связующих в производстве слоистых пластиков, к которым предъявляются высокие требования по водостойкости.
Водоэмульсионные мочевино-формальдегидные смолы, модифицированные глицерином, способствующим снижению хрупкости полимера, используют для получения тепло- и звукоизоляционного пенопласта – мипоры.
В России производятся мочевино-формальдегидные смолы марок МФ, М, УКС, бартрев. За рубежом мочевино-формальдегидные смолы выпускают под названиями: аутосет, формасет, циакор резин, урак резин, америте (США); фиталак, каларок (Великобритания); ипорка, бекурол, фестопас, элмопласт (Германия); аминоцел (Италия); сидонур (США, Канада, Великобритания, Германия), деламин (Австрия) и др.
Заключение
Из всего вышесказанного можно сделать вывод о том, что развитие производства данного полимера довольно перспективно. Разнообразный характер применения мочевино-формальдегидных смол объясняется их дешевизной и доступностью сырья. Для получения мочевино-формальдегидных смол есть развитая сырьевая база, а технология изготовления их сравнительно проста.
Широкое применение мочевино-формальдегидных смол основано на наличии у них ряда важных технических свойств, например, они способны отверждаться как при нагреве, так и при комнатной температуре, они бесцветны и способны окрашиваться в любой цвет.
На основе водных растворов мочевино-формальдегидных смол изготовляют клеи, применяемые в деревообрабатывающей и мебельной промышленности. Клеи способны клеить древесину с влажностью 8 – 15%, они стойки к микроорганизмам, воде, бензину и маслам и негорючи. Жизнеспособность отдельных марок клеев (время, в течение которого клей не желатинизируется) составляет от 3 до 6 часов. Недостаток их – в постепенном выделении в помещении формальдегида, которого содержится в клее около 2%.
Наряду с чистыми мочевино-формальдегидными полимерами выпускаются модифицированные полимеры, модифицированные бутиловым и многоатомными спиртами. Эти полимеры являются важными в техническом отношении продуктами и применяются для изготовления лаков горячей воздушной сушки, используемых для пропитки ткани, бумаги, для изготовления кабеля, окраски холодильников, медицинского и торгового оборудования.
Немодифицированные и модифицированные мочевино-формальдегидные смолы широко используются для получения пресс-материалов, которые применяются для производства деталей телефонов, радиоприёмников и телевизоров, электроосветительной аппаратуры и бытовых предметов.
К сложностям производства можно отнести то обстоятельство, что моно- и диметилолмочевина получаются только при точном соблюдении условий реакции. При несоблюдении указанных условий можно получить нерастворимый в воде и других растворителях осадок – метиленмочевину. При получении мочевино-формальдегидных смол избегают образования метиленмочевины, так как она ухудшает качественные показатели смол. Процесс надо вести так, чтобы смола получилась при конденсации смеси моно- и диметилолмочевины.
Список литературы
1. “Энциклопедия полимеров”, 2-й том. Изд. “СЭ”, М., 1975 г.
2. А.Ф. Николаев, “Синтетические полимеры и пластические массы на их основе”, изд. 2-е, “Химия”, М., 1966 г.
3. И.Ш. Пик, С.А. Азерский “Технология пластических масс. Учебное пособие для проф.-техн. учебн. заведений. М., “Высшая школа”, 1975 г.
| Развитие, становление и основные аспекты фармации | |
|
РАЗВИТИЕ, СТАНОВЛЕНИЕ И ОСНОВНЫЕ АСПЕКТЫ ФАРМАЦИИ Для ветеринарного провизора необходимы знания, с помощью которых можно контролировать качество ... При осторожном наслаивании на раствор формальдегида в концентрированной серной кислоте раствора препарата на границе слоев появляется кольцо красного цвета (проба Ле Розена). Серебро восстанавливается из аммиачного раствора серебра нитрата при нагревании с раствором формальдегида. |
Раздел: Рефераты по медицине Тип: книга |
| Методы анализа лекарственных препаратов | |
|
Оглавление Вступление Глава 1. Основные принципы фармацевтического анализа 1.1 Критерии фармацевтического анализа 1.2 Ошибки, возможные при проведении ... Так, например, температура плавления, растворимость, рН среды водного раствора и т.д. являются критериями как подлинности, так и чистоты лекарственного вещества. 1 (с. 116) приведены подробные сведения о приготовлении стандартных буферных растворов для различных областей рН: от 1,2 до 11,4. В качестве реактивов для этой цели используют ... |
Раздел: Рефераты по медицине Тип: дипломная работа |
| Проект производства формалина | |
|
РЕФЕРАТ Дипломный проект состоит из 186 страниц, 36 таблиц, 2 рисунка, 19 источников и 8 листов графического материала. Тема дипломного проекта ... В - третьих, в виде водно-метанольного раствора формальдегид может применяться в большинстве производственных синтезов, а также при непосредственном использовании. и, наконец, в ... Поэтому формальдегид транспортируется и хранится либо в растворах, либо в виде полимера. |
Раздел: Промышленность, производство Тип: дипломная работа |
| Общая и неорганическая химия | |
|
Квантово-механическая модель атома. Квантовые числа. Атомные орбитали. Порядок заполнения орбиталей электронами Теория строения атома основана на ... Эти отклонения связаны с тем, что молекулы электролита в водном растворе распадаются на ионы, и в единице объёма раствора будет содержаться большее число частиц, чем в исходной ... Отсюда ясно, что в нейтральном растворе pH=7; в кислых растворах рН<7 и тем меньше, чем кислее раствор; в щелочных растворах рН>7, и тем больше, чем больше щёлочность раствора. |
Раздел: Рефераты по химии Тип: учебное пособие |
| Химия и технология платиновых металлов | |
|
Буслаева Татьяна Максимовна Химия и технология платиновых металлов (Лекционный курс) Москва - 1999 г. Введение Платиновые металлы - это элементы VIII ... 8 представлены результаты ионообменной сорбции хлорокомплексов Pt(II), Pt(IV), Pd(II), Pd(IV), Os(IV), Ir(III), Ir(IV) из солянокислых растворов на сильноосновной анионообменной ... ПОЛИОРГС'ы химически устойчивы в водной среде в широком диапазоне кислотности, а также при нагревании растворов до 100 оС. |
Раздел: Рефераты по химии Тип: учебное пособие |