Курсовая работа: Биологическая функция нуклеиновых кислот
Курсовая работа по биохимии растений
Тема: Биологическая функция нуклеиновых кислот
Воронеж 2011г.
Введение
Термин нуклеиновые кислоты был предложен немецким химиком Р. Альтманом в 1889г после того, как эти соединения были открыты в 1868г. швейцарским врачом Ф. Мишером. Он экстрактировал клетки гнойного пневмококка разбавленной соляной кислотой в течение нескольких недель и получил в остатке почти чистый ядерный материал, назвав его нуклеином (от лат. nucleus — ядро). По своим свойствам нуклеин резко отличался от белков: он был кислым, не содержал серы, было много фосфора. Нуклеин хорошо растворялся в щелочах, но не растворялся в разбавленных кислотах.
Впоследствии из животных, растительных объектов и микроорганизмов были выделены разные нуклеиновые кислоты. Их наилучшим источником оказались клетки, имеющие большие ядра.
Химически нуклеиновые кислоты представляют собой биополимеры, состоящие из мономерных звеньев — нуклеотидов. Каждый нуклеотид содержит три различных компонента: азотистое (пуриновое или пиримидиновое) основание, моносахарид пентозу (рибозу или дезоксирибозу) (Rb), остаток фосфорной кислоты (P). Как показал специфический гидролиз (кислотный, щелочной), а также гидролиз ферментами-нуклеазами, эти компоненты соединены друг с другом в такой последовательности: азотистое основание — пентоза — фосфат. Соседние нуклеотиды связаны друг с другом посредством эфирной связи между моносахаридом и фосфатом другого нуклеотида.
Поскольку остаток пентозы и фосфат соединены эфирной связью, то при образовании полинуклеотидной цепи связь Rb-P-Rb называется фосфодиэфирной.
Азотистые основания не участвуют в образовании никаких других ковалентных связей, помимо связывающей их с остатками пентозы сахарофосфатной цепи. Именно последовательность азотистых оснований в полинуклеотидной цепи определяет уникальную структуру и специфическую функцию молекул нуклеиновых кислот.
Гидролиз нуклеиновых кислот, выделенных из ядер клеток, показал, что они состоят из пуриновых (аденина, гуанина) и пиримидиновых (цитозина, тимина) оснований, 2-дезоксирибозы и фосфорной кислоты. Эта нуклеиновая кислота была названа дезоксирибонуклеиновой кислотой (ДНК). Из дрожжей была получена другая по химическому составу нуклеиновая кислота, содержащая вместо тимина урацил и вместо дезоксирибозы рибозу. Ее назвали рибонуклеиновой кислотой (РНК).
Биологическая функция нуклеиновых кислот оставалась неизвестной в течение почти столетия. Только в 40-х гг. XXв. О.Т . Эвери, К. Мак-Леод и М. Мак-Карти установили, что эти биополимеры ответственны за хранение, репликацию (воспроизведение), транскрипцию (передачу) и трансляцию (воспроизведение на белок) генетической (наследственной) информации. В 1953г., когда Дж. Уотсон и Ф. Крик сообщили о расшифровке молекулярной структуры ДНК, биохимия и вообще биология начала отсчет новой эры познания живой материи.
1. Обзор литературы
1.1. Структура нуклеотидов
Пуриновые основания имеют следующее строение
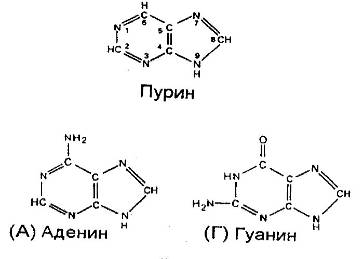
Сам пурин не входит в состав нуклеотидов, а входят его производные – аденин (А), или 6-аминопурин, и гуанин (G), или 2-амино-6-оксипурин.
Пиримидиновые азотистые основания имеют следующее строение
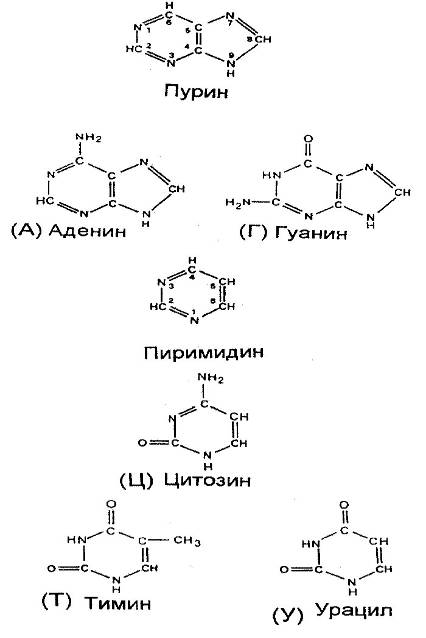
Пиримидин также не входит в состав нуклеотидов, а входят его производные — урацил (U), или 2,4-диоксипиримидин, тимин (Т), или 5-метилурацил, цитозин (С), или 2-окси-4-аминопиримидин.
В составе ДНК и РНК встречаются более редкие азотистые основания, например, 5-метилцитозин, 4-тиоурацил и дигидроурацил; они получили название минорных оснований.
В состав ДНК входят ![]()
![]() -D-2-дезоксирибоза, в состав РНК —
-D-2-дезоксирибоза, в состав РНК — ![]() -D-рибоза. И в том, и в другом случае эти монозы являются пентозой
(пять углеродных атомов), различия касаются лишь второго углеродного атома. В
рибозе углерод-2 связан с ОН-группой, тогда как в дезоксирибозе на месте
ОН-группы находится Н, отсюда префикс "дезокси". Буквы
-D-рибоза. И в том, и в другом случае эти монозы являются пентозой
(пять углеродных атомов), различия касаются лишь второго углеродного атома. В
рибозе углерод-2 связан с ОН-группой, тогда как в дезоксирибозе на месте
ОН-группы находится Н, отсюда префикс "дезокси". Буквы ![]() и D отражают специфическую конфигурацию при атомах С-1' и С-4'
фуранозного цикла:
и D отражают специфическую конфигурацию при атомах С-1' и С-4'
фуранозного цикла:
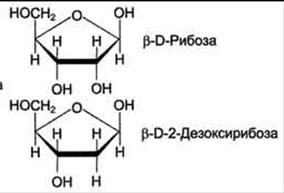
Нуклеозиды — соединения, в которых пуриновые или пиримидиновые основания связаны с рибозой (рибонуклеозиды) или дезоксирибозой (дезоксирибонуклеозиды). Нуклеозиды относятся к N-гликозидам: атом С-1' рибозы или дезоксирибозы связан с N-9 пуринового или N-1 пиримидинового основания:
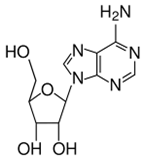
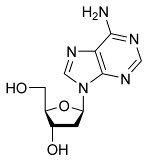
Аденозин 2'-дезоксиаденозин
В состав ДНК и РНК входят следующие нуклеозиды.
ДНК
Аденин + дезоксирибоза = дезоксиаденозин.
Гуанин + дезоксирибоза = дезоксигуанозин.
Цитозин + дезоксирибоза = дезоксицитидин.
Тимин + дезоксирибоза = дезокситимидин.
РНК
Аденин + рибоза = аденозин.
Гуанин + рибоза = гуанозин.
Цитозин + рибоза = цитидин.
Урацил + рибоза = уридин.
Кроме выше перечисленных главных нуклеозидов встречаются и минорные нуклеозиды, из которых наиболее распространены дигидроуридин, псевдоуридин; в последнем отсутствует обычная N-гликозидная связь: в нем атом С-1' рибозы соединен с атомом С-5 урацила.
Нуклеозиды лучше растворимы в воде, чем исходные азотистые основания. Их легко можно разделить и идентифицировать методом тонкослойной хроматографии. Они устойчивы к щелочам, но легко гидролизуются кислотами, а также ферментом нуклеозидазой.
Нуклеотиды представляют собой нуклеозиды с присоединенной эфирной связью к остатку рибозы или дезоксирибозы фосфатной группой. В образовании связи участвует 5'-углеродный атом пентозы. В зависимости от строения пентозы все нуклеотиды можно разделить на рибонуклеотиды и дезоксирибонуклеотиды:
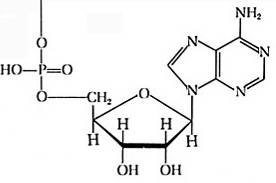

Аденозин-5'-монофосфат 2'-Дезоксиаденозин-5'-монофосфат
В зависимости от числа остатков фосфорной кислоты нуклеотиды подразделяются на нуклеозид-5'-монофосфаты, нуклеозид-5'-дифосфаты и нуклеозид-5'-трифосфаты. В принципе нуклеозид может быть фосфорилирован до тетрафосфата.
Ниже приводятся названия и сокращенные обозначения нуклеотидов:
Названия Сокращенные обозначения
Рибонуклеотиды
Аденозинмоно-, ди-, трифосфат АМР, АDР, АТР
Гуанозинмоно-, ди-, трифосфат GМР, GDР, GТР
Цитидинмоно-, ди-, трифосфат СМР, СDР, СТР
Уридинмоно-, ди-, трифосфат UМР, UDР, UТР
Дезоксирибонуклеотиды
Дезоксоаденозинмоно-, ди-, трифосфат dАМР, dАDР, dАТР
Дезоксигуанозинмоно-, ди-, трифосфат dGМР, dGDР, dGТР
Дезоксицитидинмоно-, ди-, трифосфат dСМР, dCDР, dCТР
Дезокситимидинмоно-, ди-, трифосфат dТМР, dTDР, dTTP
Данная номенклатура нуклеотидов рассматривает их как фосфорные эфиры. В то же время благодаря наличию кислотной фосфатной группы удобно рассматривать нуклеозидмонофосфаты как кислотные производные исходных нуклеозидов, например, адениловая, уридиловая, гуанидиловая, цитидиловая кислоты.
Нуклеотиды — сильные кислоты, так как остаток фосфорной кислоты, входящей в их состав, сильно диссоциирован. При рН 7,0 свободные нуклеотиды в клетках находятся главным образом в форме
R —рибоза— ![]()
где R—азотистое основание.
Уникальны биохимические функции нуклеотидов. В качестве основных можно отметить следующие:
1) являются строительными блоками нуклеиновых кислот (ДНК и РНК); участвуют в молекулярных механизмах, с помощью
которых генетическая информация хранится, реплицируется и транскрибируется;
2) выполняют важную роль в энергетическом (фосфорном) обмене, в аккумулировании и переносе энергии;
3) служат агонами (коферментами и активными простетическими группами) в окислительно-восстановительных ферментах;
4) играют важную роль в синтезе олиго- и полисахаридов, жиров.
Таким образом, нуклеотиды — универсальные биомолекулы, играющие фундаментальную роль в обмене веществ и энергии живой клетки.
1.2. Первичная структура полинуклеотидов
ДНК и РНК представляют собой полинуклеотиды, имеющие три уровня структуры: первичную, вторичную, третичную.
Специфичность нуклеиновых кислот определяется не только их
нуклеотидным составом, но и последовательностью отдельных нуклеотидов в цепи
нуклеиновых кислот. В состав ДНК входит всего 4 нуклеотида, но, учитывая очень
высокую молекулярную массу ДНК, нетрудно представить, что разнообразие ее типов
выражается поистине астрономическими цифрами. Например, если мы возьмем
цепочку, состоящую только из 100 нуклеотидов, то очевидно, что она может быть
построена 4![]() способами.
способами.
Установлено, что ДНК каждого определенного вида характеризуется только ей присущей специфичной последовательностью нуклеотидов.
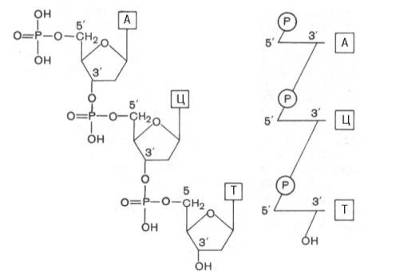
Рис.1 Схематическое изображение фрагмента полинуклеотида
Полинуклеотиды состоят из нуклеотидов, соединенных фосфорноэфирными связями с участием 3'- и 5'- углеродных атомов пентозных остатков двух соседних нуклеотидов. Длинные полинуклеотидные цепи содержат тысячи, миллионы нуклеотидных остатков. Фосфатные группы в цепях обладают сильнокислыми свойствами и при рН 7,0 полностью ионизированы. Поэтому в живых клетках нуклеиновые кислоты существуют в виде полианионов. Нуклеиновые кислоты плохо растворимы в растворах кислот. Они экстрагируются из разрушенных тканей и клеток растворами нейтральных солей или фенолом.
1.3. Вторичная и третичная структуры ДНК
Растворы ДНК характеризуются аномальной (структурной) вязкостью. В потоке обладают двойным лучепреломлением, что объясняется удлиненной формой молекул ДНК.
В расшифровку структуры ДНК большой вклад внесли исследования Э. Чаргаффа и его сотрудников (1945—1951 гг.). Для разделения оснований, полученных при кислотном гидролизе ДНК, Э. Чаргафф использовал метод хроматографии. Каждое из этих оснований было определено спектрофотометрически. Он впервые определенно заявил, что ДНК обладают выраженной видовой специфичностью. ДНК, выделенные из различных источников, отличаются друг от друга по соотношению входящих в их состав азотистых оснований. Э. Чаргафф сформулировал закономерности состава ДНК, известные под названием правил Чаргаффа. Независимо от происхождения ДНК эти закономерности представляются следующим образом:
1) количество молекул аденина равно количеству молекул тимина (А = Т);
2) количество молекул гуанина равно количеству молекул цитозина (G = С);
3) количество молекул пуриновых оснований равно количеству молекул пиримидиновых оснований (А + G = Т + С);
4) количество оснований с 6-аминогруппами в цепях ДНК равно количеству оснований с 6-гидроксигруппами (А + С = G + Т);
5) отношение (G+С)/(А+Т) резко отличается для разных видов ДНК, но постоянно для клетки одного вида; это отношение называется фактором специфичности.
Фактор специфичности одинаков для ДНК различных органов и тканей одного организма и практически не отличается у разных видов животных и растений в пределах одного класса. У высших растений и животных его величина находится в пределах 0,55—0,93; у бактерий — 0,35—2,73.
Правила Чаргаффа сыграли решающую роль в разработке проблем молекулярной биологии. Именно они легли в основу открытия строения ДНК, ее вторичной структуры.
Прежде чем приступить к рассмотрению этой структуры, необходимо отметить следующее. Интерес к проблеме изучения структуры ДНК возрос в связи с полной неясностью механизма воспроизведения (репликации) ДНК, который отличается очень высокой степенью точности. На основании уже полученных экспериментальных данных предполагалось, что генетическая информация в живой клетке зашифрована (т.е. записана с помощью определенного кода) в специфической последовательности оснований ДНК. Однако было неясно, как воспроизводится такая последовательность.
В 1953 г. Дж. Уотсон и Ф. Крик предложили модель структуры ДНК (рис.2). Она учитывала рентгеноструктурные данные Р. Франклин и М. Уилкинса и "эквимолярность" оснований, открытую Э. Чаргаффом. Модель Уотсона — Крика не только объяснила физико-химические свойства ДНК, но и дала основание высказать предположение о возможном механизме репликации ДНК. Согласно их выводу, молекула ДНК должна быть двухцепочечной. Каждое основание одной цепи "спарено" с лежащим в той же плоскости основанием второй полинуклеотидной цепи. Это спаривание специфично; поскольку количество оснований с гидроксигруппами равно количеству оснований с аминогруппами, то, по Уотсону и Крику, только определенные пары оснований входят в структуру так, что могут образовывать друг с другом водородные связи. Так как аденин содержит аминогруппу, а тимин — гидроксигруппу, цитозин и гуанин — соответственно эти же группы и поскольку они находятся в ДНК в эквимолекулярных количествах, то разрешенными являются только пары А-Т и G-С
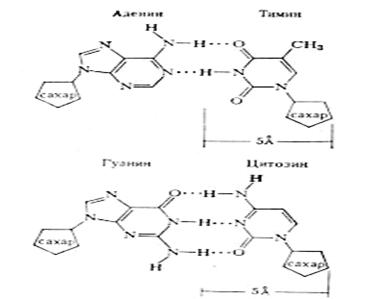
Рис.2. Соединение пар аденина и тимина, цитозина и гуанина в молекуле ДНК при помощи водородных связей
Между А и Т образуются две водородные связи, между G и С - три водородные связи.
Две полинуклеотидные цепи ДНК отличаются одна от другой как последовательностью оснований, так и нуклеотидным составом. Однако основания, стоящие в данном положении в одной цепи, определяют природу основания в другой цепи. Например, если в одной цепи стоит аденин, то напротив него в другой цепи будет располагаться тимин, и наоборот. Если в одной цепи стоит гуанин, то в другой обязательно будет цитозин, и наоборот. Действительно, рентгеноструктурный анализ ДНК показал, что пуриновые и пиримидиновые основания нуклеотидных остатков ДНК лежат в одной плоскости, перпендикулярной продольной оси молекулы, тогда как циклы дезоксирибозы находятся в плоскости, почти перпендикулярной той, в которой лежат циклы оснований.
Явление, при котором последовательность оснований одной цепи однозначно определяет последовательность оснований другой цепи, получило название комплементарности. Таким образом, цепи молекул ДНК комплементарны по отношению друг к другу.
Сформулированный Уотсоном и Криком принцип комплементарности явился универсальным принципом в биологии. Он дал начало развитию новых научных направлений — молекулярной биологии, молекулярной генетике, генной инженерии. Водородные связи обеспечивают способ спаривания оснований, стабильность двухцепочечной системы. Основания плотно упакованы, причем расстояние между центрами оснований, лежащих друг над другом, равно 0,34 нм. На каждый полный виток двойной спирали приходится 10 нуклеотидных пар. Упакованные внутри двойной спирали основания гидрофобны и недоступны молекулам воды. Ионизированные фосфатные группы и гидрофильные остатки дезоксирибозы находятся на поверхности молекулы и контактируют с молекулами воды. Таким образом, двойная спираль стабилизирована не только водородными связями между комплементарными основаниями, но и гидрофобными взаимодействиями между основаниями, расположенными вдоль длинной оси молекулы ДНК. Из-за высокой степени упорядоченности макромолекул ДНК ее иногда называют апериодическим одномерным кристаллом.
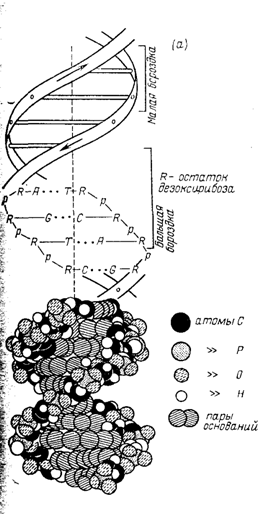
Рис.3 Макромолекулярная структура ДНК
При рентгенографическом исследовании головок сперматозоидов получается такая же дифракционная картина, что и для образцов ДНК, т.е. спираль Уотсона—Крика наблюдается непосредственно в живых клетках.
Модель строения ДНК в настоящее время является общепризнанной. За расшифровку структуры ДНК Дж. Уотсону, Ф. Крику и М. Уилкинсу в 1962 г. была присуждена Нобелевская премия.
Третичная структура ДНК образуется в результате дополнительного скручивания в пространстве двухцепочечной молекулы. Она имеет вид суперспирали или изогнутой (сломанной) двойной спирали.
В настоящее время описаны три формы структуры ДНК: А-, В- и Z-формы (рис.4). Параметры модели Уотсона—Крика соответствуют конформации ДНК в физиологических условиях (В-форме ДНК). Однако при изменении условий среды двойная спираль может принимать другие формы. Так при уменьшении влажности (в препарате образца для рентгеноструктурного анализа) ДНК переходит в А-форму. Этот переход связан с изменением конформации в остатках дезоксирибозы, уменьшением расстояния между фосфатными группами сахарофосфатного остова. Расстояние между парами нуклеотидов вдоль оси спирали, равное 0,34 нм в уотсон-криковской модели, уменьшается (примерно до 0,25 нм при 11 нуклеотидных остатках на один виток спирали). Диаметр спирали увеличивается; изменяются ширина и глубина бороздок; комплементарные пары азотистых оснований образуют с осью спирали угол 20° и, главное, они смещаются к периферии спирали. Поэтому двойная спираль похожа на пологую винтовую лестницу и внутри нее возникает полость диаметром 0,40 нм.
Переход молекулы ДНК из В- в А-форму можно осуществить при понижении активности воды в растворе (при внесении в него органического растворителя, например, этанола). Существует мнение, что В-форма представляет собой некую промежуточную форму двух или большего числа конформаций. Одной из особенностей В-формы, называемой В'-формой, является способность менять в молекуле ДНК положение двух цепей на обратное. Более того, В-форма может существовать в виде как правой, так и левой спирали.
Хотя более стабильными в А- и В-формах являются правозакрученные спирали, существуют довольно устойчивые и левозакрученные спирали ДНК. Одна из таких спиралей была получена в 1979 г. А. Ричем. Из-за нерегулярного зигзагообразного изгиба cахарофосфатного остова она была названа Z-формой (рис.4). Повторяющаяся единица в Z-форме ДНК включает две пары нуклеотидов, а не одну, как в В- и А-формах. Вследствие этого линия, соединяющая фосфатные группы, через каждые две пары нуклеотидов имеет излом и принимает зигзагообразный вид. По сравнению с В-формой в левой Z-форме резко изменен характер стэкинга оснований: сильные и слабые межплоскостные взаимодействия также чередуются. Z-форма может переходить в В-форму при снижении ионной силы раствора, добавлении этанола. Однако вопрос о существовании Z-формы ДНК in vivo и ее биологической роли до конца не выяснен. Высказывается мнение, что переход правозакрученной формы в левозакрученную может служить регуляторным сигналом, контролирующим экспрессию генов.
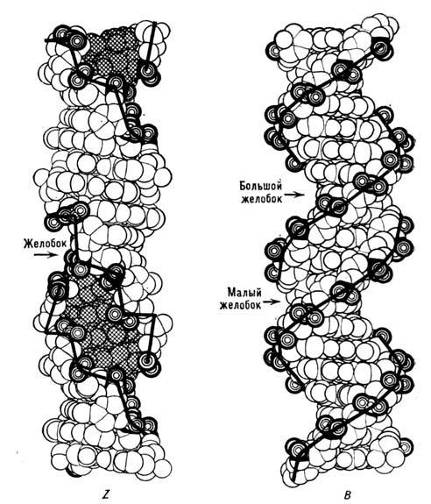
Рис.4. B- и Z-формы структуры ДНК
1.4. Физико-химические свойства ДНК
ДНК — довольно сильная многоосновная кислота, полностью ионизированная
при рН 4,0. Фосфатные группы расположены по периферии. Они прочно связывают
ионы Са![]() и
Мg
и
Мg![]() , амины, гистоны — положительно
заряженные белки. Устойчивость комплементарных пар оснований зависит от
величины рН. Пары оснований наиболее устойчивы в интервале рН 4,0—11,0. За его
пределами двухцепочечная спираль ДНК теряет устойчивость и раскручивается.
, амины, гистоны — положительно
заряженные белки. Устойчивость комплементарных пар оснований зависит от
величины рН. Пары оснований наиболее устойчивы в интервале рН 4,0—11,0. За его
пределами двухцепочечная спираль ДНК теряет устойчивость и раскручивается.
Молекулярная масса ДНК неодинакова и зависит от источника ее
получения. К тому же даже при самых тщательных и щадящих процедурах выделения
ДНК подвергается некоторой деградации. Препараты, полученные современными
методами из тканей животных и растений, имеют молекулярную массу 6 10![]() —10 10
—10 10![]() . Однако истинная
молекулярная масса ДНК животных и растений, определенная по вязкости и по длине
молекул, значительно выше и достигает десятков миллиардов.
. Однако истинная
молекулярная масса ДНК животных и растений, определенная по вязкости и по длине
молекул, значительно выше и достигает десятков миллиардов.
У большинства вирусов ДНК представляет собой двойную спираль,
линейную или замкнутую в кольцо. У некоторых вирусов она представляет собой
одну полинуклеотидную цепь, замкнутую в кольцо и имеющую сравнительно небольшую
молекулярную массу — 2 10![]() . ДНК сравнительно легко
деполимеризуется под действием некоторых химических соединений, ультразвука,
ионизирующей и ультрафиолетовой радиации. Нагревание растворов ДНК до температур
70—80 °С, а также их подщелачивание вызывают денатурацию ДНК, заключающуюся в
плавлении двойной спирали (разрушение водородных связей и гидрофобных взаимодействий),
и расхождение полинуклеотидных цепей. Денатурация сопровождается понижением
вязкости раствора, повышением поглощения в ультрафиолетовой области,
увеличением отрицательного удельного вращения плоскости поляризации света,
увеличением плавучей плотности образцов ДНК. Возрастание светопоглощения света
при 260 нм называется гипохромным эффектом; это важнейший критерий денатурации
ДНК, по которому можно контролировать этот процесс.
. ДНК сравнительно легко
деполимеризуется под действием некоторых химических соединений, ультразвука,
ионизирующей и ультрафиолетовой радиации. Нагревание растворов ДНК до температур
70—80 °С, а также их подщелачивание вызывают денатурацию ДНК, заключающуюся в
плавлении двойной спирали (разрушение водородных связей и гидрофобных взаимодействий),
и расхождение полинуклеотидных цепей. Денатурация сопровождается понижением
вязкости раствора, повышением поглощения в ультрафиолетовой области,
увеличением отрицательного удельного вращения плоскости поляризации света,
увеличением плавучей плотности образцов ДНК. Возрастание светопоглощения света
при 260 нм называется гипохромным эффектом; это важнейший критерий денатурации
ДНК, по которому можно контролировать этот процесс.
В отличие от многих глобулярных белков, денатурация которых происходит постепенно в широком температурном интервале, нативные ДНК денатурируют в узком интервале температур (~10 °С), поэтому тепловую денатурацию часто называют плавлением. Температура плавления тем выше, чем больше в молекуле ДНК GС-пар; этот показатель может использоваться для определения нуклеотидного состава ДНК. Установлено, что температура плавления линейно связана с составом ДНК: ее повышение на 1° соответствует 2,5 молярных % GС-пар. Гомогенные препараты ДНК характеризуются плавлением с резким переходом спираль—клубок, тогда как гетерогенные препараты дают сравнительно широкую зону плавления, что может служить мерой гетерогенности ДНК. При быстром охлаждении после тепловой денатурации ДНК не восстанавливает своих нативных свойств; однако, при медленном охлаждении полинуклеотидные цепи реассициируются по принципу комплементарности, т.е. происходит ренатурация молекул ДНК. Это продемонстрировано, в частности, на препаратах ДНК пневмококка с помощью методов электронной микроскопии и градиентного ультрацентрифугирования в СsСl.
1.5. Биологические функции ДНК
Важнейшая биологическая функция ДНК — генетическая, т.е. хранение и передача наследуемых признаков. В 1943 г. О. Т. Эвери,
К. Мак-Леод и М. Мак-Карти из Рокфеллеровского института обнаружили это впервые. Они экспериментально установили, что невирулентный штамм бактерии Pneumococcus может превратиться в вирулентный простым добавлением ДНК, выделенной из вирулентных пневмококков. Исследователи заключили, что ДНК может содержать генетическую информацию. Работа О. Т. Эвери и его сотрудников признана выдающейся, представляющей собой важную историческую веху в исследовании генетической функции ДНК. Сейчас многочисленными экспериментами установлено, что ДНК — основной компонент клеточных органелл-хромосом. Трансформирующаяся ДНК включается ковалентно в ДНК невирулентной клетки (клетки-реципиента) и, таким образом, реплицируется вместе с хромосомой реципиента; свойство вирулентности наследуется. В то же время возможность передачи генетической информации бактериальным клеткам в результате введения РНК или белка не получила экспериментального подтверждения.
На вопрос, почему наследуемые признаки копируются с удивительной
точностью, дает ответ принцип комплементарности. Модель ДНК, разработанная
Уотсоном и Криком, четко объясняет механизм передачи информации. В связи с тем,
что последовательность азотистых оснований одной цепи однозначно определяет последовательность
оснований в другой цепи, репликация ДНК в клетке происходит в результате
расхождения двух полинуклеотидных цепей и последующего синтеза двух новых
(дочерних) цепей на старых (родительских) цепях как на матрицах. В результате
образуются две дочерние двухцепочечные молекулы ДНК, идентичные родительской
молекуле ДНК, содержащие по одной цепи из родительской молекулы. Такой механизм
репликации был назван полуконсервативным. Он получил блестящее подтверждение в
экспериментах с клетками E.coli и меченым азотом N![]() , проведенных М. Мезелсоном и Ф. Сталем в 1957 г. Полученные ими результаты точно согласуются с полуконсервативным механизмом редупликации
макромолекул ДНК.
, проведенных М. Мезелсоном и Ф. Сталем в 1957 г. Полученные ими результаты точно согласуются с полуконсервативным механизмом редупликации
макромолекул ДНК.
1.6. Структура и физико-химические свойства РНК
Рибонуклеиновые кислоты (РНК) — однонитевые молекулы, поэтому
в отличие от ДНК их вторичная и третичная структуры нерегулярны. Нуклеотидная
цепь РНК обладает гибкой структурой, ее длина в зависимости от вида РНК может
варьировать в очень широких пределах — от нескольких десятков до десятков тысяч
нуклеотидных остатков; молекулярная масса РНК находится в пределах 10![]() —10
—10![]() .
.
Последовательность нуклеотидных звеньев, соединенных фосфодиэфирной связью в неразветвленную полинуклеотидную цепь, представляет собой первичную структуру РНК. Вторичная и третичная структуры РНК, определяемые как пространственная конформация полинуклеотидной цепи, формируются в основном за счет водородных связей и гидрофобных взаимодействий между азотистыми основаниями. Если для молекулы нативной ДНК характерна устойчивая спираль, то структура РНК более многообразна и лабильна. Рентгеноструктурный анализ показал, что отдельные участки полинуклеотидной цепи РНК, перегибаясь, навиваются сами на себя с образованием внутриспиральных структур. Стабилизация структур достигается за счет комплементарных спариваний азотистых оснований антипараллельных участков цепи; специфическими парами здесь являются А - U, G - С и, реже, G – U.
Образование спиральных структур сопровождается гипохромным эффектом — уменьшением оптической плотности образцов РНК при 260 нм. Разрушение этих структур происходит при понижении ионной силы раствора РНК или при его нагревании до 60—70 °С; оно также называется плавлением и объясняется структурным переходом спираль — хаотический клубок, что сопровождается увеличением оптической плотности раствора нуклеиновой кислоты.
Хотя РНК относится к однониточным полинуклеотидам, вместе с тем в ее цепях имеются участки различной длины, состоящие из комплементарных друг другу нуклеотидных последовательностей, включающих от десятков до тысяч нуклеотидных остатков, расположенных на небольшом удалении друг от друга. Благодаря этому в молекуле РНК возникают как короткие, так и протяженные биспиральные участки, принадлежащие одной цепи; эти участки носят название шпилек. Модель вторичной структуры РНК со шпилькообразными элементами была создана в конце 50-х — начале 60-х гг. XX в. в лабораториях А. С. Спирина (Россия) и П. Доти (США).
полинуклеотид нуклеозидфосфат тонкослойный хроматография
1.7. Типы РНК и их биологические функции
Клетки содержат три основных типа РНК: рибосомную — рРНК, транспортную — тРНК и матричную (информационную) — мРНК. Каждая из этих РНК выполняет специфическую роль в сложном процессе биосинтеза белка, при котором последовательность аминокислот однозначно определяется нуклеотидной последовательностью ДНК.
В эукариотических клетках существуют также малые ядерные РНК (мяРНК), являющиеся участниками процессинга РНК, и гетерогенные ядерные РНК (гяРНК), представляющие собой предшественников мРНК. Кроме того, обнаружена так называемая антисмысловая РНК, участвующая в регуляции процесса репликации ДНК.
В процессе транскрипции нуклеотидная последовательность локуса (место в хромосоме, где находится ген) в ДНК копируется в молекулу РНК. Транскрибируются три вида генов. Транскрипты генов рРНК используются в синтезе рибосом, нуклеотидная последовательность мРНК переписывается в последовательность аминокислот при синтезе полипептида на рибосоме, а транскрипты генов тРНК связываются с аминокислотами, которые затем переносятся в рибосомный синтезирующий центр в последовательности, зашифрованной в мРНК; этот процесс называется трансляцией.
Рибосомная РНК. Она входит в состав клеточных органелл —
рибосом. Биохимическая функция рРНК пока до конца не изучена.
Предполагается, что она выполняет роль молекулярного каркаса, на котором
крепятся участники процесса трансляции; рРНК имеет большую молекулярную массу
(до 2 10![]() ),
характеризуется метаболической стабильностью. На ее долю приходится до 85—90 %
всех клеточных РНК. Степень спирализованности молекул рРНК находится в пределах
70—80 %.
),
характеризуется метаболической стабильностью. На ее долю приходится до 85—90 %
всех клеточных РНК. Степень спирализованности молекул рРНК находится в пределах
70—80 %.
Предполагается, что в белоксинтезирующей системе клетки
функция рРНК не исчерпывается ролью структурного компонента. У прокариотов обнаружено, что в рРНК имеются небольшие участки, комплементарные участкам мРНК. Спаривание этих участков, видимо, способствует первоначальному связыванию мРНК с рибосомой. Не исключено, что некоторые участки рРНК играют определенную роль в формировании пептидтрансферазного центра рибосомы, ответственного за образование пептидных связей при синтезе белка.
Транспортные РНК. Это низкомолекулярные нуклеиновые кислоты; молекулярная масса колеблется в пределах 23 000—30 000, каждой из 20 белковых аминокислот соответствует, по крайней мере, одна тРНК. Однако некоторым аминокислотам специфичны от 2 до 6 тРНК; предполагается их общее количество около 60. Они составляют примерно 15 % общего количества клеточных РНК. Многие тРНК получены в гомогенном состоянии, некоторые — в кристаллическом виде.
Небольшая молекулярная масса, наличие достаточно большого количества
(до 10 %) минорных оснований, которые являются прекрасными маркерами,
существенно облегчают проблему определения нуклеотидной последовательности
тРНК. В 1965 г. Р. Холли и его сотрудники установили полную нуклеотидную
последовательность аланиновой тРНК дрожжей; в 1967 г. А.А. Баев и сотрудники установили последовательность нуклеотидов валиновой тРНК дрожжей. А.
Рич и др. (1975—1977 гг.) провели полную расшифровку пространственной структуры
фенилаланиновой тРНК на основе рентгенограмм с разрешением до 0,4 нм. Вторичная
структура тРНК в плоском изображении имеет вид клеверного листа (рис. 3). тРНК
содержит 4 двухцепочечных спиральных участка, 3 из которых являются "шпильками",
несущими петли из неспаренных нуклеотидов; 3'- и 5'-концы полинуклеотидной цепи
объединены в наиболее длинный спиральный участок, образованный водородными
связями между азотистыми основаниями и завершающийся неспаренным тринуклеотидом
ССА, Кроме четырех основных ветвей, более длинные тРНК содержат короткую пятую,
или дополнительную, ветвь. Две из основных ветвей непосредственно обеспечивают
функцию тРНК как адалтора (между двадцатибуквенным кодом белков и четырехбуквенным
кодом нуклеиновых кислот). Антикодоновая ветвь имеет антикодон, представляющий
собой специфический триплет нуклеотидов, комплементарный кодону мРНК и способный
образовывать с ним пары оснований. Акцепторная ветвь присоединяет специфическую
аминокислоту за счет образования эфирной связи между ее карбоксильной группой и
гидроксильной группой 3'-концевого остатка аденина в тРНК, Две другие главные
ветви тРНК называются дигидроуридиловая ветвь и Т![]() С-ветвъ. Первая содержит необычный
нуклеозид дигидроуридин, а вторая — нуклеозиды псевдоуридин (
С-ветвъ. Первая содержит необычный
нуклеозид дигидроуридин, а вторая — нуклеозиды псевдоуридин (![]() ) и риботимидин (Т),
обычно не присутствующие в составе РНК.
) и риботимидин (Т),
обычно не присутствующие в составе РНК.
Исследования структуры тРНК методом рентгеноструктурного анализа показали, что их нативные молекулы имеют компактную форму; отдельные двухспиральные "шпильки" клеверного листа складываются в специфическую третичную структуру, которая является близкой для всех тРНК.
После ферментативной этерификации свободной 3'-гидроксигруппы концевого остатка адениловой кислоты в последовательности ССА специфической в отношении тРНК аминокислотой образуется активная форма, называемая аминоацил-тРНК. Остаток этой аминокислоты переносится к концу растущей полипептидной цепи. Антикодон обеспечивает специфичность взаимодействия тРНК с мРНК. Боковые петли, видимо, играют важную роль в связывании тРНК с аминоацил-тРНК-синтетазой и с комплексом рибосома—мРНК. Аддукты аминоцил—тРНК располагаются в определенной последовательности, связанной с последовательностью кодонов мРНК.
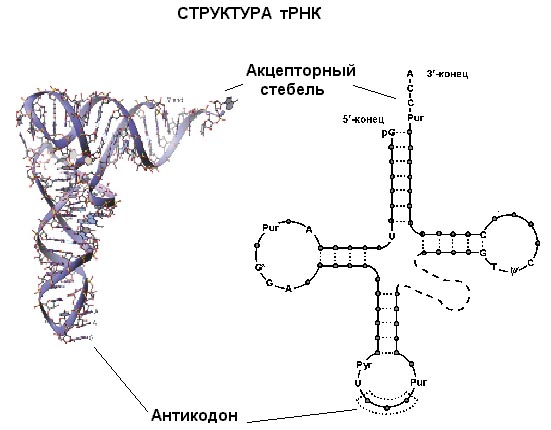
Рис.5 Структура транспортной РНК
Матричная РНК составляет незначительную часть (3—10 %) всех
клеточных РНК; молекулярная масса колеблется в широких пределах и доходит до 14
10![]() . Она
программирует синтез всех клеточных белков цитоплазмы. Относительное содержание
индивидуальной мРНК в суммарном препарате РНК может составлять тысячные доли
процента. Первые экспериментальные доказательства существования мРНК получили
А.Н. Белозерский, А.С. Спирин и их сотрудники (1957—1960 гг.). Они показали,
что нуклеотидный состав общей РНК бактерий E. coli коррелирует с
составом их ДНК, и пришли к заключению о наличии, по крайней мере, двух типов
РНК, один из которых (большая фракция) имеет состав, не отражающий состава ДНК,
а второй (меньшая фракция) воспроизводит состав ДНК. В дальнейшем выяснилось,
что первая фракция — это рибосомная РНК, а вторая — мРНК. Но это сделали в 1961 г. Ф. Гросс и сотрудники.
. Она
программирует синтез всех клеточных белков цитоплазмы. Относительное содержание
индивидуальной мРНК в суммарном препарате РНК может составлять тысячные доли
процента. Первые экспериментальные доказательства существования мРНК получили
А.Н. Белозерский, А.С. Спирин и их сотрудники (1957—1960 гг.). Они показали,
что нуклеотидный состав общей РНК бактерий E. coli коррелирует с
составом их ДНК, и пришли к заключению о наличии, по крайней мере, двух типов
РНК, один из которых (большая фракция) имеет состав, не отражающий состава ДНК,
а второй (меньшая фракция) воспроизводит состав ДНК. В дальнейшем выяснилось,
что первая фракция — это рибосомная РНК, а вторая — мРНК. Но это сделали в 1961 г. Ф. Гросс и сотрудники.
Если рРНК и тРНК метаболически устойчивы, то мРНК в большинстве случаев, особенно у прокариот, является относительно короткоживущей. Ее нуклеотидный состав близок к составу ДНК, выделенной из того же организма. мРНК имеют отчетливо выраженную вторичную структуру; в состав двухцепочечных участков включено до 75 % всех нуклеотидных последовательностей мРНК. Значительная часть участков вторичной структуры в мРНК идентифицирована "шпильками". Однако роль участков вторичной структуры в реализации матричных функций пока точно не установлена. Предполагается, что "шпильки" выполняют роль специфических структур, обусловливающих узнавание определенных участков рибосом при их связывании с мРНК.
Если рРНК и тРНК относятся к обслуживающему аппарату белоксинтезирующей системы клетки, то мРНК является прямым посредником между ДНК и белками, играет роль матрицы для синтеза последних, поэтому считают, что она выполняет роль мессенджера. Сама мРНК синтезируется в ядре клетки в процессе транскрипции у в ходе которой нуклеотидная последовательность одной из цепей хромосомной ДНК ферментативным путем "переписывается" (транскрибируется) с образованием предшественника пре-мРНК; последняя имеет копии палиндромов ДНК, поэтому ее вторичная структура содержит шпильки и линейные участки. При созревании пре-мРНК шпильки отсекаются ферментами и образуется мРНК.
2. Материалы и методы исследований
2.1. Кислотный гидролиз нуклеопротеидов дрожжей и изучение свойств ДНК И РНК
Оборудование и реактивы: весы технические; весы торзионные;
электроплитка; водяная баня; центрифуга; колба на 100 мл с обратным
холодильником; пробирки; пипетки на 1 и 20 мл. Концентрированная и 10%-ная
серная кислота; 10%-ный раствор NaOH; концентрированный
раствор аммиака; 1% раствор AgNO![]() ; бидистиллированная вода; раствор дифениламина (1 г дифениламина растворяют в 50 мл ледяной уксусной кислоты, добавляют 2,75 мл концентрированной H
; бидистиллированная вода; раствор дифениламина (1 г дифениламина растворяют в 50 мл ледяной уксусной кислоты, добавляют 2,75 мл концентрированной H![]() SO
SO![]() и доводят ледяной уксусной кислотой до 100 мл);
молибденовый реактив (18,75 г молибдата аммония растворяют в 250 мл 32%-ного
раствора HNO
и доводят ледяной уксусной кислотой до 100 мл);
молибденовый реактив (18,75 г молибдата аммония растворяют в 250 мл 32%-ного
раствора HNO![]() ); 1%-ный раствор CuSO
); 1%-ный раствор CuSO![]() ; 1%-ный раствор тимола.
; 1%-ный раствор тимола.
Материалы: дрожжи сухие; препараты ДНК и РНК.
Ход работы
1. Гидролиз нуклеопротеидов. В коническую колбу на 100 мл
вносят 1 г сухих дрожжей, добавляют 20 мл 10%-ного раствора H![]() SO
SO![]() и 20 мл бидистиллированной воды. Колбу соединяют с
обратным холодильником, нагревают до кипения и кипятят в течение 1 ч, охлаждают
и центрифугируют 5 мин при 5000 об/мин.
и 20 мл бидистиллированной воды. Колбу соединяют с
обратным холодильником, нагревают до кипения и кипятят в течение 1 ч, охлаждают
и центрифугируют 5 мин при 5000 об/мин.
2. Качественные реакции на пентозы:
а) к 0,5 мл нейтрализованного щелочью гидролизата добавляют 2 капли 1%-ного спиртового раствора тимола, перемешивают и осторожно прослаивают равный объем концентрированной серной кислоты. На дне пробирки образуется красное окрашивание в результате конденсации тимола с фурфуролом, получившимся из пентозы;
б) к 5-10 мг продажного препарата ДНК прибавляют 1 мл 0,4%-ного раствора NaOH, перемешивают. Из полученного раствора отбирают 0,3-0,5 мл раствора дифениламина и ставят на кипящую водяную баню на 10 мин. Жидкость приобретает синий цвет вследствие взаимодействия дезоксирибозы, образовавшейся в результате гидролиза ДНК, с дефиниламином;
в) к 10 мг продажного препарата РНК прибавляют 1 мл 0,4%-ного
раствора NaOH, перемешивают. К 0,5 мл щелочного раствора
РНК добавляют 0,5 мл раствора дифениламина и ставят пробирку на кипящую водяную
баню на 15 мин. Развивается зеленая окраска ![]() жидкости вследствие взаимодействия
рибозы с дефиниламином.
жидкости вследствие взаимодействия
рибозы с дефиниламином.
3. Серебряная проба на пуриновые основания. К 1 мл гидролизата дрожжей приливают 2 капли концентрированного раствора аммиака и 5 капель 1%-ного раствора азотнокислого серебра. Через 3-5 мин выпадает бурый осадок серебряных соединений пуриновых оснований.
4. Молибденовая проба на фосфорную кислоту. К 1 мл гидролизата дрожжей прибавляют 5 капель молибденового реактива и осторожно кипятят несколько минут. Развивается лимонно-желтая окраска жидкости вследствие образования фосфорномолибденовокислого аммония по реакции
H![]() PO
PO![]() + 12 (NH
+ 12 (NH![]() )
)![]() MoO
MoO![]() + 21 HNO
+ 21 HNO![]()
![]() (NH
(NH![]() )
)![]() PO 12 MoO
PO 12 MoO![]() + + 21 NH
+ + 21 NH![]() NO
NO![]() + 12 H
+ 12 H![]() O
O
2.2. Определение нуклеозидфосфатов методом тонкослойной хроматографии
Оборудование и реактивы: СФ; хроматоскоп; весы; рефрижераторная центрифуга; камера для тонкослойной хроматографии; пластинки Silufol uv 254; ножницы; фарфоровые ступки; пробирки; микропипетки; градуированные пипетки на 1 и 2 мл; мерный цилиндр на 100 мл; препаровальная игла. Пропанол; 25%-ный раствор аммиака; жидкий азот; 5%-ный раствор ТХУ кислоты; 0,1 н. HCl; стандартные 0,01 М растворы АТФ, АДФ, АМФ.
Материалы: проростки; ткани животных.
Ход работы
Навеску (0,5 – 1 г) растительной или животной ткани измельчают ножницами на холоду, заливают жидким азотом и растирают в ступке. Затем к растертому порошку приливают 1 мл 5%-ной ТХУ кислоты, перемешивают и центрифугируют 5 мин при 5000 об/мин при 0 - 4° С. Надосадочную жидкость сливают в пробирку, к осадку приливают еще 1 мл 5%-ной ТХУ кислоты, перемешивают и центрифугируют. Супернатанты объединяют и используют для хроматографии. На пластинки Silufol uv 254 в нижней части, отступив 2 см, наносят в виде полосы 0,03 – 0,05 мл насадочной жидкости. После подсыхания ставят в сосуд для восходящей хроматографии. В качестве растворителя используют систему н-пропанол – 25%-ный аммиак – вода (60 : 30 : 10). Время разделения около 2 ч. Затем вынимают хроматографические пластинки, высушивают на воздухе и просматривают в хроматоскопе (светофильтр УФС-1).
Нуклеотиды располагаются в порядке снизу вверх: АТФ, АДФ, АМФ. Зоны, в которых обнаруживаются нуклеотиды, обводят препаровальной иглой, соскабливают в пробирки и экстрагируют 1,8 мл 0,1 н. HCl, интенсивно встряхивают и центрифугируют при 3000 об/мин в течение 5 мин. Надосадочную жидкость фотометрируют в кювете шириной 3 мм при длине волны 257 нм против контроля. Контролем служит соскобленный с пластинки сорбент из золы, не содержащий нуклеотидов; с ним поступают в дальнейшем так же, как с золами, в которых обнаружены нуклеотиды.
Содержание нуклеотидов рассчитывают по калибровочным графикам, составленным для каждого нуклеотида по формуле
C=![]()
где D –
оптическая плотность; В – общий объем экстракта, мл; К – коэффициент экстинкции
(равный для АТФ, АДФ, АМФ соответственно 14,6 10![]() , 15,0 10
, 15,0 10![]() , 14,7 10
, 14,7 10![]() ); А – объем нанесенного экстракта,
мл; n – навеска, г.
); А – объем нанесенного экстракта,
мл; n – навеска, г.
Заключение
В результате выполненной курсовой работы можно сделать вывод, что структурными блоками гигантских молекул нуклеиновых кислот являются нуклеотиды. Каждый нуклеотид содержит три различных компонента: азотистое (пуриновое или пиримидиновое) основание, моносахарид пентозу (рибозу или дезоксирибозу), остаток фосфорной кислоты. Эти компоненты соединены друг с другом в такой последовательности: азотистое основание пентоза — фосфат. Соседние нуклеотиды соединены друг с другом посредством эфирной связи между моносахаридом и фосфатом другого нуклеотида.
Гидролиз нуклеиновых кислот, выделенных из ядер клеток, показал, что они состоят из пуриновых и пиримидиновых оснований (аденина, гуанина, цитозина, тимина), дезоксирибозы и фосфорной кислоты. Эта кислота была названа дезоксирибонуклеиновой (ДНК). Из дрожжей была получена другая нуклеиновая кислота, содержащая вместо дезоксирибозы рибозу. Ее назвали рибонуклеиновой кислотой (РНК). В нее входят основания — аденин, урацил, цитозин и гуанин. ДНК и РНК ответственны за хранение, репликацию (воспроизведение), транскрипцию (перенос) и трансляцию (передачу) генетической (наследственной) информации.
Уникальны биологические функции нуклеотидов. Помимо того, что нуклеотиды входят в состав нуклеиновых кислот, они выполняют важную функцию в энергетическом (фосфорном) обмене, в аккумулировании химической энергии и ее переносе; служат активными простетическими группами в окислительно-восстановительных ферментах, играют важную роль в синтезе жиров, олиго- и полисахаридов.
На основе правил Чаргаффа и данных рентгеноструктурного анализа, Дж. Уотсон и Ф. Крик предложили двухспиральную модель ДНК и развили важную для биохимии концепцию комплементарности. Они предложили три уровня структуры ДНК: первичную (последовательность нуклеотидов), вторичную (структура двух правозакрученных спиралей), третичную (дополнительное закручивание в пространстве двухспиральной молекулы). В образовании вторичной и третичной структур важную роль играют водородные связи, возникающие между парами оснований аденин — тимин и гуанин — цитозин, а также гидрофобные взаимодействия между основаниями, направленные вдоль цепей молекулы ДНК. Разрушение этих связей нагреванием или подщелачиванием растворов вызывает денатурацию ДНК.
Точное копирование молекулы ДНК (ее репликацию) обеспечивает так называемый полуконсервативный механизм, заключающийся в расхождении двух цепей материнской ДНК и использовании их в качестве матриц для синтеза двух новых (дочерних) цепей ДНК, Этот механизм доказан экспериментально.
РНК — однонитевые молекулы, в отличие от ДНК; их вторичная и третичная структуры нерегулярны. По своим биологическим функциям РНК подразделяются на три типа: рибосомная — рРНК, транспортная — тРНК и матричная — мРНК. рРНК входит в состав клеточных органелл — рибосом. Данный тип РНК участвует в формировании структуры рибосом, на которых осуществляется синтез белка. тРНК выполняют функцию переносчика аминокислот к месту синтеза белка. мРНК передает считанную ею информацию с ДНК на синтезируемый белок, выполняет роль матрицы при синтезе полипептидной цепи.
Список использованной литературы
1. Жеребцов Н. А., Попова Т. Н., Артюхов В. Г. Биохимия: Учебник. — Воронеж: Издательство Воронежского государственного университета, 2002.
2. Землянухин А.А. Практикум по биохимии: учебн. пос — Воронеж: Издательство Воронежского государственного университета, 1993.
3. Зенгер В. Принципы структурной организации нуклеиновых кислот. — М: Мир, 1987.
4. Ленинджер А. Основы биохимии: Учебник. — М.: Мир, 1985.
5. Остерман Л. А. Методы исследования белков и нуклеиновых кислот. — М.: Наука, 1981.
6. Плешков Б.П. Биохимия сельскохозяйственных растений: Учебник. — М.: Агропромиздат, 1987.
| Волновой генетический код | |
|
СОДЕРЖАНИЕ Актуальность темы Пересмотр модели генетического кода Расширение модели волнового генетического кодирования Экспериментальные подтверждения ... Точность кодирования последовательностей аминокислот белков в этой модели странным образом уживается с двойной вырожденностью предлагаемого "кода" по линиям избытка транспортных ... Вероятно, процесс естественной эволюции абиогенно возникшего "первичного бульона" из органических молекул - предшественников РНК, ДНК, белков и других существенных компонентов ... |
Раздел: Рефераты по математике Тип: дипломная работа |
| Обнаружение единичных нуклеотидных замен в ДНК: расщепление РНКазой и ... | |
|
Обнаружение единичных нуклеотидных замен в ДНК: расщепление РНКазой и денатурирующий градиентный гель-электрофорез Введение Методы обнаружения ... 2. Гибридизация зонда с комплементарными последовательностями геномных ДНК - Если в гибриднзуемой ДНК имеется замена нуклеотида, образующие РНК-ДНК-дуплексы содержат ... Еще одна проблема, которая возникает при использовании зондов с длиной цепи более 1000 п.и., заключается в том, что под действием РНКазы наряду с расщеплением РНК-ДНК-дуплексов по ... |
Раздел: Рефераты по биологии Тип: учебное пособие |
| Являются ли вирусы живыми организмами | |
|
Можно ли считать вирусы живыми ? Являются ли вирусы живыми ? Согласно Львову, "организм - некая независимая единица интегрированных и взаимосвязанных ... Инфекционные нуклеиновые кислоты, независимо от того выделены ли они из фагов или из вирусов животных или растений, как правило, обладают значительно меньшим инфекционным титром ... Это справедливо как для вирусов с низким содержанием нуклеиновой кислоты, так и для вирусов с высоким содержанием РНК и ДНК. |
Раздел: Рефераты по медицине Тип: дипломная работа |
| Физиология растений | |
|
Куниченко Наталья Александровна, кандидат сельскохозяйственных наук, доцент, заведующая кафедрой защиты растений и экологии Приднестровского ... В РНК входят нуклеотиды А, Г, У и Ц, в состав которых входит рибоза, а в ДНК входят нуклеотиды А, Г, Т и Ц, в состав которых входит дезоксирибоза. В матриксе помимо белков, включающих многочисленные ферменты, катализирующие биохимические реакции цикла Кребса, глиоксилатного цикла, дыхательной цепи, имеются и молекулы РНК и ... |
Раздел: Рефераты по биологии Тип: учебное пособие |
| ДНК. Основы генетического материал | |
|
Челябинский Государственный Университет Юридический факультет Контрольная работа По предмету: "Концепции современного естествознания" На тему: "ДНК ... Белки при этом остаются в осадке; из раствора, содержащего нуклеиновые кислоты и подвергнутого гидролизу 0,3- 1,0 н. щелочью, вызывающей распад РНК до нуклеотидов, ДНК осаждают ... Последовательность нуклоотидов в цепи ДНК переписывается в комплементарную ей последовательность нуклеотидов в молекуле РНК - так называемая транскрипция. |
Раздел: Рефераты по биологии Тип: контрольная работа |