Контрольная работа: Исследование уравнений реакций
1. Рассчитайте молярную массу эквивалентов воды при реакции
а) с металлическим натрием;
б) с оксидом натрия.
Решение:
а) 2Na + 2H2O = 2NaOH + H2h
Из закона эквивалентов:
![]()
![]()
где ne – число отданных Na электронов.
![]()
б) Na2O + H2O = 2NaOH
Из закона эквивалентов:
![]()
![]()
где n – число катионов соответствующих оксиду основания Na2O.
|c.o| – абсолютное значение степени окисления катиона Na
![]()
2. Назовите элементы, внешний энергетический уровень атомов который выражается электронной конфигурацией np4. Напишите полную электронную конфигурацию атома одного из этих элементов и укажите электронное семейство
Решение
Элементы, внешний энергетический уровень атомов которых выражается электронной конфигурацией np4 являются:
Кислород 8 O 2s22p4 1s22s22p4
Сера 16 S 3s23p4 1s22s22p63s23p4
Селен 34 Se 4s24p4 1s22s22p63s23p64s23d104p4
Теллур 52 Te 5s25p4 1s22s22p63s23p64s23d104p65s24d105p4
Полоний 84 Po 6s26p4 1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p4
Все вышеперечисленные элементы принадлежат к p – электронному семейству.
3. Исходя из положения металла в Периодической системе, дайте мотивированный ответ на вопрос: какой из двух гидроксидов является более сильным основанием: а) Mg(OH)2 или Ba(OH)2; б) Ca(OH)2 или Co(OH)2; в) Ca(OH)2 или Zn(OH)2? Напишите уравнения реакций, доказывающих амфотерность гидроксида цинка
Внутри подгруппы с увеличением заряда ядра возрастают металлические свойства и ослабевают неметаллические, следовательно, усиливаются основные свойства их соединений и ослабевают кислотные свойства.
а) В главной подгруппе сверху вниз периодической системы усиливается основной характер гидроксидов: из пары Mg(OH)2 и Ba(OH)2 более сильным основанием будет являться Ba(OH)2;
В периоде с лева на право основной характер гидроксидов постепенно ослабляется, сменяясь амфотерностью к кислотным свойствам внутри периода, т.к. анионам легче присоединять электроны чем отдавать;
б) В паре Ca(OH)2 и Co(OH)2 более сильным будет Ca(OH)2 т. к. элемент кобальт является d-элементом (не заполненный d-подуровень), и будет склонен к комплексообразованию, также они находятся в разных подгруппах;
в) В паре Ca(OH)2 и Zn(OH)2 более сильным основанием будет Ca(OH)2 т.к. находятся в разных подгруппах и цинк будет склонен к комплексообразованию (d-элемент, наличие свободных f-орбиталей)
ZnCl2 +NaOH = Zn(OH)2 +NaCl – cоли цинка взаимодействуют со щелочами образуя гидроксид
Zn(OH)2+HCl=ZnCl2+H2O – гидроксид цинка при взаимодействии с кислотами растворяется образуя соль
Zn+ H2O+2KOH=K2[Zn(OH)4]+H2h – при переизбытке щелочи Zn образует комплексные соединения
Zn +2NaOH = Na2ZnO2 + H2h
Zn+2HCl=ZnCl2+H2h
4. При растворении 16 г. CaC2 в воде выделяется 31,27 кДж теплоты. Определить стандартную энтальпию образования Ca(OH)2
CaC2 кр+ 2H2Oжид = Ca(OH)2кр+ C2H2газh-rHp
1) Рассчитаем сколько количество молей CaC2 прореагировало:
М (CaC2)=64 г/моль
M(CaC2)=16 г
![]()
2) т.е. при взаимодействии 0,25 моля СаС2 выделяется – 31,27 кДж теплоты, а т.к. стандартная энтальпия рассчитывается на 1 моль вещества, то рассчитываем сколько тепла выделится при взаимодействии 1 моля СаС2
0,25 моля выделится – 31,27 кДж теплоты
1,0 моля выделится – х кДж теплоты
![]()
3) исходя из таблицы «стандарт энтальпии образований» находим стандартные энтальпии веществ:
rH(СаС2кр)=-62,7 кДж
rH(H2Oж)=-285,8 кДж
rH(C2H2газ)= 226,8 кДж
4) Исходя из уравнения rHp рассчитывается как:
rHp=∑rH(продуктов) – ∑rH (исходных веществ);
rHp=(rH (Ca(OH)2кр)+ rH(C2H2г)) – (rH(CaC2кр)+2rH(H2Oж)) =>
rHp=rH (Ca(OH)2кр+ rH(C2H2г) – rH(CaC2кр) – 2rH(H2Oж), находим rH (Ca(OH)2кр:
rH (Ca(OH)2кр=rHp – rH(C2H2г) + rH(CaC2кр) + 2rH(H2Oж) подставим значения стандартных энтальпий в уравнение:
rH (Ca(OH)2кр=-125,08 – (226,8)+(-62,7)+2*(-285,8)=-125,08–226,8–62,7–2*285,8= = – 986,18кДж/моль
Ответ: -986,2 кДж/моль
5. При состоянии равновесия системы N2 +3H2 ↔ 2NH3 концентрации веществ были (моль/л): [N2] = 0,3; [H2] = 0,9; [NH3] = 0,4. Рассчитайте, как изменятся скорости прямой и обратной реакции, если давление увеличить в 4 раза. В каком направлении сместится равновесие?
Для решения воспользуемся законом действия масс.
1. Записываем математическое выражение для начальной скорости прямой и обратной реакции
ϑн(п) = k ∗ CN2 ∗ (CH2)3
ϑн(о) = k ∗ (СNH3)2
2. Записываем математическое выражение для конечной скорости прямой обратной реакции (после увеличения давления в 4 раза)
ϑк(п) = k ∗ 4 ∗ CN ∗ (4∗CH2)3 = k ∗ 256 ∗ CN ∗ (CH2)3
ϑк(о) = k ∗ (4∗СNH3)2 = k ∗ 16 ∗ (СNH3)2
3. Найдём отношение скоростей прямой и обратной реакции
ϑк(п) k ∗ 256 ∗ CN ∗ (CH2)3
ϑн(п) k ∗ CN2 ∗ (CH2)3
6. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) BaCO3 и HNO3; б) Fe2(SO4)3 и KOH; в) HCl и K2S; г) CH3COOK и HCl
молекулярный реакция амфотерность уравнение
а) BaCO3 â+ 2HNO3 = Ba(NO3)2 + H2CO3h
BaCO3â+2Н2++2NO3- = Ba2+ +2NO3 – +2H+ + CO32-
BaCO3â= Ba2+ + CO32-
б) Fe2(SO4)3+6KOH=2Fe(OH)3â+3K2SO4
2Fe3+ +3SO42 – +6K+ +6OH – =2Fe(OH)3â+6K+ +3SO42-
2Fe3+ +6OH – =2Fe(OH)3â
в) 2HCl+K2S=H2S+2KCl
2H++2Cl – +2K+ +S2 – =2H+ +S2 – +2K+ +2Cl-
В реакции прореагировали все вещества, но ионная реакция сопровождается образованием газа (сероводорода), тогда:
2HCl+K2S=H2Sh+2KCl
2H++2Cl - +2K+ + S2- = H2Sh +2K+ +2Cl -
2H+ +S2- = H2Sh
г) CH3COOK+HCl=CH3COOH+KCl
CH3COO - + K++H++Cl – =CH3COO - + H++ K+ +Cl –
CH3COO - + K++H++Cl – =CH3COОН + K+ +Cl -, слабый элетролит CH3COОН
CH3COO - + H+ =CH3COОН
7. Чему равна величина ЭДС гальванического элемента, составленного из стандартных цинкового и серебряного электродов, погруженных в растворы их солей? Приведите схему гальванического элемента и реакции, и реакции протекающие на электродах при его работе
Схема гальванического элемента:
(–) Zn | Zn2+ || Ag+ | Ag (+)
На аноде протекают реакции: Zn0-2e=Zn2+
На катоде протекают реакции: Ag++e=Ag0
Т.к. потенциал Е0(Ag)> Е0(Zn)
Е0(Ag+ |Ag)= +0,80В
Е0(Zn2+ | Zn)= -0,763В
то на серебряном электроде будет протекать восстановление (будет являться катодом), а на цинковом электроде будет протекать окисление (он будет анодом);
Потенциал гальванического элемента:
Е = Е0катода – Е0анода =0,80 – (-0,763)=1,562В
Ответ: 1,562 В.
8. Изделие из алюминия склёпано медью. Какой из металлов будет подвергаться коррозии с водородной деполяризацией, если эти металлы попадут в кислую среду (HCl)? Составьте уравнения проходящих при этом процессов, приведите схему образующегося гальванического элемента. Определите продукты коррозии
В реакциях с кислотами атомы алюминия окисляются ионами водорода в ионы алюминия, которые переходят в раствор:
2Al+6H+→2Al3+ +3H2h
Медь в электрохимическом ряду напряжения металлов находится за водородом, (т.е. её стандартный потенциал положительный) и с разбавленными кислотами не реагирует (положительно заряженные ионы меди не переходят в раствор).
В кристаллической решетке меди (в отличие от алюминия) свободные электроны не накапливаются. При соприкосновении этих двух металлов свободные электроны алюминия переходят к меди и восстанавливают на её поверхность ионы водорода:
2H+ +2e→H2h
Продуктами коррозии будет являться результат взаимодействия алюминия с соляной кислотой:
2Al+6HCl→2AlCl3+3H2h
Образуется гальванический элемент:
(–) Al |AlCl3|Cu(+)
Анод катод.
9. При электролизе водных растворов каких из приведённых ниже веществ на катоде выделяется только металл: хлорид бария, хлорид меди (II), иодид калия, нитрат серебра, сульфид натрия? Приведите соответствующие уравнения электродных процессов
При электролизе водных растворов катионов металлов, у которых стандартный электродный потенциал больше чем водорода (Е0>>-0,41В) на катоде восстанавливаются только катионы металлов. В данном случае это хлорид меди (II) и нитрат серебра:
|
(–) Катод
![]()
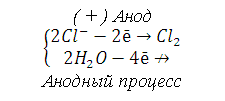
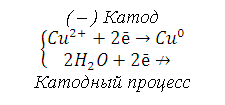
Суммарный процесс электролиза:
![]()
Суммарный процесс электролиза:
![]()
Суммарное молекулярное уравнение электролиза:
![]() .
.
Библиографический список
1. Будякк Е.В. Химия: учеб. пособие Иркутск: Изд-во ИрГТУ, 2008. – 160 с.
2. Коровин Н.В. Общая химия. М. Высш. шк., 2002. 558 с.
3. Кузнецова А.А. Химия: метод. указания по освоению дисциплины для студентов заочной формы обучения. Иркутск: Изд-во ИрГТУ, 2010. 44 с.
4. Химия: метод. указания, программа, решение типовых задач и контрольные задания для студентов заочного обучения технических направлений и специальностей / сост.: В.И. Дударев, В.П. Зуева, О.В. Лебедева, Ю.Н. Пожидаев, З.Н. Топшиноева, А.Н. Шибанова. Иркутск: Изд-во ИрГТУ, 2007. 92 с.
| Химия, элементы таблицы Менделеева | |
|
Седьмая группа периодической системы Из членов данной группы водород был рассмотрен ранее. Непосредственно следующие за ним элементы - F, Сl, Br и I ... Очистка технического алюминия производится обычно при 710-740 °С электролизом в системе из трёх жидких фаз: катодом служит чистый алюминий (плотность 2,35 г/см3), электролитом ... Кристаллические модификации гидроксида алюминия в форме минералов диспора (HAlO2), бемита [AlO(OH)] и гидраргаллита [Al(OH)3] составляет основу природных бокситов. |
Раздел: Рефераты по химии Тип: реферат |
| Изучение и анализ производства медного купороса | |
|
... изучение и анализ производства медного купороса, основанного на переработке отработанного передаточного электролита цеха электролиза меди. В ходе ... Важным видом сырья для получения солей меди является ватержакетная пыль, представляющая собой тонкий порошок и содержащая 0,5 - 5 % Cu в форме сульфида и сульфата, 40 - 50 % Fe, 3 ... При проведении электролиза с растворимым медным анодом в растворе любой соли щелочного металла получающаяся на аноде медная соль, реагируя с образующейся на катоде щелочью, дает ... |
Раздел: Рефераты по химии Тип: дипломная работа |
| Качественный анализ (кислотно-основная классификация) | |
|
... Содержание Аналитические реакции катионов I группы: Lі+, Na+, К+, NH-. 4 Аналитические реакции катионов 2 группы: Ag+, Hg2+, Pb2+ 6 Качественные ... Zn2+ + 2 ОН- = Zn(OH)2 (белый) После растворения гидроксида алюминия и образования гидроксокомплексов алюминия к раствору прибавляют несколько кристаллов соли аммония (NH4C1). |
Раздел: Рефераты по химии Тип: дипломная работа |
| Анализ свариваемости сплавов на основе меди (М1) | |
|
ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ Государственное образовательное учреждение высшего профессионального образования "МАТИ" - Российский ... Важнейшие соединения меди: оксиды Cu2O, CuO, Cu2O3; гидроксид Cu(OH)2, нитрат Cu(NO2)2*3H2O, сульфид CuS, сульфат(медный купорос) CuSO4*5H2O, карбонат CuCO3*Cu(OH)2, хлорид CuCl2 ... 1) К первой группе относятся элементы, растворимые в твердой меди (Al, Fe, Ni, Sn, Zn, Au, Ag, Al, pt, Cd, Sb). |
Раздел: Промышленность, производство Тип: курсовая работа |
| Основы химии | |
|
Глава 1. Общие химические и экологические закономерности. С чего начинается химия? Cложный ли это вопрос? На него каждый ответит по-своему. В середней ... Например, в четвертом периоде за двумя s-элементами (K, Ca) следует 10 d-элементов (от Sc до Zn). Физический смысл константы скорости заключается в том, k равна скорости V, если концентрации реагирующих веществ равны единице [A]a=1 моль/л; [B]в=1 моль/л или [A]a[B]в=1 моль/л ... |
Раздел: Рефераты по химии Тип: реферат |