Реферат: Барий и его соединения
Реферат
Барий и его соединения
Выполнил студент: Глушков А.М
Принял преподаватель:
Красноярск, 2002 г.
Содержание
ВВЕДЕНИЕ. 3
РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. 3
ПОЛУЧЕНИЕ МЕТАЛЛИЧЕСКОГО БАРИЯ.. 4
Термическое разложение гидрида и Ва(NH3)6 6
Электролиз хлорида бария. 6
Очистка. 6
ХИМИЧЕСКИЕ И ФИЗИЧЕСКИЕ СВОЙСТВА.. 6
ПРИМЕНЕНИЕ. 8
СОЕДИНЕНИЯ (ОБЩИЕ СВОЙСТВА) 8
Неорганические соединения. 9
ПОЛУЧЕНИЕ ТИТОНАТА БАРИЯ.. 12
Использование титоната бария в радиоэлектронике. 15
Список использованных источников. 16
ВВЕДЕНИЕ
Тяжелый шпат, BaSO4, был первым известным соединением барин. Его открыл в начале XVII в. итальянский алхимик Касциароло. Он же установил, что этот минерал после сильного нагревания с углем светится в темноте красным светом и дал ему название «ляпис соларис» (солнечный камень).
Окись бария ВаО открыл в 1774 г. Шееле. Он назвал ее «тяжелой землей». В 1797 г., прокаливая нитрат бария, Вокелен получил : окись бария. Карбонат бария был открыт в 1783 г. в Шотландии , и назван «витеритом».
Металлический барий впервые получил Дэви в 1808 г. Название , «барий» происходит от слова «барис» (тяжелый).
РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕВ природе барий встречается в виде соединений (сульфатов, карбонатов, силикатов, алюмосиликатов и т.д.) в различных минералах. Содержание бария в земной коре 0,05 вес. % — больше, чем содержание стронция. Ниже перечислены важнейшие минералы бария:
Барит (персидский шпат), BaSO4, содержит 65,7 Ва0, встречается в виде гранул или бесцветных прозрачных трубчатых кристаллов (иногда окрашенных примесями в желтый, коричневый, красный, серый, голубой, зеленый или черный цвет) с плотностью 4,3—4,7 г/см3 и твердостью 3—3,5 по шкале Mooca. Залежи барита есть в России, США, Франции, Румынии и других странах. В природе встречаются разновидности барита, которые содержат сульфат стронция (баритоцелестин), сульфат свинца и радия.
Барит применяют в химической промышленности для получения солей бария, используемых в пиротехнике, производстве красок и лаков, бумажной промышленности, для приготовления фотобумаги, цементирования рыхлых пород во время бурения нефтяных скважин, защитной облицовки стен рентгеновских камер.
Витерит, ВаСОз, содержит 77,7% Ва0. Встречается в небольших количествах в России, Англии, Японии, США. Это белая масса с сероватым или желтым оттенком; твердость 3—3,5 по шкале Mooca, плотность 4,25—4,35 г/см". Некоторые разновидности витерита содержат карбонат кальция или карбонат стронция (ВаСО3*СаСО3, ВаСО3*SrСО3).
Гиалофан (бариевый полевой шпат) K2Ba[AI2Si4O12], встречается в виде прозрачных бесцветных (или окрашенных примесями в желтый, голубой, красный цвета) моноклинных кристаллов с плотностью 2,6—2,82 г1смР.
Известны также другие минералы бария:
бариевый брюстериг SrBa[Al2Si6O16(OH)2]*3H20, бариевый апатит [Ba10(PO4)6]Cl2, бариевая селитра Ba(NO3)2
Соединения бария найдены во многих силикатных и известняковых породах, подземных и морских, водах, на солнце.
ПОЛУЧЕНИЕ МЕТАЛЛИЧЕСКОГО БАРИЯМеталлический барий получают металлотермическим восстановлением окиси или хлорида бария, термическим разложением гидрида и нитрида бария или Ba(NH.3)e, электролизом расплавленного хлорида бария (смесей BaCl2 и NaCI, BaCI2 и BaF2) или насыщенного раствора BaCI2*H2O на ртутном катоде. Во избежание контактов с воздухом все эти процессы ведут в вакууме или защитной атмосфере. В процессе промышленной переработки барита или витерита получают хлорид или окись бария, из которых металлотермическим восстановлением вырабатывают технический барий (см. схему 1).
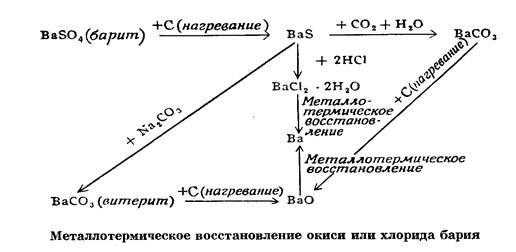
Схема 1 Восстановление окиси или хлорида бария
В промышленности металлический барий получают термическим восстановлением окиси бария порошком металлического алюминия (избыток) при температуре 1200—1250°. Процесс идет в вакууме (0,1 мм рт. ст.).
ЗВаО + 2А1 = ЗВа + Аl2О3 — 25 ккал
Восстановление проводится в кварцевых или герметичных фарфоровых капсулах. После удаления воздуха током водорода в них создается вакуум, затем окись бария и порошок алюминия в течение 2—3 час нагревают при температуре 1250°. По окончании восстановления нагревание прекращают. После охлаждения перед разборкой установки в нее подают сухой воздух.
Силикотермическое восстановление окиси бария проводится в вакууме в стальной трубке (температура 1200°):
ЗВаО + Si = 2Ва + ВаSiO3 — 37 ккал
В процессе магнийтермического восстановления окиси бария в вакууме получается металлический барий. В этом случае образуется промежуточный окисел Ba2O:
2ВаО + Mg = Ba2O + Mg0 Вa2О = Ва0 + Ва
При цинкотермическом восстановлении окиси бария в вакууме образуется сплав цинка и бария.
Металлотермическое восстановление хлорида бария натрием, калием или металлическим цинком в вакууме приводит к образованию сплавов бария с натрием, бария с калием и бария с цинком. Если восстановление хлорида бария идет при нагревании с карбидом кальция CaC2, образуется сплав бария и кальция.
Термическое разложение гидрида и Ва( NH3)6
Термическая вакуумная диссоциация гидрида бария (900—1000°), нитрида Ва3N2 (160—180°) и Ва(NH3)6 (комнатная температура) сопровождается образованием металлического бария.
Электролиз хлорида бария
При электролизе расплавленного хлорида бария (или расплавленной смеси BaCl2— NaCI, BaCl2 — BaF2) с расплавленным свинцовым или оловянным катодом образуются сплавы бария со свинцом или оловом. Во время электролиза насыщенного раствора хлорида бария на ртутном катоде образуется амальгама бария.
Электролитический метод вследствие трудоемкости практически не используется в промышленности.
Очистка
Сырой металлический барий очищают перегонкой в вакууме (1—1,5 мм рт. ст., температура 800°) в аппаратуре, подобной применяемой для очистки магния.
ХИМИЧЕСКИЕ И ФИЗИЧЕСКИЕ СВОЙСТВАБарий — белый серебристый металл с объемно-центрированной кубической решеткой (модификация α-Ва устойчива ниже 375°, модификация β-Ва — от 375 до 710°). Плотность бария 3,74 г1см3, твердость 3 по шкале Мооса (тверже свинца). Ковкий металл. При загрязнении ртутью становится хрупким. Т. пл. 710°, т. кип. 1696°. Соли бария окрашивают пламя газовой горелки в желто-зеленый цвет.
Самый важный радиоактивный изотоп бария — (β- и γ-активный 140Ва — образуется при распаде урана, тория и плутония; период полураспада 13,4 дня. 140Ва извлекают хроматографически из смеси продуктов распада. Распад изотопа 140Ва сопровождается выделением радиоактивного 140La.
При облучении цезия дейтронами образуется ядерный изотоп 133Ва с периодом полураспада 1,77 дней. Со свинцом, никелем, сурьмой, оловом и железом барий образует сплавы.
Барий химически активнее кальция и стронция. Металлический барий хранят в герметичных сосудах под петролейным эфиром или парафиновым маслом. На воздухе металлический барий теряет блеск, покрывается коричневато-желтой, а затем серой пленкой окиси и нитрида:
Ва + 1/202 = Ва0 + 133,1 ккал.
ЗВа +N2 = Ba3N2 + 89,9 ккал
Под действием галогенов металлический барий образует безводные галогениды ВаХ2 (X == F ˉ, С1ˉ , Вг ˉ, I ˉ ). Металлический барий разлагает воду:
Ва + 2Н2О = Ва(ОН)2 + 112 + 92,5 ккал
Растворение металлического бария в жидком аммиаке (—40") сопровождается образованием аммиаката Ba(NH3)6-При обычной температуре барий реагирует с двуокисью углерода:
5Ва + 2C02 = ВаС2 + 4Bа0
Металлический барий — сильный восстановитель. С его помощью при восстановлении хлорида америция (1100°) и фторида кюрия (1300°) были получены элементы америций (N 95) и кюрий (N 96). При высокой температуре барий восстанавливает закись углерода, а выделяющийся свободный углерод реагирует с барием с образованием карбида ВаС2.
Приведенная ниже схема иллюстрирует химическую активность бария.

Растворимые соли бария чрезвычайно ядовиты. Введенный внутривенно хлорид бария мгновенно вызывает смерть. Карбонат и сульфит бария ядовиты, так как они растворяются в соляной кислоте, которая содержится в желудочном соке.
ПРИМЕНЕНИЕМеталлический барий применяется для металлотермического восстановления америция и кюрия, в антифрикционных сплавах на основе свинца, а также в вакуумной технике. Сплавы свинец — барий вытесняют полиграфические сплавы свинец — сурьма.
СОЕДИНЕНИЯ (ОБЩИЕ СВОЙСТВА)Известны многочисленные соединения, в которых барий присутствует в виде двухвалентного катиона. Ион Ва2+ бесцветен, имеет устойчивую восьмиэлектронную конфигурацию. Радиус иона 1,34 А. Он обладает относительно большим объемом и слабо выраженной тенденцией к поляризации, поэтому не образует устойчивых комплексных соединений. Гидроокись Ba(OH)g представляет собой сильное основание.
Неорганические соединения
Гидрид бария, ВаН2, получают нагреванием металлического бария, сплавов кадмий — барий, ртуть — барий или окиси бария в атмосфере водорода:
Ва + Н2 = ВаН2 + 55 ккал Ва0+ 2Н2 = BaH2 + Н2О
BaH2 — серовато-белые кристаллы с плотностью 4,21 г/см3. Выше 675° они подвергаются термической диссоциации. Гидрид бария разлагает воду и взаимодействует с азотом, соляной кислотой и аммиаком.
Гидрид бария применяют в качестве катализатора реакций гидрогенизации.
Окись бария, ВаО, получают непосредственным синтезом из элементов. Кроме того, используют термическое разложение гидроокиси, перекиси, карбоната или нитрата бария. Применяют также прокаливание смеси карбоната бария с углем, сульфата бария с односернистым железом или нагревание сульфида бария с окисью магния и водой.
ВаО представляет собой кубические (решетка типа NaCI) или гексагональные бесцветные кристаллы (или белый аморфный порошок), очень гигроскопичные, с плотностью 5,72 г/см3 (для кубической модификации) и 5,32 г/см3 (для гексагональной) и твердостью 3,3 по шкале Mooca; т. пл. 1923°, т. кип. 2000°. Ва0 люминесцирует под действием ультрафиолетовых лучей и фосфоресцирует в рентгеновских лучах.
Растворяясь в воде, окись бария дает гидроокись бария Ba(OH)2. В отличие от окислов кальция и стронция окись бария при температуре 500° в заметных количествах поглощает двуокись углерода. На холоду окись бария взаимодействует с хлором, а при нагревании — с кислородом, серой, азотом, углеродом, двуокисью серы, сероуглеродом, двуокисью кремния, двуокисью свинца, окисью железа, хрома, а также с солями аммония.
При нагревании окись бария восстанавливается магнием, цинком, алюминием, кремнием и цианидами щелочных металлов.
Окись бария применяют для изготовления стекла, эмалей и термо' катализаторов. В результате замещения в цементе окиси кальция окисью бария получают цементы с исключительной устойчивостью по отношению к воде, содержащей сульфат-ионы.
Перекись бария, ВаО2, получают, сильно прокаливая гидроокись, нитрат или карбонат бария в токе воздуха в присутствии следов воды. Другие способы получения: непосредственный синтез из элементов при нагревании, прокаливание окиси бария с окисью меди, нагревание окиси бария с хлоратом калия, нагревание окиси бария до 350°, дегидратация кристаллогидрата
BaO2*8H2O при 120°:
Ва + 02 = Ва02 + 145,7 ккал Ba0 + СиО = Ва02 + Сu
Ba0 +1/2 02 = Ва02 + 12,1 ккал 3ВаО + КclO3 = ЗВа02 + КСl
Ba02 представляет собой белый парамагнитный порошок с плотностью 4,96 г1см3 и т. пл. 450°. Он разлагается до Ba0 (600°) или до кислорода (795°), устойчив при обычной температуре (может храниться годами), плохо растворяется в воде, спирте и эфире, растворяется в разбавленных кислотах.
Термическое разложение перекиси бария ускоряют окислы - СеО, Cr2O3,
Fe2 O3 и Cu0.
Известны кристаллогидраты BaO2*8H2O и BaO2H2O. Октагид-рат Ba02•H2O получают действием перекиси водорода на баритовую поду в слабощелочных растворах, а также обработкой на холоду раствора хлорида пли гидроокиси бария перекисью натрия:
Ва(ОН)2 + H2O2 + 6H2O = Ва02*8Н2О
BaO2*8H2O выделяется в виде бесцветных гексагональных кристаллов, трудно растворимых в воде, спирте, эфире. Нагретое с перекисью водорода это соединение превращается в желтое вещество — надперекнсь бария ВаО^.
Перекись бария реагирует при нагревании с водородом, серой, углеродом, аммиаком, солями аммония, феррицианидом калия и т. д.
С концентрированной соляной кислотой перекись бария реагирует, выделяя хлор:
ВаO2 + 4НС1конц. = BaCl2 + Cl2 + 2H2O
Перекись бария восстанавливает соли благородных металлов (обладающие малой химической активностью) до соответствующего металла. Перекись бария применяют для получения перекиси водорода, в зажигательных бомбах, а также в качестве катализатора крекинг-процесса.
BaO2•H2O2 представляет собой желтые моноклинные микрокристаллы, устойчивые при 0°, трудно растворимые в обычных растворителях.
Гидроокись бария, Ва(ОН)2, получают действием воды на металлический барий или ВаО. Используют также обработку растворов солей бария (особенно нитрата) щелочами. В промышленности применяют действие перегретого пара на сульфид бария. С этой же целью можно нагреть до 175" (под давлением) метаспликат бария BaSiOs с раствором NaOH. Описан метод, основанный на восстановлении перекиси бария при 550°:
Ba(OH)2— белый порошок с плотностью 4,495 г/см3 и т. пл. 408°. В катодных лучах гидроокись бария фосфоресцирует желто-оранжевым цветом. Растворяется в воде, трудно растворима в ацетоне и метплацетате.
При растворении Ва(ОН)2 в воде получается бесцветный раствор с сильно щелочной реакцией — баритовая вода, которая в присутствии двуокиси углерода быстро покрывается поверхностной пленкой карбоната бария.
Известны кристаллогидраты Ва(ОН)2*8Н2О, Ва(ОН)2*7H2O, Ва(ОН) •2Н2O и Ва(ОН)2*H2O. Кристаллогидрат Ва(ОН)2*8H2O выделяется в виде бесцветных моноклинных призм с плотностью 2,18 г/cм3 и т. пл. 78°. При нагревании до 650° в токе воздуха кристаллогидрат превращается в окись или перекись бария.
Пропускание хлора через баритовую воду сопровождается образованием хлорида, хлората и очень незначительных количеств гино-хлорита бария:
6Ва(ОН)2 + 6CL2 = 5BaCl2 + Ва(ClO3)2 + 6H2О
Баритовая вода реагирует при 100° с сероуглеродом:
2Ва(ОН)2 + CS2 = ВаСО3 + Ba(HS)2 + H2O
Металлический алюминий взаимодействует с баритовой водой с образованием гидроксоалюмината бария и водорода:
2Аl + Ва(ОН)2 + 10H2O = Ba[Al(OH)4(H2O)2]2+3H2
Выше 1000° гидроокись бария подвергается термической диссоциации:
Ва(ОН)2 → ВаО + Н2O
Баритовая вода Ва(ОН)2 применяется в качестве очень чувствительного химического реактива на двуокись углерода.
Фторид бария, BaF2, получают непосредственным синтезом из элементов, действием фтористого водорода на окись, гидроокись, карбонат или хлорид бария, обработкой баритовой воды фтористо-водородной кислотой, обработкой нитрата или хлорида бария фто-ридом натрия или калия, а также сплавленном хлорида магния с фторидом кальция или магния в атмосфере CO2 и термическим разложением гексафторосиликата бария в атмосфере инертного газа.
Бесцветные кубические кристаллы BaF2 имеют решетку типа CaF2 с расстоянием между центром иона Ва2+ и иона Fֿ 2,68 А. Плотность 4,83 г/см3, т.пл. 1280°, т. кип. 2137°. Кристаллы мало растворимы в воде (1,63 г/л при 18°), растворяются в фтористоводо-родной, соляной и азотной кислотах. Применяются для изготовления эмалей и оптических стекол. Температура плавления смеси BaF2*LiF 850°, а смеси BaF2*BaCl2 1010°.
Под титанатом бария понимают соединение BaO-TiO2 , в котором соотношение катионов и анионов может быть различным от BaTiO3 до Ba6Ti17O40, промежуточные вещества – политканаты нестехлометричны и в них могут добавлены вещества, частично замещающие Ba и Ti, то есть проведено легирование.
BaTiO3 имеет структуру неравномерно, а с кубической гране или объёмо-центрированной кристаллической решёткой. Кубическая структура характерна до 120 °C.
При более низких температурах происходит искажения структуры, она переходит в тирагональную, и , возникает деформация кислородной подрешётки, как Ti несколько смещается.
Деформация вызывает поляризацию. Для иона существует 2 энергетически равновесных стабильных положения, симметричных относительно центра. Направление поляризации едино внутри домена так как поляризация возникает без внешнего … поля, то она спонтанная. Внешнее напряжение вызывает упорядочение ориентации диполей. Между поляризацией и напряжённостью поля возникает гистерезисы.
При Т>120°C=Тс
сегнетоэлектрические свойства пропадают из за высоты симметрии кристалла
(кубическая структура). При Т>Тс диэлектрическая проницаемость Еr зависит от
температуры поз Кюри-Вейтса
Хорошие нелигированные вещества BaTiO3 – диэлектрики. С D Е~ 3Эв. И тип энергия активации докоров 0,1 Эв. То есть при номинальной температуре эти носители полностью ионизированы. Кроме легированных элементов роль донора играет кислородные вариации при кислородной мстехлометрии за счёт отчёта.
s =rBaTiO3-1»10ом-1м-1
Nd»5*10^25м-3
Из РЭДС и Холла
Таким образом часть примеси носит акцепторный характер. Акцепторы захватывают электроны и на поверхности кристалита создаётся отрицательный поверхностный заряд. Отрицательный поверхностный заряд вызывает увеличение электростатического потенциала на границе зерна. Удельная проводимость зависит от высоты потенциального барьера С ростом температуры проводимость растёт. Для сохранения электронейтральности образца в приповерхностном слое кристалла возникает положительный пространственный заряд. В том слое, толщиной S подвижных носителей заряда мало и плотность. Пространственный заряда определяется практически только легирующей примесью доноров nD
r =e*nд
Внутри кристалла отсутствуют акцепторы, способные компенсировать доноры.
Если А – площадь приповерхностной области с глубиной ОЗ “S”, то
r*А*S – приграничный “+” ОЗ
N’а – концентрация акцепторов, захвативших электроны, заряд ОПЗ “-” e* N’а
По условию нейтронейтральности
r*А*S- e* N’а=0 ® S=![]() =
=![]()
По уравнению пуассона потенциал ПЗ
Dj =-r /(x r*x 0) так как r=e*nд, a*x? S
j 0=(e/(2*nд*x r*x 0))*(N’a/A)^2
b - константа, связанная с N’a По полученному уравнению с ростом температуры R растёт.
В некотором интервале температур так как при высокой температуре Nа уменьшается из за высвобождения электронов с захваченных по границам зёрнен.
Использование титоната бария в радиоэлектроникеОсобое место среди п/п приборов с aR>0 занимают приборы на основе тинаната бария BaTiO3. В диапазоне ΔT 100 – 150 K они обладают очень высоким ТКС, до 0,3К-1. Термисторы с положительным температурным коэффициентом сопротивления – РТС – термисторы-позисторы.
aR=![]()
![]() >0 – ТКС.
>0 – ТКС.
Термисторы с a>0 называются РТС-термисторами или позисторами. ТКС>0 имеет большиство металлови некоторые поликристаллические п/п
Керамические позисторы имеют ТКС>0 в узком диапазоне температур. Вне этого диапазона их ТКС<0, как у обычных полупроводников.
1. Локшин Э.П., Воскобойников Н.Б. Барий. – Барий и его свойства, изд.КНЦ РАН. - 1996 г. - 168 с.
2. Лебедев В.Н., Локшин Э.П., Маслобоев В.А., Дозорова Р.Б., Михлин Е.Б. Сырьевые источники металлов России и проблемы их вовлечения в переработку // Цветные металлы. - 1997. - №8. - С.46-50.
3. Гуцол А.Ф. Титонат бария // Успехи физ. наук. - 1997. - Т.167. - №6. - С.165-187.
| Аналитический контроль качества титаната бария | |
|
... государственный университет Кафедра аналитической химии Дипломная работа тема: Аналитический контроль качества титаната бария Пермь 2005 Введение Титанилоксалат бария BaC2O4TiO(C2O4) - 4H2O, или BaTiO(C2O4)2 - 4H2O, можно синтезировать взаимодействием хлоридов бария и титана со щавелевой кислотой на холоду или при нагревании ... Титанат бария, высушенный под вакуумом, имел четкую кристаллическую структуру перовскита, не содержащую карбоната бария. |
Раздел: Рефераты по химии Тип: дипломная работа |
| Химия, элементы таблицы Менделеева | |
|
Седьмая группа периодической системы Из членов данной группы водород был рассмотрен ранее. Непосредственно следующие за ним элементы - F, Сl, Br и I ... Эту группировку содержат зелёные кристаллы, выделяющиеся из раствора в HCl продукта восстановления ЭCl5 металлическим свинцом при 600 °С. Состав этих кристаллов - Э6Cl12-2HCl-7H2O ... Для получения небольших количеств этих металлов удобно пользоваться нагреванием в вакууме их хлоридов с металлическим кальцием. |
Раздел: Рефераты по химии Тип: реферат |
| Кристаллы в природе | |
|
Содержание ВВЕДЕНИЕ 3 Тепловые и механические свойства твёрдых тел I. Симметрия кристаллов 1.1 Как растут кристаллы 5 1.2 Идеальная форма кристаллов 7 ... В 1824 году ученик великого Гаусса, профессор физики во Фрайбурге Л.А.Зеебер для объяснения расширения кристаллов при нагревании предложил заменить многогранники Гаюи их центрами ... По характеру сил, которые действуют между частицами, находящимися в узлах решётки кристалла, различают четыре типичные кристаллические структуры: ионную, атомную, молекулярную и ... |
Раздел: Рефераты по физике Тип: реферат |
| Галлий и его соединения | |
|
ДОНЕЦКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ КАФЕДРА ПРИКЛАДНОЙ ЭКОЛОГИИ И ОХРАНЫ ОКРУЖАЮЩЕЙ СРЕДЫ КУРСОВАЯ РАБОТА по химии ТЕМА: Галлий и его ... Низший окисел галлия Ga2O можно получать нагреванием металла в разреженной атмосфере углекислого газа или водяного пара, а также восстановлением окиси галлия (лучше всего ... При нагревании до 200 C они частично дегидратируются без нарушения структуры, а при более высоких температурах разлагаются с образованием смеси окиси галлия и карбоната щелочного ... |
Раздел: Рефераты по химии Тип: реферат |
| Общая и неорганическая химия | |
|
Квантово-механическая модель атома. Квантовые числа. Атомные орбитали. Порядок заполнения орбиталей электронами Теория строения атома основана на ... Метод основан на неодинаковой растворимости хлоридов, гидроокисей, карбонатов и сульфидов металлов. При нагревании воды с высокой щелочностью происходит гидролиз карбоната магния с образованием труднорастворимого соединения гидроокиси магния: |
Раздел: Рефераты по химии Тип: учебное пособие |