Реферат: Белки, их строение и состав
Магнитогорский Лицей Российской Академии наук
реферат по химии
на тему:
“Белки.
Их строение и состав”
Составил _________________ Григоренко М.
ПБС-1-95
Магнитогорск 1997

оглавление
ОГЛАВЛЕНИЕ_________________________________________________________ 1
БЕЛКИ________________________________________________________________ 3
СТРУКТУРА БЕЛКОВ__________________________________________________ 5
ФИЗИЧЕСКИЕ СВОЙСТВА_____________________________________________ 7
ХИМИЧЕСКИЕ СВОЙСТВА____________________________________________ 7
СИНТЕЗ БЕЛКОВ______________________________________________________ 8
Литература:___________________________________________________________ 8
белки
| Б |
ЕЛКИ — это азотсодержащие высокомолекулярные органические вещества со сложным составом и строением молекул.
Белок можно рассматривать как сложный полимер аминокислот.
Белки входят в состав всех живых организмов, но особо важную роль они играют в животных организмах, которые состоят из тех или иных форм белков (мышцы, покровные ткани, внутренние органы, хрящи, кровь).
Растения синтезируют белки (и их составные части a-аминокислоты) из углекислого газа СО2 и воды Н2О за счет фотосинтеза, усваивая остальные элементы белков (азот N, фосфор Р, серу S, железо Fe, магний Mg) из растворимых солей, находящихся в почве.
Животные организмы в основном получают готовые аминокислоты с пищей и на их базе строят белки своей организма. Ряд аминокислот (заменимые аминокислоты) могут синтезироваться непосредственно животными организмами.
Характерной особенностью белков является их многообразие, связанное с количеством, свойствами и способах соединения входящих в их молекулу аминокислот. Белки выполняют функцию биокатализаторов — ферментов, регулирующих скорость и направление химических реакций в организме. В комплексе с нуклеиновыми кислотами обеспечивают функции роста и передачи наследственных признаков, являются структурной основой мышц и осуществляют мышечное сокращение.
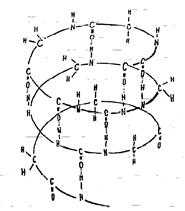
В молекулах белков содержатся повторяющиеся амидные связи С(0)—NH, названные пептидными (теория русского биохимика А.Я.Данилевского).
Таким образом, белок представляет собой полипептид, содержащий сотни или тысячи аминокислотных звеньев.
Структура белков
| О |
|
|
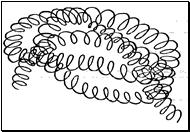
собый характер белка каждого вида связан не только с длиной, составом и строением входящих в его молекулу полипептидных цепей, но и с тем, как эти цепи ориентируются.
В структуре любого белка существует несколько степеней организации:
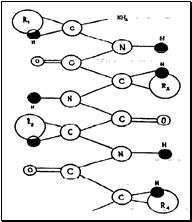
1. Первичная структура белка — специфическая последовательность аминокислот в полипептидной цепи.
|
|
|
|
2.
|
3.
|
· дисульфидный мостик (-S-S-) между атомами серы,
· сложноэфирный мостик – между карбоксильной группой (-СО-) и гидроксильной (-ОН),
· солевой мостик - между карбоксильной (-СО-) и аминогруппами (NH2).
|
|
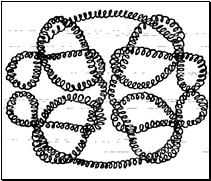
4. Четвертичная структура белка — тип взаимодействия между несколькими полипептидными цепями.
|
Физические свойства
| Б |
елки имеют большую молекулярную массу ( 104—107), многие белки растворимы в воде, но образуют, как правило, коллоидные растворы, из которых выпадают при увеличении концентрации неорганических солей, добавлении солей тяжелых металлов, органических растворителей или при нагревании (денатурация).
Химические свойства1. Денатурация — разрушение вторичной и третичной структуры белка.
2. Качественные реакции на белок:
n биуретовая реакция: фиолетовое окрашивание при обработке солями меди в щелочной среде (дают все белки),
n ксантопротеиновая реакция: желтое окрашивание при действии концентрированной азотной кислоты, переходящее в оранжевое под действием аммиака (дают не все белки),
n выпадение черного осадка (содержащего серу) при добавлении ацетата свинца (II), гидроксида натрия и нагревании.
3. Гидролиз белков — при нагревании в щелочном или кислом растворе с образованием аминокислот.
Синтез белковБелок — сложная молекула, и синтез его представляется трудной задачей. В настоящее время разработано много методов прекращения [ГМВ1] a-аминокислот в пептиды и синтезированы простейшие природные белки — инсулин, рибонуклеаза и др.
Большая заслуга в создании микробиологической промышленности по производству искусственных пищевых продуктов принадлежит советскому ученому А.Н.Несмеянову.
Литература:Справочник школьника
“ХИМИЯ” М.,”СЛОВО” 1995.
Г.Е.Рудзитис, Ф.Г.Фельдман
“Химия 11. Органическая химия”
М., “Просвещение”,1993.
А.И.Артеменко, И.В. Тикунова
“Химия 10-11. Органическая химия”
М., “Просвещение” 1993.