Статья: Синтез и исследование моно- и диамидов тиодигликолевой кислоты как возможных ингибиторов коррозии железа
В.А. Мухин, M.B. Mухина, Т.В. Яцкевич, Омский государственный университет, кафедра неорганической химии
Существенное влияние на скорость растворения железа в кислых средах оказывают многие органические соединения, в том числе и тиодигликоль [1,2]. Основываясь на определенной структурной аналогии между тиодигликолем S(CH2CH2OH)2 и тиодигликолевой кислотой S(CH2COOH)2, можно было предположить, что тиодигликолевая кислота (ТДГК) и ее азотсодержащие производные тоже будут оказывать влияние на растворение железа в кислой среде.
Исследования показали [3], что ТДГК, ее ангидрид, дигидразид, эфир действительно ускоряют растворение железа в 1 н серной кислоте и могут использоваться в процессах травления. Продолжая начатые исследования, казалось интересным расширить круг производных ТДГК с целью изыскания cреди них возможных ингибиторов и стимуляторов коррозии металлов.
Для этого были взяты моно- и диамиды на основе ТДГК и различных аминов. Сама ТДГК была получена реакцией монохлорацетата с сероводородом [4]. Моноамиды синтезировали исходя из аминов и ангидрида ТДГК, полученного, в свою очередь, кипячением ТДГК в среде хлористого ацетила по схеме:
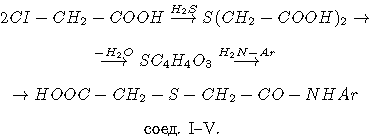
Синтез диамидов ТДГК (соединения V-X) осуществляли из дихлорангидрида ТДГК и тех же аминов:
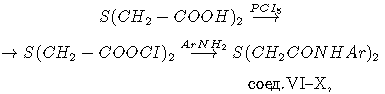
где Аr- фенил, 4-дифенил, alpha- и beta-нафтил, 2-флуоренил. Характеристика соединений приведена в табл. 1 и 2.
Моноамиды и диамиды ТДГК - соединения, плохо растворимые в воде при комнатной температуре, поэтому для испытаний их приходилось растворять в малых объемах органических растворителей (диоксан, диметилформамид), и этот раствор в качестве ингибитора вводить в 0,1 н серную кислоту. К тому же можно было надеяться, что малые дозы органических растворителей усилят защитные свойства ингибиторов, вызывая эффект синергизма [6].
Изучение предполагаемых ингибиторов проводили методом поляризационного
сопротивления [7,8] на приборе Р-5035 при температуре ![]() oC течение 2 ч.
Величина электродного потенциала железа измерялась с помощью прибора рН-340 с хлорсеребряным
электродом сравнения. Измеренное значение поляризационного сопротивления Rin усредняли
из пяти параллельных опытов и сравнивали со значением Ron в кислоте без ингибитора.Вычисляли
коэффициент торможения
oC течение 2 ч.
Величина электродного потенциала железа измерялась с помощью прибора рН-340 с хлорсеребряным
электродом сравнения. Измеренное значение поляризационного сопротивления Rin усредняли
из пяти параллельных опытов и сравнивали со значением Ron в кислоте без ингибитора.Вычисляли
коэффициент торможения ![]() , который показывает,
, который показывает,
Таблица I
Моноамиды тиодигликолевой кислоты HOOC-CH2-S-CH2-CONHAr (соед. I-V)
| Вещество | Ar |
Выход, % |
Tпл oC (р-ль для крист.) |
Формула | Найдено, % | Вычислено, % | ||||||
| C | H | N | S | C | H | N | S | |||||
| I | фенил | 85 | 101-103 (a) | C10H11NO3S | 14,02 | 14,22 | ||||||
| II | 4-дифенил | 87 | 167-168 (a) | C16H14NO3S | 64,66 | 5,16 | 4,62 | 10,73 | 64,16 | 4,71 | 4,68 | 10,70 |
| III |
|
83 | 157-158 (a) | C14H13NO3S | 60,50 | 4,78 | 5,22 | 11,76 | 61,06 | 4,76 | 5,09 | 11,64 |
| IV |
|
80 | 113-114 (a) | C14H13NO3S | 60,75 | 4,86 | 5,25 | 11,70 | 61,06 | 4,76 | 5,09 | 11,64 |
| V | 2-флуоренил | 91 | 159-160 (б) | C17H15NO3S | 65,34 | 4,91 | 4,36 | 10,25 | 65,15 | 4,82 | 4,48 | 10,23 |
Таблица 2
Диамиды тиодигликолевой кислоты S(CH2CONHAr)2 (соед. VI-X)
| Соединение | Ar |
Выход, % |
Tпл oC (р-ль для кристалл.) |
Формула | Найдено, % | Вычислено, % | ||
| N | S | N | S | |||||
| VI | фенил | 90 | 167,168 [5] | |||||
| VII | 4-дифенил | 80 | 234-235 (ДМФА) | C28H24N2O2S | 6,24 | 6,94 | 6,19 | 7,08 |
| VIII |
|
79 | 192-193 (б) | C24H20N2O2S | 6,87 | 8,74 | 6,99 | 8,004 |
| IX |
|
75 | 202-203 (б) | C24H20N2O2S | 6,40 | 8,17 | 6,99 | 8,004 |
| X | 2-флуоренил | 82 | 255-256 (разл.) | C30H24N2O2S | 5,53 | 5,88 |
ДМФА-диметилформамид; а-вода; б-спирт+вода.
Таблица 3
Значения коэффициента торможения коррозии ![]()
для моно- и диамидов ТДГК
| Соединение | Ar |
Моноамиды
|
Диамиды
|
| I, VI | фенил | 5,30 | 7,30 |
| II, VII | 4-дифенил | 6,40 | 1,96 |
| III, VIII |
|
7,90 | 0.99 |
| IV, IX |
|
12,10 | 2,90 |
| V, X | 2-флуоренил | 6,80 | 7,40 |
во сколько раз замедляется скорость коррозии. Результаты представлены в табл.3.
Среди моноамидов ТДГК, хорошо растворимых в смеси диоксан-кислота, наибольший эффект показало соединение IV (Y=12,1).Следует отметить, что сами растворители незначительно замедляют коррозию. Коэффициент торможения для диоксана составляет 1,6.
Если принять адсорбционный механизм действия ингибиторов, то станет понятным, почему диамиды ТДГК дают сравнительно низкий коэффициент торможения (Y=7,4 для соединения X). Они плохо растворимы и даже в смесях с органическими растворителями образуют лишь коллоидную взвесь. Моноамиды в условиях испытаний, вероятно, при диссоциации отщепляют крупные анионы, адсорбирующиеся на поверхности железа (которая при стационарном потенциале заряжена положительно), обеспечивая ингибирующий эффект.
Список литературы
Путилова И.Н., Балезин С.А., Баранник В.П. Ингибиторы коррозии металлов. М.: Госхимиздат, 1958. С.62.
Makrides A., Hackreman N. Industr. and Eng. Chem. 1955. Т.47. С.1173.
Мухин В.А., Мухина М.В. Стимуляторы растворения железа на основе тиодигликолевой кислоты. Защита металлов. 1978. Т.14. N 2. С.191.
Мухина М.В., Цеханович Е.Ю., Постовский И.Я. Ди-(карбогидразидометил)-сульфид, соответствующие ему сульфоксид, сульфон и их производные // Изв. высш. учеб. завед. Сер."Химия и хим. технология". 1966. N 4. С.586.
Anschutz R., Biernaux F. Ann. 1893. Т. 273. С.69.
Иванов Е.С., Егоров В.В. Исследование влияния малых добавок органических растворителей на эффективность ингибиторов // Реферативный научно-технический сборник. Сер. "Коррозия и защита в нефтегазовой промышленности". М.: 1982. Вып.10. С.10.
Антропов Л.И., Бабенков В.М., Будницкая Е.А. и др. Измеритель скорости коррозии Р-5035 // Защита металлов. 1976. Т.12. N 2. С.234.
Антропов Л.И., Герасименко Ю.С. Определение скорости коррозии и эффективности ингибиторов методом поляризационного сопротивления // Защита металлов. 1966. Т.2. N 2. С.115.