Статья: Исследование влияния солевого состава пластовых вод и малых добавок неэлектролитов на дисперсность водо-нефтяных эмульсий
Ергин Ю.В., Кострова Л.И., Кузнецова Н.В.
Добываемая на промыслах нефть практически всегда представляет собой водо-нефтяную (в/н) эмульсию, содержание воды в которой определяется в первую очередь продолжительностью эксплуатации данного месторождения. В значительной степени это связано с тем, что для поддержания в нефтяной залежи пластового давления используются различные методы заводнения продуктивных пластов. Для заводнения применяют как воды поверхностных водоемов, так и воды глубинных горизонтов, химический состав которых может значительно отличаться от пластовой воды, добываемой с нефтью. Для повышения нефтеотдачи пластов широко используют различные методы воздействия на залежь специальными химическими реагентами (полимеры, поверхностно-активные вещества, мицеллярные растворы и др.).
В то время, как действие природных и искусственных деэмульгаторов на свойства в/н эмульсий и процессы вытеснения нефти из пласта изучены достаточно подробно [1-3], исследованию влияния солевого состава пластовых вод, различных химических реагентов, хорошо растворимых в воде, на свойства эмульсий, образующихся в процессе вытеснения нефти закачиваемыми в пласт водами, внимания практически не уделялось. Цель настоящей работы состоит хотя бы в частичном восполнении этого пробела.
С помощью автоматических магнитных весов [4, 5] методом седиментационного анализа исследовались кривые g(r) распределения глобул воды в 5% в/н эмульсиях, приготовленных механическим перемешиванием безводной нефти Сергиевского месторождения РБ, поверхностно-активного вещества (дисольван 4411 из расчета 0,02 кг/т нефти), пресной и пластовой вод, в которых растворялись различные соли и неэлектролиты.
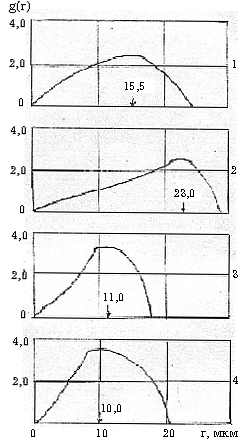
Сравнение вида кривых g(r) и величин средних размеров глобул воды в эмульсиях, приготовленных на основе 1N-водных растворов электролитов с соответствующей кривой и средними размерами глобул в эмульсии с пресной водой (табл. 1, рис. 1) показывает, что их можно разделить на две группы. К первой относятся эмульсии, образованные водными растворами хлоридов щелочно-земельных металлов, хлоридом натрия, а также сульфатами аммония, магния и гидрокарбоната натрия. Средние размеры глобул воды в них меньше, чем в эмульсиях на основе пресной воды (rпресн=15,5 нм).
Таблица 1. Средние размеры глобул воды в 5% в/н эмульсиях в зависимости от электролита.
| Электролит | MgCl2 | CаCl2 | SrCl2 | BaCl2 | NaCl | KCl | KBr |
| r, мкм | 10,0 | 9,5 | 13,0 | 15,0 | 12,0 | 15,3 | 21,0 |
| Электролит | KJ | (NH4)2SO4 | MgSO4 | NaHCO3 | NaNO3 | KNO3 |
| r, мкм | 25,0 | 4,3 | 10,5 | 10,5 | 16,5 | 21,0 |

Рис 1. Кривые распределения g(r) глобул воды в 5% в/н эмульсиях, приготовленных на основе IN-растворов электролитов: 1 - NaCl, 2 - KCl, 3 - KBr, 4 - Kl, 5 - MgCl2, 6 - CaCl2, 7 - SrCL2, 8 - BaCl2 , 9 - (NH4)2SO4, 10 - MgSO4, 11 - NaHCO3, 12 - NaNO3, 13 - KNO3, а также пресной (14) и пластовой (15) воды.
Ко второй группе относятся эмульсии, образованные водными растворами галогенидов калия, а также азотнокислым натрием и калием. Средние размеры глобул воды в них больше, чем в эмульсии, приготовленной на основе пресной воды. К этой же группе относится эмульсия на основе пластовой воды, причем средние размеры глобул воды (rпласт=30,0 мкм) в этом случае максимальны.
Полученные результаты находятся в соответствии с представлениями о структурных изменениях, происходящих в воде при растворении в ней электролитов. Электролиты, образующие эмульсии первой группы, по знаку интегральных теплот растворения относятся к типу электролитов, растворяющихся с выделением тепла, а электролиты, образующие эмульсии второй группы, растворяются с поглощением тепла [6, 7].
Более тонкое проявление изменений состояния воды в эмульсиях становится понятным при рассмотрении не суммарного действия электролита, а аниона и катиона в отдельности. По О.Я.Самойлову [8, 9] следует различать случаи положительно и отрицательно гидратирующихся ионов. Первый из них соответствует эффективному связыванию ионами ближайших к ним молекул воды раствора (из исследуемых нами это ионы Na+, Mg2+, Ca2+, Sr2+, Ba2+, HCO3-, SO42-). Во втором случае (из исследуемых нами это ионы Cl-, Br-, J-, NH4-, NO3-) ближайшие к иону молекулы воды раствора более подвижны, чем в свободной воде. Суммарно структурное действие электролита определяется знаками и величинами энергий ближней гидратации соответствующей пары аниона и катиона [5, 9], что полностью объясняет обнаруженный нами характер изменения кривых g(r) и величин средних размеров глобул воды в эмульсиях на основе всех исследованных электролитов.
В качества добавок (4,66 % мол.) неэлектролитов (“стабилизирующих” и “разрушающих” структуру воды) мы использовали гексаметилфосфортриамид (ГМФТ), карбамид (мочевину) и ацетамид. Введение двух первых из них приводит к некоторому уменьшению средних размеров глобул воды в эмульсии по сравнению с размерами глобул воды в эмульсиях на основе как пресной, так и пластовой воды. Ацетамид, наоборот, влияет на размеры глобул воды в эмульсиях в противоположную сторону (рис. 2, 3).
|
Рис. 2. Кривые распределения g(r) глобул воды в 5% в/н эмульсиях, приготовленных на основе пресной воды (1) и с добавлением (4,66 % мол.) неэлектролитов: 2 - ацетамида, 3 - ГМФТ, 4 - карбамида. |
Рис. 3. Кривые распределения g(r) глобул воды в 5% в/н эмульсиях, приготовленных на основе пластовой воды (1) и с добавлением (4,66 % мол.) неэлектролитов: 2 - ацетамида, 3 - ГМФТ, 4 - карбамида. |
Введение в пресную воду полиакриламида (ПАА) показывает, что размеры глобул воды по сравнению с контрольным опытом сначала уменьшаются (при концентрациях 0,01-0,04 % весового ПАА в пересчете на чистый полиакриламид), а затем увеличиваются и становятся больше, чем в пресной воде. Максимальные размеры глобул достигаются при концентрации в воде ~0,08 % вес. ПАА. При дальнейшем увеличении концентрации полиакриламида размеры глобул воды в эмульсиях практически не изменяются. Эта концентрация ПАА, кстати, соответствует промысловой концентрации, характерной наиболее эффективному вытеснению нефти из пласта.
Список литературы
Бабалян Г.А. Физико-химические процессы в добыче нефти. М.: Недра, 1974.
Шерман Ф. (ред.). Эмульсии. Л.: Химия, 1972.
Григоращенко Г.И., Зайцев Ю.В., Кукин В.В. и др. Применение полимеров в добыче нефти. М.: Недра, 1973.
Ергин Ю.В., Яруллин К.С. Магнитные свойства нефтей. М.: Наука, 1979.
Ергин Ю.В. Магнитные свойства и структура растворов электролитов. М.: Наука, 1983.
Мищенко К.П., Полторацкий Г.М. Вопросы термодинамики и строения водных и неводных растворов электролитов. Л.: Химия, 1968.
Крестов Г.А. Термодинамика ионных процессов в растворах. Л.: Химия, 1973.
Самойлов О.Я. Структура водных растворов электролитов и гидратация ионов. М.: Изд. АН СССР, 1957.
Samoilow O.Ya. In: Water and Aqueons Solutions / Ed. Horne R.A. N-Y: I.Willey and Sons, Inc., 1972. P. 597-610.