Реферат: Роль многократной ионизации в действии излучения
Введение. Шестнадцать лет назад Платцман блестяще рассмотрел вопрос о возможной роли многократной ионизации в действии излучения. К сожалению, к проблеме изучения действительной роли, которую играет переданная энергия, вызывающая образование многократно заряженных ионов, приступить очень трудно и она остается довольно неясной.
Механизмы ионизации. Существуют различные процессы, которые могут привести к образованию многократно заряженных ионов. В этом обзоре мы не будем обсуждать такие процессы, как одновременный электронный захват и ионизацию «тяжелыми» положительными частицами (см., например, [2], а также следующую статью Кистемейкера), ионизацию при мезонном захвате [3] и т. д. Блестящий анализ ионизации, связанной с различными процессами ядерного распада, был недавно опубликован Вексле-ром [4].
Мы обсудим здесь кратко многократную ионизацию, обусловленную смежными ионизациями, и многократное испускание слабо связанных электронов по существу в «одном акте». Основная часть настоящей статьи будет посвящена многократной ионизации, связанной с первоначальной ионизацией внутренних оболочек.
Смежные ионизации. Гипотеза, согласно которой определенный тип эффектов облучения может обусловливаться смежными ионизациями, не нова. Напомним модель Ли — Кэтчесайда (представляющую интерес хотя бы с исторической точки зрения [5]), согласно которой каждая ионизирующая частица, которая пересекает хроматиду в традесканции, может с большой вероятностью разрушить ее только в том случае, если в пределах диаметра хро-матиды эта частица производит 15—20 актов ионизации. Аналогично в ранних попытках объяснить радиационные повреждения сухих белков, исходя из предположения о «прямом действии», допускалось, что для инактивации одной молекулы иногда необходимо, чтобы при прохождении одной частицы наступало несколько ионизации [6]. Па основании этих рассуждений, а также анализа более общей модели Ховарда-Фландерса [7], были выполнены расчеты вероятности того, что в пределах данного расстояния образуется некоторое число ионов, причем допускались статистические флуктуации как чдсдз ионных скорлений, так и числа ионов в каждом из них [8]. Эти расчеты, основанные на данных об ионизации газа, следует, однако, пересмотреть, чтобы учесть прогресс наших знаний о характеристических потерях энергии электронами в конденсированных средах [9]. Согласно гипотезе Хатчинсона, на одну первичную ионизацию требуется меньшая энергия, чем обычно считалось [10], т. е. для инактивации ферментов, облучаемых в сухом состоянии в отсутствие кислорода (но не в его присутствии), требуется, как правило, многократная ионизация. Наконец, механизм инактивации, предложенный Плат-цманом и Франком и заключающийся в разрыве вторичных связей волной поляризации, предполагает необходимость небольшого числа ионизации в самой молекуле белка или вблизи нее [11].
По-видимому, вопрос о пространственных корреляциях возникших зарядов относится к важным. Количественные характеристики ионных скоплений еще не установлены. Кроме того, не существует резкого экспериментального различия между «смежными ионизациями» и состоянием, возникающим при различных видах многократной ионизации, обсуждаемых ниже.
«Одноактное» испускание внешних электронов. Для физиков-экспериментаторов и теоретиков объяснение «одноактного» испускания двух или большего числа слабо связанных атомных или молекулярных электронов под действием, скажем, удара электрона до сих пор представляется очень сложным.
К счастью, возможные детали механизма многократного испускания слабо связанных электронов для наших целей имеют лишь второстепенный интерес. К сожалению, эмпирические данные о вероятности (сечении) тг-кратной ионизации (п ]> 2) до сих пор чрезвычайно скудны [12, 13]. Однако основная масса «вторичных» электронов, создаваемых высокоэнергетическим излучением, имеет энергию, при которой сечение даже наиболее вероятной двукратной ионизации мало. Поэтому при обычных условиях облучения значение полного выхода такой двукратной ионизации в 103 раз меньше значения выхода для однократных ионизации [1]. Кроме того, химическая активность этих двукратно ионизированных атомов не должна быть особенно большой. Аналогичной ионизацией более высокой кратности можно полностью пренебречь. Что же касается первичных ионизации, то в некоторых атомарных газах около 10% всех ионизации, создаваемых электронами средней энергии, могут оказаться двукратными и около 1% —трехкратными [12, 13].
Внутриоболочечная ионизация. Общие соображения. Особенный интерес представляет механизм многократной ионизации с потерей электронов внутренними, глубоколежащими оболочками, за которой следует — вероятно, через 10~14 — 10~15 сек — эмиссия других электронов с последующей перестройкой атомного или молекулярного электронного облака. Этот механизм предполагает выделение болыноц порции энергии, способной вызвать
сильные локальные нарушения и затем быстро преобразоваться в потенциальную энергию молекулы. Даже в кислороде— легком атомо — по крайней мере 530 эв остается в ионе при испускании одного K-электрона, что более чем в 10 раз превышает энергию, необходимую для удаления двух валентных электронов.
Сечения однократной внутриоболочечной ионизации можно довольно точно вычислить из теории. Число первичных двукратных или многократных внутриоболочечных ионизации очень мало. (Даже если эти ионизации маловероятны, они сыграли известную роль в интерпретации Kα-сателлитов в рентгеновском спектре [14].) Теоретический выход внутриоболочечной ионизации в реальных условиях облучения был получен Дурупом и Платцмашш [15, 10] путем расчета сечений с использованием теории Спенсера и Фано [17]. Наконец, процессы, вызываемые образованием внутриоболочечных вакансий, интенсивно изучались как физиками, так и химиками, занимающимися ядерной химией [4, 18].
Процессы, непосредственно следующие за образованием внутриоболочечных вакансий.
Изолированные атомы. В тяжелом атоме, электроны которого располагаются на многочисленных оболочках и подоболочках (энергетических уровнях), перестройка может происходить громадным числом способов, в том числе путем как радиационных, так и нсрадиационных переходов, причем последние могут вызывать значительную потерю электронов. Образование внутриоболочечной вакансии в атоме Хе (Z — 54) иногда сопровождается ливнем, состоящим из более чем 20 электронов [19], а наиболее вероятное их число равно 8 [19, 201 (см. также [13]). Этот процесс представляет собой каскад простых переходов Оже, в'каждом из которых один электрон переходит на внутреннюю орбиту, а энергия перехода идет на выбивание другого электрона.
Однако такая картина формирования заряда не полна. В основном закопченная картина была недавно создана Карлсоном и Краузе [21] для простейшего случая атома Ne (Z = 10), т. е. легкого атома, подвергнутого рентгеновскому облучению. Некоторые основные ее особенности заключаются в следующем.
а) В тот момент, когда быстрый фотоэлектрон вылетает из K-оболочки Ne, поле, в котором движутся оставшиеся электроны, претерпевает внезапное возмущение, приводящее к «выбросу» одного или нескольких электронов примерно в 16% случаев.
б) Вероятность последующего процесса Оже, в котором испускается два электрона (или большее их число), равна приблизительно 8% («двойной» процесс Оже может иметь ту же природу, что и в пункте а) [22].
Если бы не было таких механизмов эмиссии добавочных электронов, следовало бы предсказать только образование Ne1+ (вакансия в k-оболочке заполнена в результате радиационного перехода) и Ne2+ (простой переход Оже), Однако на самом деле наблюдается около 22% Ne3+, около 3% Ne4+ и 0,3% Ne6+. Сходная ситуация должна наблюдаться для атомов О, N и С [20].
Изучался также случай не столь легкого атома Аг (Z = 18) [13, 23]. Полученные результаты можно в известном приближении применить к таким биологически важным атомам, как S (Z = 16) и Р (Z = 15) [20]. При К-ионизации аргона примерно в 40% случаев теряется пять электронов или более; наиболее вероятна потеря четырех электронов. Что касается количества выделившейся энергии, то при К-ионизации ее величина в Аг, S и Р равна соответственно 3,2, 2,5 и 2,1 кэв [24]. В этих атомах ионизация L-оболочки также сопровождается (≈ 100%) одним или несколькими процессами Оже, иногда комбинированными с «выбросом» электрона. Таким образом, в Аr вероятность ионизации L-оболочки, приводящей к образованию ионов с зарядом три и больше, превосходит 40%. Ионизация L-оболочки падающей частицей обычно значительно более вероятна, чем ионизация .К-оболочки; исключением служит фотоэлектрический эффект при энергиях фотона, превышающих порог ионизации К-оболочки. Энергии ионизации L-оболочки, конечно, меньше и равны 290—245 эв, 190—163 эв и 150—128 эв для Аr, S и Р соответственно [24].
Исследования, проведенные с помощью рентгеновского облучения, дали возможность установить эмпирические правила, посредством которых можно оценить средний заряд, возникающий при образовании вакансий в результате атомной перестройки в любой оболочке любого изолированного атома [20].
Изолированные молекулы. Можно ожидать, что в молекулах во время конечных стадий перестройки будет осуществляться быстрый внутримолекулярный перенос заряда. Давно известно, что в случаях, когда внутренние вакансии создаются включенными в молекулу радиоактивными ядрами [4], в ней могут произойти сильные нарушения. Более точная информация была недавно получена в исследованиях Карлсона и Уайта [25] с использованием рентгеновского облучения. Изображенный на рис. 1 спектр зарядов показывает, что при ионизации внутренней оболочки йода в газообразном CH3J нейтральные фрагменты образуются редко (отношение атомарных ионов отражает долю данных атомов в молекуле). Кроме того, мы видим, что происходит целый ряд распадов, но наиболее вероятна реакция
CH3J + рентгеновские лучи- С2+ + 3Н+ + J5+ + 10 электронов. (1)
В этом случае три электрона переносятся, по-видимому, из метильной группы к йоду, поскольку следует ожидать, что свободный атом йода имеет заряд +8, так как этот элемент (Z — 53) находится рядом с Хе. Таким образом, два «добавочных» электрона, по-видимому, теряются при каком-то молекулярном процессе автоионизации. Примерно за 10~14 сек молекула превращается в крошечный рой положительных ионов, который затем расширяется. Измерялся также, спектр энергий ядер ртдачи. Для C2+40 его максимум находится примерно при 40 эв. Для Н+ и J5+ он лежит приблизительно при 34 и 9 эв соответственно. Эти энергии относятся к области химии «горячих атомов» или «высоких скоростей». Они хорошо согласуются с моделью «кулоновского взрыва». Получены, однако, указания на то, что уже в процессе появления заряда имеет место небольшое расхождение ионов [25]. Конденсированная среда. Разрушение молекул в результате эффекта Оже с последующим кулоновским отталкиванием было
качественно рассмотрено еще в 1941 г. [26] (см. также [27]). За исключением первоначальных переходов, которые, по существу, не зависят от окружающей среды, детали возникновения зарядов в конденсированных средах неизвестны. В жидкостях разрушения молекул надежно установлены [4].
Что касается действия радиации, то и образовавшиеся многократно заряженные положительные ионы, и испускаемые электроны ^ участвуют в создании маленьких химически активных областей возмущений. Первичные испускаемые электроны, так же как и один или несколько оже-электронов, могут иметь довольно большую энергию, но в случае легких атомов она не очень велика. Приближенное рассмотрение энергии связи дает для электронов, излучаемых в переходе K-+LL, энергию, примерно равную 500 эв и 250 эв для кислорода и углерода соответственно. Следует отметить, что эти энергии лежат в области, в которой сечения ионизации электронами особенно велики. К примеру, для оже-электронов из СН4 наблюдаемое значение равно (246,6^0,6) эв [28]. Следует ожидать, что «выброшенные» электроны, а также ряд других обладают в среднем гораздо меньшей энергией.
Как отмечал Платцман [1], тот факт, что при ионизации внутренней
оболочки могут образоваться высокоактивные участки с многочисленными
ионизациями и возбуждениями, дает 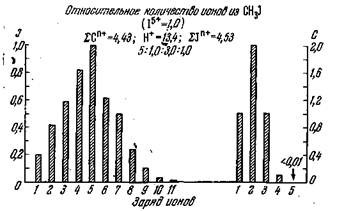
Рис. .1. Спектр зарядов ионов при разрушении йодистого метила [25].
возможность объяснить атомные смещения в твердых веществах, облучаемых электронами, в тех случаях, когда величина смещения при прямой передаче импульса очень мала. Необходимое условие осуществления механизмов такого типа состоит в том, что время, требуемое для снятия электронного возбуждения, должно превышать примерно 10-13 сек, т. е. время, необходимое для смещения атома. Для постлучевого эффекта при ионизации K-оболочки в диэлектриках это время, по-видимому, можно считать правильным. Некоторые исследования временной зависимости постлучевых эффектов были выполнены [29] с использованием эффекта Меесбауэра.
В работе [15] подчеркивалось, что многократные ионизации в ионных кристаллах происходят как в катионах, так и в анионах. Вместе с тем Варлей [30] отметил только пространственную нестабильность аниона, когда знак его заряда меняется под действием многократной ионизации. Смолуховский и др. [31] рассмотрели модификацию «механизма Варлея» с учетом снятия возбуждения при столкновении между положительными и отрицательными ионами одних и тех же элементов.
Теоретические значения выходов для ионизации внутренней оболочки. Метод, развитый Дурупом и Платцманом [15], содержит общие указания о способах вычисления абсолютных значений выходов для ионизации внутренних оболочек при полном поглощении падающих моноэнергетических электронов. Обобщая предложения Харта [32], эти авторы оставили символ G для измеряемого выхода и использовали, например, gk для обозначения теоретически найденного числа K-ионизации на 100 эв поглощенной энергии. Опубликованные ими численные результаты для кристаллов LiF и КСl показывают, что значение g для ионизации данной внутренней оболочки атома быстро падает по мере того, как первоначальная энергия электрона Т7, приближается к величине, в 100 раз меньшей соответствующей пороговой энергии (рис. 2). Такая зависимость позволяет осуществить экспериментальную проверку роли удаления электронов с различных внутренних оболочек при действии радиации. При наибольших значениях T0 вторичные электроны вносят существенный вклад в ионизацию K-оболочек даже в случае Cl и К- Поэтому плато на графике gK для этих атомов можно достичь лишь для самых больших значений Т0 (если оно вообще существует). При Т0 — 1 Мэв значения g k составляют около 0,16; 0,007; 0,0004 и 0,0003 для Li (Z = 3), F (Z = 9), Cl (Z = 17) и К (Z = 19) соответственно. Заметим, однако, что ионизация L-оболочки, по-видимому, сопровождается одним или двумя переходами Оже для случаев, подобных К и G1, у которых выход (при 1 Мэв) для субоболочек LI и LII, LIII приблизительно равен 20 gK и, 100 gK [15] (данные для других веществ см. ниже). Метод Дурупа и Платцмана применим также к ренгтеновскому и γ-из лучениям, которые воздействуют посредством создаваемых ими электронов. Позднее мы обсудим упрощенные вычисления.
Преобладающее количество электронов малой энергии, образуемых тяжелыми заряженными частицами; неспособно ионизовать K-оболочку. Вторичные частицы большой энергии встречаются очень редко [33]. Например, для падающих протонов gK можно рассчитать (см. последний раздел) из сечений ионизации К-оболочки [33, 34] и данных о полной тормозной способности облучаемого вещества.
Радиационная химия и радиобиология.
Вводные замечания. В первую очередь нас интересуют эффекты облучения, и поэтому мы не будем рассматривать (см. [4], [35]) образование внутриоболочечных вакансий в веществах с включенными радиоактивными ядрами. Однако последствия образования внутриоболочечной вакансии, по существу, не зависят от пути ее образования. Мы уже обсуждали некоторые наблюдаемые и предсказываемые эффекты, вызываемые внутриоболочечными вакансиями, созданными облучением, а также некоторые теоретические значения выходов испускания электронов с внутренних оболочек. В следующем разделе мы обсудим их более подробно.
Вода. В 1950 г. Платцман представил результаты вычислений, касающихся вырывания электронов с внутренних оболочек протонами в воде. Его данные остаются заслуживающим доверия приближением, несмотря на прогресс, достигнутый с тех пор в изучении проникновения протонов в вещество [33, 34, 36], а результаты, полученные для воды, примерно совпадают с данными для биологической среды.
Если полная энергия падающих протонов составляет, например, 3 Мэв или 1 Мэв, то доля ее, идущая на выбивание К-электронов кислорода в воде, равна соответственно около 4% и 1%. Общее число К-электронов, вырываемых из кислорода, быстро растет с увеличением первоначальной энергии протонов и равно примерно 10 и 80 при 1 и 3 Мэв соответственно. Эти числа соответствуют значениям gK (О) (выход в воде атомов кислорода с ионизированной ^-оболочкой) приблизительно равным 10 -3 и 2,7-10-3 соответственно. Платцман обнаружил, что даже в случае очень малых выходов таких процессов эти события происходят чаще, чем прямая передача «сильного» импульса всему атому.
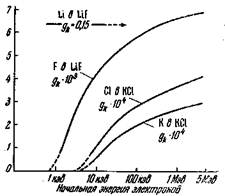
Рис. 2. Теоретические значения выхода ионизации K-оболочки LiF и КСl [15].
По оси ординат отложены gk -10n, величины п показаны у кривых.
Однако число дельта-электронов даже с энергиями, превышающими 500 эв, по-видимому, больше. Для электронов с энергией выше 50 кэв Дуруп и Платцман [16] нашли (предположив, что происходит полное их поглощение) gK (О) для воды порядка 0,01 числа ионизации К-оболочки атомов кислорода на 100 эв поглощенной энергии. Это означает, что около 5% всей поглощенной энергии первоначально должно передаться молекулам воды, атомы кислорода которых содержат внутриоболочечные вакансии. Добавляя эту энергию к энергии выбитого электрона, получим значительно большую долю падающей энергии, затраченную на ионизацию К-оболочки кислорода.
Приведенные выше данные о конечном заряде, приобретаемом изолированными атомами и молекулами, указывают, что часто молекулы воды несут больше двух зарядов, даже если энергетически возможен только один переход Оже (в данном случае в атоме кислорода). Хотя молекулярная связь делает второй переход Оже энергетически возможным, появление необходимой вакансии в Li-оболочке, по-видимому, не всегда является наиболее вероятным результатом первого перехода [37]. Нестабильность Н202+ и Н2О3+ в газовой фазе подтверждается отсутствием этих ионов в спектре масс [38].
В воде и других веществах, состоящих из малых молекул, образованных только легкими атомами, эффекты ионизации внутренних оболочек могут не играть заметной роли. Тем не менее детальный анализ, подобный анализу Платцмана [39] для сверхвозбужденных молекул воды, по-видимому, представляется интересным. В льде необычайно большие локальные возмущения подобного типа можно отличить от эффектов ионизации валентных электронов. Например, могут наблюдаться различия в их термолюминесценции.
Вместе с тем в средних или очень крупных молекулах соответствующее возмущение будет возникать (по крайней мере в основном) в самой молекуле и, даже если она не содержит атомов тяжелее С, N и О, соответствующая энергия равна приблизительно 300—500 эв. Эта энергия может оказаться особенно существенной, если молекула особо устойчива к воздействиям, сопровождающимся передачей малой энергии, или способна репарироваться после таких воздействий.
Углеводороды, белки и нуклеиновые кислоты. В случае полного поглощения электронов большой энергии теоретический выход gK (С) для ионизации Х-оболочки углерода, связанного в полиэтилене [16], примерно в 2,5 раза больше выхода gK (О) в воде, что нетрудно объяснить. К-электроны углерода легче отрываются, и, кроме того, они составляют 25% всех электронов С2Н4, тогда как К-электроны кислорода составляют только 20% от общего их числа в воде.
Качественно зависимость gK (С) для полиэтилена от начальной энергии электрона Т0 совпадает с приведенной в предыдущем разделе. Величины gK (С) равны 0; 0,01; 0,02 и 0,03 при значениях Т0, примерно равных 0,3; 1; 10 кэв и 3 Мэв соответственно. Выход, равный 0,03, означает, что ионизация К-оболочки составляет около 1% от всех ионизации, включая те, которые производятся электронами, возникающими при каждой ионизации К-оболочки.
Вычисления Дурупа и Платцмана [16] справедливы также для рентгеновского и γ-излучения при следующих упрощающих предположениях, вполне реальных для многих экспериментов: комптоновские электроны и фотоэлектроны поглощаются полностью, а фотоны, образовавшиеся при комптоновском рассеянии, не претерпевают дальнейших неупругих столкновений в облучаемом веществе. Для моноэнергетических фотонов большой энергии gк (С) для полиэтилена получается, как и ожидалось, приблизительно таким же, как и для электронов большой энергии. Подобным же образом при высоких энергиях gK медленно уменьшается с уменьшением энергии фотона, но в этом случае график gK проходит через широкий минимум. Такое поведение отражает возрастающий вклад фотоэлектрического эффекта при низких энергиях .
Результаты вычислений для полиэтилена легко распространяются на другие углеводороды. Специфика углеводорода определяется главным образом отношением числа атомов углерода н общему числу связанных электронов. Выход gK (С) пропорционален этому отношению, которое может меняться приблизительно на 50% от одного углеводорода к другому. Физическое состояние углеводорода, по существу, не влияет на величину gK. Даже если абсолютные значения теоретических выходов малы, они находятся в соответствии с наблюдаемыми значениями G для различных строго эндотермических процессов радиолиза ароматических углеводородов. Другие возможные причины следует, конечно, исключить, прежде чем можно будет сказать, что ионизация K-оболочки является преобладающим процессом. Это, по-видимому, будет не легкой задачей. Однако, как указывалось выше, предсказанная зависимость выходов от энергии падающих частиц вероятно поможет найти один из возможных путей ее решения.
Дуруп и Платцман распространили свои расчеты для электронного облучения и на некоторые белки. Было найдено, что при небольшой примеси серы gK (S) пренебрежимо мало, тогда как по оценке gK (S) составляет менее 10% от суммы значений gK для С, N и О (последняя величина составляет приблизительно 80% от значения gK (С) для полиэтилена). Следовательно, при воздействии электронами, так же как и при воздействии рентгеновским и γ -излучениями большой энергии при нормальных условиях, атомы серы не должны заметно увеличивать возможную роль, которую играет ионизация внутренних оболочек в молекуле белка.
Нуклеиновые кислоты не обсуждались явным образом теми же авторами. Несмотря на относительно большое содержание фосфора, следует ожидать, что величина £# (Р) составит только около 1% от суммы значений gK для С, N и О. Однако значение gL (P) должно быть по крайней мере сравнимо с этой величиной. Так как ионизация L-оболочки фосфора почти всегда приводит к переходам Оже, выход многократных ионизации при облучении нуклеиновых кислот (включая эффект Оже) может даже, как указывалось выше, превзойти довольно большое значение gK (С), вычисленное для полиэтилена.
Когда дело касается биологических макромолекул, физик вряд ли сможет отличить возмущения, вызванные переходами Оже, от эффектов, обусловленных вырыванием валентных электронов. Существуют некоторые экспериментальные исследования, которые, по-видимому, имеют отношение к данному вопросу. В этих исследованиях действия рентгеновского излучения авторы рассматривают преобладающую ионизацию К-оболочки, которая начинается после того, как энергия фотона превзойдет ее порог.
Уже 15 лет назад Гилд [41] пытался использовать это, чтобы решить, является ли ионизация атомов фосфора более эффективной для инактивации бактериофага Т 1, чем ионизация любой другой молекулы. Его гипотеза не подтвердилась. Манойлов [42] приписывал некоторые наблюдаемые радиационные повреждения ионизации К-оболочки железа (Z — 26) в цитохромной системе. Недавно Аддинк [43] пытался объяснить вызванное рентгеновским излучением отщепление жестко связанного цинка (Z = 30) от карбоангидразы результатом возмущения, вызванного переходом Оже. Однако два последних наблюдения имеют чисто качественный характер, и к тому же Гилд использовал только немо но энергетическое рентгеновское излучение.
Гомбергидр. [44] использовали монохроматические регулируемые источники рентгеновского излучения. В их планы входило изучение возможного радиационного эффекта TsT-резонанса в металлсодержащих ферментах и в хромосомах с введенными тяжелыми атомами. Положительные предварительные результаты были доложены. Сообщалось также [44] о возрастающей скорости образования F-центров в кристаллах КВr при К-резонансе в Вr(Z = 35). В таком случае следует ожидать заметной ионизации К-оболочки калия (Z = 19), а также ионизации L-оболочки брома, проявляющейся в флуоресцентном рентгеновском излучении, испускаемом бромом с ионизированной K-оболочкой. Выход K-флуоресценции для этих довольно тяжелых атомов превосходит 50%.
ЛИТЕРАТУРА
1. R.L.Platzman, в сб.: «Symposium on radiobiology», ed. J. J. Nick-son, J. Wiley a. Sons, 1952, Ch. 7.
2. H. В. Ф е д о p e н к о, УФН 68, 481 (1959).
3. С. F. P о w e 1 I, P. F. Fowler, D. H. P e г k i n sf The study of elementary particles by the photographic method, Perganion Press, 1959,
53
4. S. W e x 1 e г, в сб.: «Actions chimiques et biologiques des radiations», vol. 8, M. Haissinsky (ed4.), Masson, 1965, Ch. 3.
5. G. J. N e a r y, Int. J. Radiation Biol. 9, 477 (1965); J. R e a d, Physics Med. Biol. 2, 258 (1957/58).
6. W. P. McNutly, F. Hutchinson, Arch. Biochem. Biophys. 50, 92 (1954); E. G. P о 1 1 а г d, W. R. G u i Id, F. Hutchinson, R. B. S e t 1 о w, в сб.: «Progress in Biophysics», vol. 5, J. A. V. Butler, J. T. Randall (eds.), Pergamon Press, 1955, Ch. 3.
7. P. H о w а г d-F la n d e r s, в сб: «Advances in biological and medical physics», vol. 6, C. A. Tobias, J. H. Lawrence (eds.), Acad. Press, 1958, p. 553; Т. В r u s t a d, В сб.: «Advances in biological and medical physics», vol. 8, 1962, p. 161.
8. А. О r e, A. L a r s e n, Radiation Res. 21, 331 (1964).
9. A. M. R a u t h, J. A. Simpson, Radiation Res. 22, 643 (1964).
10. F. Hutchinson, Radiation Res., Suppl. 2, 49 (1960).
11. R. L. Platzman, J. Franc k, в сб.: «Symposium on information theory in biology», H. P. Yockey, R. L. Platzman, H. Ouastler (eds.), Pergamon Press, 1958, p. 262.
12. L. J. К i e f f e r, G. H. D u n n, Revs. Mod. Phys. 38, 1 (1966).
13. B. L. S с h r a m, A. J. H. В о e r b о m, J. К i s t e m a k e r, Physica 32, 185 (1966); B. L. S с h r a m, Physica 32,197 (1966); B. L. S с h г a m, lonization of noble gases and molecular gases by high energy electrons, Thesis, Univ. of Amsterdam Van Soest, 1966.
14. R. D. R i с h t m у e r, Phys. Rev. 49, 1 (1936); F. K. R i с h t m у e r, Revs. Mod. Phys. 9, 391 (1937).
15. J. D u r u p, R. L. Platzman, Disc. Faraday Soc. 31, 156 (1961).
16. J. D u r u p, R. L. P 1 a t z m a n, J. Ghim. Phys., в печати.
17. L. V. S p e n с e r, U. F a n о, Phys. Rev. 93, 1172 (1954).
18. A. J. С о m p t о n, S. K. A 1 1 i s о n, X-rays in theory and experiment, Van Nostrand, 1935; E. H. В u r h о p, The Auger effect, Univ. Press, 1952; M. A. L i s t e g a r t e n, The Auger effect, Bull. Akad. Nauk, SSSR, Phys. Ser. 24, 1050 (1960); I. Bergstrom, C. N о r d 1 i n g, в сб.: «Alpha-, betha- and gamma-ray spectroscopy», vol. 2, K. Siegbahn (ed.), North-Holland Publ. Co., 1965, Ch. 25.
19. F. P 1 e a s о n t о n, A. H. S n e 1 1, Proc. Roy. Soc. 241 A, 141 (1957).
20. T. A. Carlson, W. E. Hunt, M. О. К r a u s e, Phys. Rev., в печати.
21. Т. А. С а г 1 s о n, M. О. К r a u s e, Phys. Rev. 140A, 1057 (1965).
22. T. A. Carlson, личное сообщение.
23. Т. А. С а г 1 s о n, M. О. К r a u s e, Phys. Rev. 137A, 1655 (1965).
24. A. H. W a p s t r a, G. J. N e i j g h, R. van L i e s h о u t, Nuclear spectroscopy tables, North-Holland Publ. Co., 1959, p. 77.
25. T. A. Carlson, R. M. White, в сб.: «Symposium on the chemical effects of nuclear transformations», vol. 1, Int. Atomic Energy Agency, 1965, p. 23; Т. А. С a r 1 s о n, R. M. W h i t e, J. Ghem. Phys. 44, 4510 (1966).
26. D. D e V a u U, W. F. L i b b y, J. Am. Chem. Soc. 63, 3216 (1941).
27. E. P. Cooper, Phys. Rev. 61, 1 (1942).
28. W. M e h 1 h о г n, Z. Phys. 160, 247 (1960).
29. G. K. Wertlieim, H. J. Guggenheim, J. Ghem. Phys. 42, 3873 (1965); W. Т г i f t h a u s e r, P. C. Craig, Phys. Rev. Letters 16, 1161 (1966).
30. J. H. 0. Varley, Nature 174, 886 (1954); J. Nuclear Energy 1, 130 (1954); Proc. 1-st Internatl, Conf. peaceful uses atomic energy, Geneva, 1955, vol. 7, p. 242.
31. R. S m о 1 u с h о w s k i, D. A. W i e g a n d, Disc. Faraday Soc. 31, 151 (1961); R. E. Howard, S. V о s k o, R. S m 0 1 U t h о w s k i, Phys. Rev. 122, 1406 (1961).
32. Б, J, H а г t. J. Chem, Edup, 34, 586 (1957),
§3