Реферат: Взаимодействие хлорида неодима (III) с метагерманатом калия в этаноле
В.В.Девяткин
Германаты неодима типа Nd2 GeO5 и Nd 2Ge 2 O 7 получают по обычной керамической технологии или гидротермальным способом [1]. В последние годы получил развитие синтез указанных соединений в мягких условиях, с использованием в качестве растворителей водных и органических сред. Синтез осуществляется препаративными методами [2,3], не позволяющими наиболее полно изучить условия получения германатов определённого состава.
С целью изучения условий синтеза германатов неодима в неводных растворителях исследовано взаимодействие между компонентами системы NdCl3 – K2GeO3 – C2H5OH методом остаточных концентраций при 250С. В качестве исходных веществ использованы хлорид неодима “х.ч.” и синтезированный из GeO2 “ч.д.а.” и KOH по методике [4] метагерманат калия. При составлении смесей были взяты раствор NdCl3 в этаноле с концентрацией 3,9120 . 10-2 моль/л и раствор K2 GeО3 в этаноле с концентрацией 6,6152 . 10-2 моль/л. В реакционные сосуды вводился рассчитанный объём раствора K2 GeO3 и к нему добавлялся возрастающий объём раствора NdCl3 так, что отношение n(NdCl3) / n(K2GeО3 ) ( n) изменялось от 0,09 до 2,45. Растворы разбавлялись до 50 мл и перемешивались в течение 14 суток до установления равновесия. Жидкие и твёрдые фазы отделялись и анализировались на содержание ионов неодима (III) титрованием трилоном Б с ксиленоловым оранжевым в присутствии уротропинового буфера [5]. Cодержание ионов германия (IV) определялось гравиметрическим осаждением германомолибдата 8-оксихинолина [6,7]. Показатели активности ионов водорода p(aH+) регистрировались на pH-метре pH-150. Электропроводность (k) равновесных насыщенных растворов измерялась с помощью реохордного моста P-38.
Результаты и их обсуждение. Ранее проведённые исследования [8] показали возможность использования неводных сред для получения растворов хлорида неодима (III) определённой концентрации, зависящей от физико-химических характеристик растворителя и растворяемого вещества. Проведённый нами анализ растворимости K2 GeО3 в C2H5OH при 250 С показал значение 22,84 масс. %, соответственно растворимость NdCl3 в С2Н5ОН составила 0,74 масс. %. Безводный хлорид неодима, как и любой сильный электролит, в данном случае имеет небольшую растворимость, которая увеличивается в зависимости от содержания в растворе воды. Малая энергия активации и небольшая сила кислоты-катиона Nd3+ в сравнении с К+ обусловливают меньшую растворимость NdCl3 в C2H5OH, в отличие от K2 GeO3 .
Использование протолитических растворителей (C2H5OH, ЭТГ, глицерин) способствует более сильной сольватации анионов GeO32– и Cl–, увеличению энергии связи с молекулами растворителя, в отличие от апротонных (ДМФА). Поэтому в воде или спиртах реакции образования германатов протекают в тысячи раз медленнее, чем в ДМФА [9], хотя растворимость исходных компонентов в первом случае больше [10].
Проведённые исследования взаимодействий в системе NdCl3 – K2GeO3 – C2H5OH представлены в табл.1 и на рис.1. По мере увеличения отношения компонентов ( n) в исходных растворах от 0,09 до 2,45 остаточные концентрации германат-ионов уменьшаются от 3,55 . 10-4 до 0,12 . 10-4 моль/л. В интервале n < 1,61 ионы неодима (III) в равновесной жидкой фазе отсутствуют, так как полностью реагируют с германат-ионами (точки 1-10). Количества вступивших во взаимодействие компонентов указывают, что в щелочной среде (p(aH+) = 14,30 – 13,99) в интервале 0,26<n<0,59 простого соосаждения ионов не происходит, образуются равновесные твёрдые фазы постоянного состава. Соотношение неодима (III) и германия (IV) в твёрдой фазе равно 1 (точки 2-4). В интервале 1,78 < n < 2,28 реакция cреды кислая ( p(aH+) = 4,78-3,79), неодим также связывается в строгой стехиометрии с германат-ионами, в результате чего образуются твёрдые фазы с отношением указанных компонентов, равным 2 (точки 11-14). Полученные данные подтверждаются изменениями значений p(aH+) и электропроводности (k) растворов. В интервале 0,76 < n < 1,61 образуются твёрдые фазы переменного состава с избыточным содержанием неодима.
Полученные твёрдые фазы представляют собой мелкокристаллические вещества, интенсивность окраски которых изменяется от белого (сосуд № 1) до светло-фиолетового цвета (сосуд № 15) и зависит от соотношения исходных компонентов в растворе. Твёрдые фазы были отведены от жидких фаз, промыты спиртом и эфиром до отрицательного аналитического сигнала на ионы K+ (тетрафенилборат) и Сl– (нитрат серебра) [11]. Анализ спиртовой вытяжки с соотношением n > 2,28 показывает присутствие несвязанных ионов Nd3+, что свидетельcтвует о частичном соосаждении неодима (III) в указанном интервале. Анализ промытых и высушенных при 2500С твёрдых фаз указывает, что в интервале n<1,44 сохраняется отношение компонентов, равное 1. В интервале n > 1,78 соотношение равно 2. После прокаливания (5000С) промытых мелкодисперсных фаз и их химического анализа установлено, что состав твёрдых фаз соответствует соединениям Nd2 Ge 2O7 и Nd2GeO5 , представляющим собой мелкокристаллические вещества, не растворимые в воде.
Таблица 1
Результаты исследования системы NdCl3 – K2GeO3 – C2 H5OH
|
№ п/п |
Взято Nd3+ моль . 104 |
Отношение n (Nd3+) / n (Ge4+) в исх. р-ре |
Найдено в жидкой фазе моль . 104 |
Прореагировало моль . 104 |
Отношение n (Nd3+) / n (Ge4+) в твёрдой фазе |
Свойства жидкой фазы | |||
| Nd3+ | Ge4+ | Nd3+ | Ge4+ | p(аН+) | k . 103 Ом-1 . см-1 | ||||
|
1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. |
0,39 1,18 1,96 2,74 3,52 4,3 5,09 5,87 6,65 7,43 8,22 9,00 9,78 10,56 11,35 |
0,09 0,26 0,42 0,59 0,76 0,92 1,1 1,27 1,44 1,61 1,78 1,95 2,11 2,28 2,45 |
— — — — — — — — — — 0,49 0,58 0,71 0,79 0,93 |
3,55 3,45 2,67 2,06 1,77 1,45 1,22 1,05 0,81 0,71 0,6 0,42 0,33 0,18 0,12 |
0,39 1,18 1,96 2,74 3,52 4,3 5,09 5,87 6,65 7,43 7,73 8,42 9,07 9,77 10,42 |
1,08 1,18 1,96 2,57 2,86 3,18 3,41 3,58 3,79 3,92 4,03 4,21 4,3 4,45 4,51 |
0,36 1,00 1,00 1,07 1,23 1,35 1,49 1,64 1,76 1,90 1,92 2,00 2,11 2,20 2,31 |
14,34 14,30 14,17 13,99 13,86 13,59 13,47 11,23 8,97 6,04 4,78 4,11 3,98 3,89 3,79 |
2,57 2,29 2,05 1,70 1,14 0,83 0,60 0,50 0,47 0,53 1,43 1,87 1,98 2,01 2,10 |
Взято n (K2GeO3 ) = 4,6306 . 10-4 моль. Объём каждой смеси 50 мл.
| № | Nd | Ge | |
| 1. | Найдено, % : | 52,83 | 26,55 |
|
Вычислено для Nd2Ge2O7, % : |
52,87 | 26,61 | |
| 2. | Найдено, % : | 65,36 | 16,42 |
|
Вычислено для Nd2 GeO5, % : |
65,41 | 16,46 |
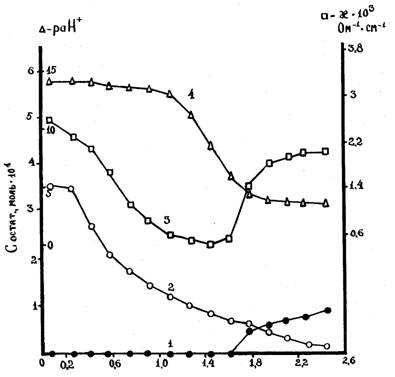
Отношение n (Nd3+) / n (Ge4+) в исходном растворе
Рис.1. Кривые остаточных концентраций ионов Nd3+ (1), Ge4+(2), электропроводность (3) и раН+ (4) жидких фаз.
Список литературы
Тананаев И.В., Шпирт М.Я. Химия германия. М.: Химия, 1967. С.146.
Тананаев И.В., Шпирт М.Я., Сендульская Т.И. // Докл. АН СССР. 1961. Т.139. С.907.
Зворыкин А.Я., Перельман Ф.М., Бабиевская И.З. // Журн.неорган.химии. 1960. Т.5. С.1717.
Schwarz R., Heinrich F.// Z.anorg. algem. Chem. 1932. B.43. S.205.
Шварценбах Г., Флашка Г. Комплексонометрическое титрирование. М.: Химия, 1970. С.249.
Назаренко В.А. Аналитическая химия германия. М.: Наука, 1973. С.103.
Алимарин И.П., Алексеева О.А. // Журн. прикл. химии. 1940. Т.13. С.1393.
Рунов Н.Н., Исаева Л.В. // Физико-химические исследования равновесий в растворах. Ярославль: ЯГПИ, 1983. Вып.202. С.26.
Фиалков Ю.Я. Растворитель как средство управления химическим процессом. Сер. “Химия”. М.: Знание, 1988. Вып.6. 48 с.
Химия редких и рассеянных элементов / Под ред. Большакова К.А. М.: Высшая школа, 1969. Т.1. С.176.
Резников А.А., Муликовская Е.П., Соколов И.Ю. Методы анализа природных вод. М.: Недра, 1970. 488 с.