Статья: Фармакологические свидетельства присутствия 5-НТ рецепторов в нервно-мышечном соединении брюхоногих моллюсков
Н.Л. Кононенко, В.В. Жуков
Исследовано влияние аппликации серотонина и его двух антагонистов (миансерина и метерголина) на сокращения дорсальной продольной мышцы гастроподного моллюска Lymnaea staganalis L., вызванные электрическим раздражением n. cervicalis inferior. Установлено, что увеличение концентрации серотонина в физиологическом растворе вызывало двоякое действие: в концентрации 2×10 -8 – 10 -6 М он усиливал мышечные сокращения, а в концентрациях свыше 10 -5, напротив, ослаблял. Блокирующее действие антагонистов серотонина на амплитуду вызванных сокращений возрастало с увеличением их концентраций в исследованном диапазоне от 10 -5 – 10 -3 М (для миансерина) и от 5×10 -8 – 10 -4 М (для метерголина). Предполагается, что 5-HT рецепторы, участвующие в нервно-мышечной передаче в исследованном соединении, имеют иной фармакологический профиль, чем 5-HТ рецепторы позвоночных животных.
Введение
Основной объем сведений о механизмах нервно-мышечной передачи дают исследования синапсов на мускулатуре позвоночных и членистоногих животных. Соответствующие эксперименты, проведенные на брюхоногих моллюсках, сравнительно немногочисленны. И это притом, что разнообразие как гистологии и свойств мышечных волокон, так и их функциональных взаимоотношений с нейронами у брюхоногих может быть не меньше, чем у животных других систематических групп. Так же, как и у членистоногих, каждая мышечная клетка этих животных может быть иннервирована функционально различными типами волокон – как возбуждающими (фазными или тоническими), так и тормозными [1]. Сами мышечные волокна могут быть связаны между собой электрически, что в большинстве случаев оставляет открытым вопрос о числе и типе иннервирующих их аксонов, которые могут образовывать на миоцитах многочисленные окончания [2]. Столь же разнообразной представляется химическая природа медиаторов нервно-мышечной передачи у этих животных. Наиболее распространенными типами нейротрансмиттеров являются соединения группы моноаминов (ацетилхолин, серотонин, дофамин), а также аминокислоты (глутамин) и нейропептиды (FMRF-амид) [3 – 6]. Поэтому любые исследования, дополняющие пока еще сравнительно разрозненную картину сведений о нервно-мышечной передаче брюхоногих моллюсков, важны для эволюционного анализа физиологических функций животного организма.
В качестве модели исследования было выбрано нервно-мышечное соединение n. cervicalis inferior с продольной дорсальной мышцей Lymnaea stagnalis, которая является одним из эффекторов оборонительного рефлекса [7]. Известно, что тела управляющих этой мышцей мотонейронов обнаружены в большинстве ганглиев ЦНС моллюска [8]. Эти нейроны принимают возбуждающие сигналы с механо- и фоторецепторов кожной поверхности тела и направляют свои аксоны к указанной мышце в составе n. cervicalis inferior и n. cervicalis superior [9; 10]. Сведения о структурной организации синапсов, присутствующих на миоцитах продольной дорсальной мышцы Lymnaea stagnalis в литературе отсутствуют. Однако предыдущими исследованиями было показано угнетающее действие двухвалентных катионов на амплитуду вызванных мышечных сокращений, что может свидетельствовать о химическом механизме нервно-мышечной передачи [11]. Одновременно было показано участие в этом процессе серотонинергических механизмов и соответствующих рецепторов. Настоящая работа представляет собой шаг в направлении детализации их фармакологических свойств этих механизмов.
Материалы и методы
Животные. Опыты выполнены на взрослых особях Lymnaea stagnalis (высота раковины около 3 см), собранных в прудах Калининграда, которых содержали в лабораторных условиях.
Препарат состоял из ноги и мантии моллюска, рассеченной по средней линии. Центральный конец нерва, n. cervicalis inferior (номенклатура по [12]), иннервирующего дорсальную продольную мышцу (название мышцы дается по [13]), помещали во всасывающий электрод.
Состав физиологического раствора (мМ): NaCl – 40; KCl – 3; CaCl2 – 3; MgCl2 – 1. Значение РН = 7,5 – 7,6 поддерживали карбонатным буфером (NaHCO3).
Исследуемые вещества. В ходе экспериментов применяли серотонин (5-НТ), миансерин и метерголин (Sigma Chemical Co). Маточные растворы веществ готовили на дистиллированной воде (серотонин, миансерин) или на 0,1 Н растворе HCl (метерголин). Рабочие растворы получали путем разведения маточных в физиологическом.
Оборудование. Датчик для регистрации сокращения мышцы был изготовлен из пары проволочных тензосопротивлений, наклеенных на противоположные стороны полоски гибкой пленки [14]. Сопротивление тензодатчика изменялось при деформации пленки, вызванной натяжением лески, прикрепленной с помощью металлического крючка к исследуемой мышце. Исходное натяжение лески устанавливали вручную винтом манипулятора. Тензосопротивления включали в схему мостика Уитстона, с которого электрический сигнал подавали на вход усилителя постоянного тока. Усиленный сигнал поступал на осциллограф С1-67 и чернильный автоматический потенциометр К-201 (Германия).
Стимуляцию нерва осуществляли сериями электрических импульсов (длительностью 2 мс, амплитудой около 5 В), которые подавали на хлорсеребряный электрод, вмонтированный в трубочку всасывающего электрода. Второй хлорсеребряный электрод помещали в физиологический раствор в экспериментальной камере.
Ход эксперимента
1. Электрическая стимуляция препарата в физиологическом растворе.
2. Замена физиологического раствора на растворы веществ и спустя 10 минут электрическая стимуляция нерва. Перед каждым новым раствором с последовательно увеличивающейся концентрацией вещества препарат промывали в физиологическом растворе в течение 30 минут.
3. Промывка препарата в физиологическом растворе в течение 30 минут и электрическая стимуляция.
Статистическая оценка полученных результатов проводилась по Т-критерию Уилкоксона [15].
Результаты
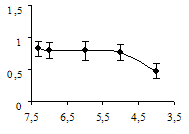
Аппликация серотонина в концентрациях в диапазоне от 2×10-8 М до 10-6 М усиливала мышечные сокращения, причем эффект наблюдался спустя 10 минут после добавления вещества в ванночку и мог сохраняться на протяжении получаса после возврата к физиологическому раствору. Более высокие концентрации серотонина (10-5 М и выше), напротив, снижали амплитуду мышечных сокращений. Максимальный усиливающий эффект серотонина проявлялся при его концентрации в ванночке около 10-7 М (рис. 1). Эта концентрация серотонина сама по себе вызывала небольшое укорочение мышцы. Изменения амплитуды сокращений, которые наблюдались в присутствии серотонина 10-8 и 10-6 М, статистически не подтверждались.

Рис. 1. Концентрационная зависимость влияния серотонина на сокращения дорсальной продольной мышцы Lymnaea stagnalis L., вызванные ритмической стимуляцией n. cervicalis inferior:
ось абсцисс – отрицательный десятичный логарифм концентрации серотонина в нормальном физиологическом растворе; ось ординат – отношение амплитуды мышечных сокращений в растворе серотонина к амплитуде мышечных сокращений в физиологическом растворе; вертикальные линии – стандартное отклонение (n = 5)
Аппликация миансерина снижала амплитуду вызванных сокращений. Статистически значимый эффект миансерина проявлялся в концентрациях от 10-4 до 10-3 М (рис. 2а). Более низкие концентрации миансерина (5×10-5 М и ниже) статистически выявляемого влияния на амплитуду мышечных сокращений не оказывали. Эффект действия миансерина, в отличие от серотонина, проявлялся непосредственно после его аппликации.
Аппликация метерголина также снижала амплитуду вызванных мышечных сокращений. Однако статистически значимый эффект метерголина проявлялся в концентрациях от 10-5 до 10-4 М (рис. 2б). Эффект действия метерголина проявлялся спустя 15 минут после его аппликации.
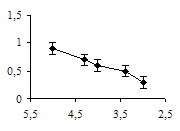
а б
Рис. 2. Концентрационные зависимости влияния миансерина (а) и метерголина (б) на сокращения дорсальной продольной мышцы Lymnaea stagnalis L., вызванные ритмической стимуляцией n. cervicalis inferior: оси абсцисс – отрицательный десятичный логарифм концентраций исследованных препаратов в нормальном физиологическом растворе; оси ординат – отношение амплитуды мышечных сокращений в физиологическом растворе к амплитуде мышечных сокращений в метерголине или миансерине; вертикальные линии – стандартное отклонение (n = 5)
Обсуждение
Усиливающее действие серотонина (5-HT) на нервно-мышечную передачу было отмечено у многих видов моллюсков [3 – 5]. Известно, что действие этого вещества проявляется через большое количество типов и субтипов рецепторов. К настоящему времени у позвоночных животных было клонировано семь различных 5-HT рецепторов: 5-HT1A, 5-HT1B, 5-HT1C, 5-HT1Da, 5-HT1Db, 5-HT2 и фармакологически не охарактеризованный 5-HT рецептор человека [16]. Однако сведения о 5-HT рецепторах в нервной системе беспозвоночных в большинстве случаев отрывочны и не поддаются классификации, установленной для позвоночных животных.
Как показали наши наблюдения, серотонин усиливает, а его антагонисты – миансерин и метерголин – подавляют амплитуду вызванных сокращений дорсальной продольной мышцы. Возможно, что механизм увеличения амплитуды вызванных мышечных сокращений в присутствии серотонина может указывать на возможную роль последнего как медиатора нервно-мышечной передачи. В этом случае взаимодействие экзогенного серотонина с синаптическими 5-HT рецепторами мышечных клеток может приводить к их деполяризации и повышению возбудимости. Частичное сокращение исследуемой мышцы при добавлении серотонина в физиологический раствор, вероятно, согласуется с таким предположением. Исчезновение усиливающего действия экзогенного серотонина при повышении его концентрации до 10-6 М мы склонны объяснять развивающейся десенситизацией 5-HT рецепторов. Угнетающее действие антагонистов серотонина на мышечные сокращения также может быть следствием их взаимодействия с синаптическими рецепторами. В наших опытах метерголин и миансерин проявляли свое действие в значительно более высоких концентрациях по сравнению с серотонином. В таких концентрациях эти вещества могут блокировать одновременно 5-HT1A и 5-HT2 типы серотониновых рецепторов, обнаруженные у L. stagnalis, фармакологический профиль которых в исследованных гигантских церебральных клетках совпадает с профилем этих рецепторов у позвоночных [17 – 19]. Поэтому влияние низких концентраций серотонина можно было бы объяснить взаимодействием его молекул с другим типом серотониновых рецепторов, например 5-HT3. Последний был обнаружен в нервной системе L. stagnalis при исследовании фармакологических свойств нейронов церебрального ганглия [20].
К настоящему моменту известно, что набор агонистов и антагонистов для 5-HT рецепторов беспозвоночных значительно отличается от набора фармакологических агентов 5-HT рецепторов позвоночных животных. К примеру, константа диссоциации (Ki, нМ) для метерголина в отношении 5-HTlym составляет 55, а при связывании с 5-HT1 и 5-HT2 рецепторами позвоночных животных 10 и 2,1 соответственно [21, 16]. Отмечается, что 5-HT рецепторы беспозвоночных животных характеризуются иными фармакологическими и функциональными свойствами, чем рецепторы позвоночных [22]. Кроме того, филогенетические различия между моллюсками и позвоночными животными настолько велики, что фармакологический профиль соответствующих рецепторов беспозвоночных видов вряд ли может быть полностью подобен профилю рецепторов позвоночных животных, поэтому требует для дифференциации других фармакологических агентов [23, 24]. Возможно, что в данном нервно-мышечном соединении присутствует особый тип серотониновых рецепторов, чей фармакологический профиль отличается от уже известных. Высокие же значения эффективных концентраций мианзерина и метерголина могут свидетельствовать о высоком значении константы диссоциации этих веществ для данного типа рецептора. По крайней мере, фармакологическая характеристика 5-HTLym рецептора, недавно полученного методом клонирования в культуре нервных клеток L. stagnalis, не совпадает ни с одним из фармакологических профилей 5-HT1 рецепторов позвоночных. На основе чего авторы сделали предположение о дополнительном субклассе – 5-HT1 – подобных рецепторов, еще не обнаруженном у позвоночных [16]. Для поиска ответа на вопрос: сходны ли свойства серотониновых рецепторов нервно-мышечного соединения и центральных нейронов моллюска L. stagnalis – необходимо существенно расширить спектр исследуемых соединений.
Авторы приносят благодарность профессорам Ф.-В. Шурману (университет Геттингена) и Г. Брилла за любезно представленные фармакологические препараты, а также К.А. Судоплатову за техническую помощь в организации экспериментов. Работа выполнена при финансовой поддержке грантов ИНТАС-РФФИ №97-04-71075 (IR-97-798) и Минобразования №97-0-10.0-207.
Список литературы
1. Muneoka Y., Twarog B. Neuromuscular transmission and excitation-contraction coupling in molluscan muscle // The Mollusca / Eds. A.S.M. Saleuddin, K.M. Wilbur. New-York; London: Academic Press, 1983. V. 4. P. 35 – 64.
2. Heyer C.B., Katert S.B., Karlsson U.L. Neuromuscular systems in mollusca // Amer. Zool. 1973. V. 13. P. 217 – 270.
3. Fox L.E., Lloyd P.E. Serotonergic neurons differentially modulate the efficacy of two motor neurons innervating the same muscle fibers in Aplysia // J. Neurophysiology. 1998. V.80. P. 647 – 655.
4. Versen B., Gokorsch S., Fiedler A., Schipp R. Monoamines and the isolated auricle of Sepia officinalis: are there b-like receptors in the heart of a cephalopod? // J. Exp. Biol. 1999. V. 202. P. 1067 – 1079.
5. Yoshida M., Kobayashi M. Modulation of the buccal muscle contraction by identified serotonergic and peptidergic neurons in the snail Achatina fulica // J. Exp. Biol. 1995. V. 198. 729 – 738.
6. Fox L.E., Lloyd P.E. Glutamate is a fast excitatory transmitter at some buccal neuromuscular synapses in Aplysia // J. Neurophysiology. 1999. V. 82. P. 1477 – 1488.
7. Cook A. The withdrawal response of a freshwater snail (Lymnaea stagnalis) // J. Exp. Biol. 1975. V.62. P. 783 – 796.
8. Ferguson G.P., Benjamin P.R. The whole-body withdrawal response of Lymnaea stagnalis. I. Identification of central motoneurones and muscles // J. Exp. Biol. 1991. V. 158. Р. 63 – 95.
9. Ferguson G.P., Benjamin P.R. The whole-body withdrawal response of Lymnaea stagnalis. II. Activation of central motoneurones and muscles of sensory input // J. Exp. Biol. 1991. V. 158. Р. 97 – 116.
10. Судоплатов К.А., Жуков В.В. Электрические реакции периферических нервов моллюска Lymnaea stagnalis на фотостимуляцию кожной поверхности // Журн. эволюц. биох. и физиол. 1999. Т. 35. №4. С. 274 – 280.
11. Жуков В.В., Кононенко Н.Л. Возможное участие серотонина в периферическом звене оборонительного рефлекса моллюска Lymnaea staganalis // Журн. эволюц. биохим. и физиол. 2002. Т.38. C.225 – 231.
12. Elo J.E. Das Nervensystem von Limnaea stagnalis (L.) Lam // Ann. Zool. Soc. Zool.-Bot. Fen. Vanamo. 1938. T. 6. №4. S. 1 – 40.
13. Plesh B., Janse C., Boer H. Gross morphology and hystology of the freshwater pulmonate Lymnaea stagnalis // Neth. J. Zool. 1975. V. 25. №3. P. 332 – 352.
14. Блаттнер Р., Классен Х., Денерт Х., Деринг Х. Эксперименты на изолированных препаратах гладких мышц. М., 1983.
15. Лакин Г.Ф. Биометрия. M., 1990.
16. Sugamori K.S., Sunahara R. K., Guan H.-C., Bulloch A.G., Tensen C.P., Seeman P., Niznik H.B., Van Tol H.H.M. Serotonin receptor cDNA cloned from Lymnaea stagnalis // Proc. Natl. Acad. Sci. 1993. V. 90. P. 11 – 15.
17. Hatakeyama P., Ito E. Three-dimensional reconstruction and mapping of serotonin-like immunoreactive neurons in the CNS of the pond snail, Lymnaea stagnalis, with the confocal laser scanning microscope // Bioimages. 1999. №7 (1). P. 1 – 12.
18. Walcourt-Ambakederemo A., Winlow W. 5-HT receptors on identical Lymnaea neurons in culture. Pharmacological characterization of 5-HT1A receptors // J. Comp. Biochem. Physiol. 1994. V. 107C. № 1. P. 129 – 141.
19. Walcourt-Ambakederemo A., Winlow W. 5-HT receptors on identical Lymnaea neurons in culture. Pharmacological characterization of 5-HT2 receptors // J. Gen. Pharmacology. 1995. V. 26. № 3. P. 553 – 561.
20. Walcourt-Ambakederemo A., Winlow W. 5-HT receptors on identical Lymnaea neurons in culture. Pharmacological characterization of 5-HT3 receptors // J. Gen. Pharmacology. 1994. V. 25. P. 1079 – 1092.
21. Peroutka S.J., Snyder S.H. Multiple serotonin receptors and their physiological significance // Federation Proc. 1983. V. 42. P. 213 – 217.
22. Zang B., Harris-Warrick R.M. Multiple receptors mediate the modulatory effects of serotonergic neurons in a small neural network // J. Exp. Biol. 1994. V. 190. P. 55 – 77.
23. Tierney A.J. Structure and function of invertebrate 5-HT receptors: a review // J. Comp. Bioch. and Physiol. Part A. 2001. V. 128. P. 791 – 804.
24. Tabor J.N., Cooper R.L. Physiologically identified 5-HT2-like receptors at the crayfish neuromuscular junction // Brain Research. 2002. V. 932. P. 91 – 98.