Реферат: Электроаналитические методы в аналитической химии
ГОУ ВПО «Курский Государственный Медицинский Университет»
Кафедра Фармацевтической, токсикологической и аналитической химии
Реферат по аналитической химии на тему
«Электроаналитические методы в аналитической химии»
Выполнил: Ларин С.Л.
Проверил: Артемьев
Геннадий Петрович
Курск, 2009
План
Введение
1. Циклическая вольтамперометрия
1.1 Хроноамперометрия
2. Вольтамперометрия с линейной разверткой потенциала
3. Кондуктометрия
4. Потенциометрия
5. Амперометрия
6. Кулонометрия
Введение
Одни из наиболее сложных электрохимических методов – электроаналитические методы – сегодня используются довольно часто, поскольку позволяют получить богатую экспериментальную информацию о кинетике и термодинамике многих химических систем. Электроаналитические методы позволяют получить доступ к уникальной информации о химических, биохимических и физических системах. Инструментальный базис и теоретические основы этих методов развиты до такой степени, что они легко могут применяться даже неспециалистами. Однако в настоящее время следует отметить невосприятие электроаналитических методов теми людьми, которые не имеют опыта их применения и в недостаточной степени знакомы с электрохимией. В настоящем реферате будут рассмотрены только важные электроаналитические методы вместе с наиболее существенной информацией о возможности их применения потенциальными пользователями, которые не имеют специальной подготовки в области электрохимии. В своем реферате я поставил следующие цели:
ü Рассмотреть наиболее важные электроаналитические методы
ü Выяснить пригодность каждого метода для определения различных ионов
ü Рассмотреть достоинства и недостатки каждого метода
1. Циклическая вольтамперометрия
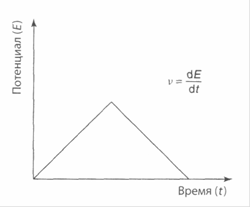
По мере восстановления на поверхности электрода окисленной формы Ох образуется восстановленная форма R, которая переходит обратно в раствор. При обратной развертке потенциала вблизи значения Е, равного окислительно-восстановительному потенциалу пары Ox-R, восстановленная форма вновь окисляется с образованием Ох. Ток при этом начинает возрастать в противоположном направлении до тех пор, пока не достигнет пикового значения. Подобный метод исследования называют циклической вольтамперометрией. На рисунке показано, как в этом методе изменяется наложенный на электроды потенциал в зависимости от времени.
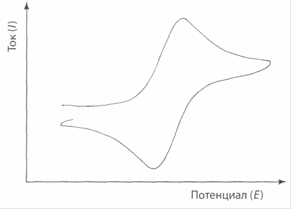
На типичной циклической вольтамперограмме видны два пика. Один из них отражает восстановление исходной окисленной формы, а другой - реокисление восстановленной формы с образованием исходного вещества. Пиковые токи практически одинаковы по величине, а соответствующие им потенциалы сдвинуты друг относительно друга на 0,056/nВ. Независимо от концентрации Ох, коэффициентов диффузии или скоростей электронного переноса, среднее арифметическое этих потенциалов равно стандартному окислительно-восстановительному потенциалу Е° пары Ox-R.
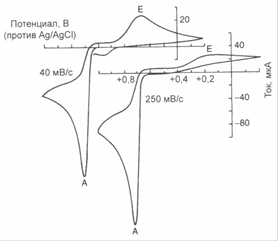
В том случае, если превращение на электроде протекает необратимо, пики будут сдвинуты друг относительно друга на большую величину: Eр(с) - Ep(a) > 0,056/n В. Однако и в этом случае среднее арифметическое пиковых потенциалов с хорошим приближением можно считать за Е°. Бывают случаи, когда обратный пик не возникает вовсе, либо он сильно отличается по форме от прямого пика. Обычно это указывает на полную необратимость процесса восстановления Ох за счет дальнейших превращений восстановленной формы R. В качестве примера можно привести циклическую вольтамперограмму 4-ацетиламинофенола (парацетамола) - вещества, легко окисляющегося наугольно-пастовом электроде.
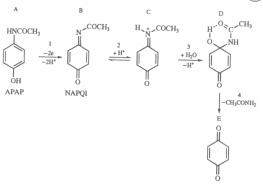
Пик, соответствующий окислению парацетамола, направлен вниз. При обратной развертке потенциала второй пик, отражающий электрохимическое восстановление, возникает на значительном удалении и гораздо шире первого. Подобные вольтамперограммы получены при трех скоростях развертки и при трех разных значениях рН. Их подробный а нализ позволил установить природу протекающих в электрохимической ячейке превращений.
1.1 Хроноамперометрия
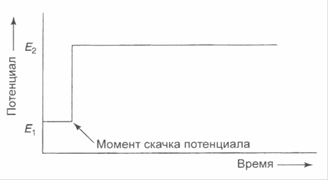
Другой метод анализа, в котором ток определяется скоростью диффузии аналита к электроду, — это хроноамперометрия. В несколько модифицированном виде этот метод представляет особый интерес для использования в биосенсорах. Суть его состоит в том, что разность потенциалов между электродами изменяется не равномерно, а скачкообразно, причем значение потенциала Е2 после скачка должно быть чуть после того значения, при котором в ходе вольтамп ерометрии с линейной разверткой возникает пика анодного или катод-ного тока. При этом сначала возникает пик тока, а затем следует его падение, что обусловлено коллапсом двойного электрического слоя в приэлектродном пространстве в соответствии с рис.2.10. Наиболее простое решение уравнений диффузии Фика приводит к уравнению Котгрелла, в соответствии с которым диффузионный ток (id) падает обратно пропорционально квадратному корню времени:
![]()
С помощью хроноамперометрии можно определить любую из переменных, фигурирующих в уравнении при условии, что известны остальные переменные. Обычно это уравнение используют для определения n, А или D, реже - С.
2. Вольтамперометрия с линейной разверткой потенциала
Термины вольтамперометрия и амперометрия относятся к методам, при которых на клеммы электродов электрохимической ячейки накладывается изменяющийся потенциал; при этом в ячейке имеются так называемые электроактивные (то есть способные к окислению или восстановлению) соединения, а проводимость внутри ячейки обеспечивается индифферентным, или поддерживающим, электролитом.
Ток через ячейку постоянно измеряется, в результате чего возникает кривая зависимости тока от наложенного потенциала, которую называют вольтамперограммой.
Наиболее простой вариант метода- это волътамперометрия с линейной разверткой потенциала. Типичная вольтамперограмма показана на рисунке.
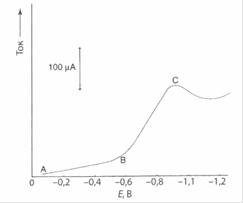
В начале кривой (точка А) ток небольшой. Между точками А и В очень медленный подъем кривой обусловлен остаточным (или примесным) током и зарядкой двойного слоя на границе электрода с раствором. Этот ток иногда называют фоновым. В точке В наложенный потенциал приближается к потенциалу восстановления частиц, находящихся в окисленном состоянии (Ох). При дальнейшем увеличении потенциала электроны с возрастающей скоростью переходят с электрода на Ох в соответствии со следующим уравнением реакции:
Все возрастающая скорость восстановления приводит к увеличению тока через ячейку. Можно показать, что общий ток через ячейку в этой области кривой слагается из катодного тока, или тока восстановления (г'с), и анодного тока.
По мере увеличения наложенного потенциала Е возрастает iс и падает ia, что и вызывает наблюдаемый подъем вольтамперометрической волны. Однако этот подъем не бесконечен: концентрация Ох в приэлектродном пространстве падает за счет его восстановления, а скорость Ох из раствора к электроду ограничена. В результате в точке С ток достигает своего пикового значения (рис. 2.9).
Влияние скорости диффузии Ох на величину диффузионного тока id определяется первым законом диффузии Фика, согласно которому:
Поток вещества к поверхности электрода = dN/dt = D dC/dx,
Второй закон диффузии Фика описывает уменьшение концентрации вещества в данной точке пространства во времени.
В приведенных выше уравнениях С — это концентрация вещества (например, Ox), N - его количество в молях, D — коэффициент диффузии, а х — расстояние от поверхности электрода.
3. Кондуктометрия
Кондуктометрия основана на измерении электропроводности раствора и применяется для определения концентрации солей, кислот, оснований и т.д. При кондуктометрических определениях обычно используют электроды из одинаковых материалов, а условия их проведения подбирают таким образом, чтобы свести к минимуму вклад скачков потенциала на обеих границах раздела электрод/электролит (например, используют переменный ток высокой частоты). В этом случае основной вклад в измеряемый потенциал ячейки вносит омическое падение напряжения IR, где R – сопротивление раствора. Электропроводность однокомпонентного раствора можно связать с его концентрацией, а измерение электропроводности электролитов сложного состава позволяет оценить общее содержание ионов в растворе и применяется, например, при контроле качества дистиллированной или деионизованной воды. В другой разновидности кондуктометрии – кондуктометрическом титровании – к анализируемому раствору порциями добавляют известный реагент и следят за изменением электропроводности. Точка эквивалентности, в которой отмечается резкое изменение электропроводности, определяется из графика зависимости этой величины от объема добавленного реагента.
4. Потенциометрия
Потенциометрия применяется для определения различных физико-химических параметров исходя из данных о потенциале гальванического элемента. Электродный потенциал в отсутствие тока в электрохимической цепи, измеренный относительно электрода сравнения, связан с концентрацией раствора уравнением Нернста. В потенциометрических измерениях широко применяются ионоселективные электроды, чувствительные преимущественно к какому-то одному иону в растворе: стеклянный электрод для измерения рН и электроды для селективного определения ионов натрия, аммония, фтора, кальция, магния и др. В поверхностный слой ионоселективного электрода могут быть включены ферменты, и в результате получается система, чувствительная к соответствующему субстрату. Отметим, что потенциал ионоселективного электрода определяется не переносом электронов, как в случае веществ с электронной проводимостью, а в основном переносом или обменом ионов. Однако уравнение Нернста, связывающее электродный потенциал с логарифмом концентрации (или активности) вещества в растворе, применимо и к такому электроду. При потенциометрическом титровании реагент добавляют в анализируемый раствор порциями и следят за изменением потенциала. S-образные кривые, характерные для такого типа титрования, позволяют определить точку эквивалентности и найти такие термодинамические параметры, как константа равновесия и стандартный потенциал.
5. Амперометрия
Амперометрия. Метод основан на измерении предельного диффузионного тока, проходящего через раствор при фиксированном напряжении между индикаторным электродом и электродом сравнения. При амперометрическом титровании точку эквивалентности определяют по излому кривой ток – объем добавляемого рабочего раствора. Хроноамперометрические методы основаны на измерении зависимости тока от времени и применяются в основном для определения коэффициентов диффузии и констант скорости. По принципу амперометрии (как и вольтамперометрии) работают миниатюрные электрохимические ячейки, служащие датчиками на выходе колонок жидкостных хроматографов. Гальваностатические методы аналогичны амперометрическим, но в них измеряется потенциал при прохождении через ячейку тока определенной величины. Так, в хронопотенциометрии контролируется изменение потенциала во времени. Эти методы применяются главным образом для изучения кинетики электродных реакций.
6. Кулонометрия
В кулонометрии при контролируемом потенциале проводят полный электролиз раствора, интенсивно перемешивая его в электролизере с относительно большим рабочим электродом (донная ртуть или платиновая сетка). Полное количество электричества (Q, Кл), необходимое для электролиза, связано с количеством образующего вещества (А, г) законом Фарадея:
A=QM/nF
Кулонометрическое титрование заключается в том, что при постоянном токе электролитически генерируют реактив, вступающий во взаимодействие с определяемым веществом. Ход титрования контролируют потенциометрически или амперометрически. Кулонометрические методы удобны тем, что являются по своей природе абсолютными (т.е. позволяют рассчитать количество определяемого вещества, не прибегая к калибровочным кривым) и нечувствительны к изменению условий электролиза и параметров электролизера (площади поверхности электрода или интенсивности перемешивания). При кулоногравиметрии количество вещества, подвергшегося электролизу, определяют взвешиванием электрода до и после электролиза.-где M – мол. масса (г/моль), F . Существуют и другие электроаналитические методы. В переменно-токовой полярографии на линейно меняющийся потенциал налагают синусоидальное напряжение малой амплитуды в широкой области частот и определяют либо амплитуду и фазовый сдвиг результирующего переменного тока, либо импеданс. Из этих данных получают информацию о природе веществ в растворе и о механизме и кинетике электродных реакций. В тонкослойных методах используются электрохимические ячейки со слоем электролита толщиной 10–100 мкм. В таких ячейках электролиз идет быстрее, чем в обычных электролизерах. Для изучения электродных процессов применяют спектрохимические методы со спектрофотометрической регистрацией. Для анализа веществ, образующихся на поверхности электрода, измеряют поглощение ими света в видимой, УФ- и ИК-областях. За изменением свойств поверхности электрода и среды следят с помощью методов электроотражения и эллипсометрии, которые основаны на измерении отражения излучения от поверхности электрода. К ним относятся методы зеркального отражения и комбинационного рассеяния света (рамановская спектроскопия), спектроскопия второй гармоники (фурье-спектроскопия).
Заключение
На сегодняшний день электроаналитические методы определения веществ – одни из самых перспективных в аналитической химии. Это связано прежде всего с их чувствительностью и возможностью определять малые концентрации ионов. Тем не менее есть и недостатки, среди которых следует отметить достаточную дороговизну оборудования и необходимость использования вспомогательных средств измерения. Однако на сегодняшний день не существует другого метода способного видеть 10-9-10-8 концентрации ионов. В связи с этим эти методы остаются перспективными и многообещающими для исследований в аналитической химии. Именно поэтому следует изучать теоретические основы методов и принципы их работы. В своем реферате я постарался раскрыть принципы только самых основных и известных электроаналитических методов. Но наука не стоит на месте и методы совершенствуются им на смену приходят новые более совершенные и чувствительные.
Литература
1. Виноградова Е.Н., Галлай З.А., Финогенова З.М. Методы полярографического и амперометрического анализа. М., изд-во МГУ, 1999
2. Рейшахрит Л.С. Электрохимические методы анализа. Ленинград, изд-во ЛГУ, 1998
3. Зозуля А.П. Кулонометрический метод анализа М. Химия, 2000
4. Выдра Ф., Штулик К., Юлакова Э Инверсионная вольтамперометрия. М. Мир, 2007, 278 с.
5. Камман К. Работа с ионселективными электродами. М.,Изд-во "Мир",. 1999, 283 с.
6. Ф. Штольц «Электроаналитические методы», Москва, 2006
| Общая и неорганическая химия | |
|
Квантово-механическая модель атома. Квантовые числа. Атомные орбитали. Порядок заполнения орбиталей электронами Теория строения атома основана на ... Так, например, стандартный редокс-потенциал электрохимической реакции Fe3+ -e < > Fe2+ равен потенциалу платиновой пластинки при 250 С в растворе, содержащем по одному г-иону ионов ... Вспомогательный электрод (или противоэлектрод) обеспечивает возможность пропускания тока через электрохимическую ячейку, а электроды сравнения - возможность измерения потенциала ... |
Раздел: Рефераты по химии Тип: учебное пособие |
| Коллоидная химия | |
|
ВВЕДЕНИЕ Предметом физической химии является объяснение химических явлений на основе более общих законов физики. Физическая химия рассматривает две ... Величина преимущественного передвижения иона в направлении одного из электродов при прохождении тока через раствор отнесённая к градиенту потенциала 1 В/см, есть абсолютная ... Электрохимическое равновесие на электроде можно рассматривать в следующем виде: |
Раздел: Рефераты по химии Тип: учебное пособие |
| Методы анализа лекарственных препаратов | |
|
Оглавление Вступление Глава 1. Основные принципы фармацевтического анализа 1.1 Критерии фармацевтического анализа 1.2 Ошибки, возможные при проведении ... Потенциометрическое определение рН основано на измерении электродвижущей силы элемента, составленного из стандартного электрода (с известным значением потенциала) и индикаторого ... Особенно перспективна ионометрия, использующая зависимость между ЭДС гальванической сети с ионоселективным электродом и концентрацией анализируемого иона в электродной ячейке цепи. |
Раздел: Рефераты по медицине Тип: дипломная работа |
| Разработка источников диффузионного легирования для производства ... | |
|
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ УКРАИНЫ Херсонский государственный технический университет Кафедра Физической электроники и энергетики ПОЯСНИТЕЛЬНАЯ ... В работе были разработаны поверхностные источники для диффузии бора и фосфора на основе спиртовых растворов борной и ортофосфорной кислот. Основной параметр СЭ - световая нагрузочная ВАХ - позволяет определить генерируемую электрическую мощность по произведению Im=Um (максимальные рабочие ток и напряжение), оценить ... |
Раздел: Промышленность, производство Тип: дипломная работа |
| Электричество и магнетизм | |
|
ОБЩИЙ ФИЗИЧЕСКИЙ ПРАКТИКУМ ЭЛЕКТРИЧЕСТВО И МАГНЕТИЗМ Ставрополь 2005 ФЕДЕРАЛЬНОЕ АГЕНТСТВО ПО ОБРАЗОВАНИЮ СТАВРОПОЛЬСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ ... ... внешних условий (температуры, влажности и т.д.) Выход может быть найден в замене электростатического поля неподвижных зарядов полем постоянного электрического тока при условии, что ... Вдали от электродов концентрация ионов (положительных и отрицательных) одинакова в разных точках электролита, вследствие этого градиент концентрации ионов внутри электролитов равен ... |
Раздел: Рефераты по физике Тип: книга |